科普·直播义诊专区 查看全部
- 精选 不孕不育、精准保胎系列讲座之 ——探索胚胎发育的奥秘
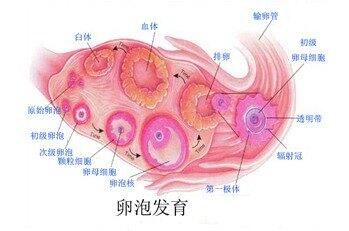
每一次流产都是有原因的,所谓不明原因流产是伪命题,只是我们没有深究其病因。为了更好预防流产发生和精准保胎治疗,追根溯源,从胚胎发育、着床过程中探寻流产及复发性流产(recurrent spontaneous abortion,RAS)病因,利于诊断和临床治疗。 一、胚胎发育 1、 卵胞的发育及成熟 (1)卵泡的发育:卵泡的发育始于始基卵泡到初级卵泡的转化,始基卵泡可以在卵巢内处于休眠状态数十年。从始基卵泡到形成窦前卵泡需9个月以上的时间,从窦前卵泡到成熟卵泡历经持续生长期(1-4级卵泡)和指数生长期(5-8级卵泡)两个阶段,共需85日,跨越了3个月经周期。一般情况下卵泡生长的最后阶段正常约需15日左右,是月经周期的卵泡期。卵泡发育过程详见图1。 (2)成熟卵泡排卵及受精:成熟卵胞和它周围的卵冠丘结构,一起从卵巢排出的过程称排卵。排卵多发生在下次月经来潮前14日左右。卵子排出后,经输卵管伞部捡拾、在输卵管壶腹部与精子相遇,完成受精,输卵管壁蠕动以及输卵管黏膜纤毛活动等协调作用,将受精卵向宫腔方向移动。 2、正常胚胎的发育与着床 (1)受精卵的形成:正常的精子与排出的卵子相遇,精子进入卵子内,卵原核与精原核融合,染色体相互混合,若正常受精,形成二倍体的受精卵。 (2)着床:受精后第3~4日,受精卵不断分裂形成桑椹胚,继续发育成为囊胚。约在受精后第4~5日早期囊胚进入宫腔并继续发育成晚期囊胚。约在受精后第6~7日,晚期囊胚侵入子宫内膜,称为胚泡着床。受精约1周后,胚泡附着于子宫内膜,约1周后,胚泡被埋入营养丰富松软的子宫蜕膜组织中,此过程称为胚胎植入(也称着床),至此,胎盘绒毛逐渐形成。 受精卵着床具备的条件有:①透明带消失;②囊胚细胞滋养细胞分化出合体滋养细胞;③囊胚和子宫内膜同步发育且功能协调;④体内分泌足量的雌激素和孕酮,雌激素和孕激素支持的子宫内膜具有容受性,允许受精卵着床。排卵、受精至胚胎植入的全过程见图。 排卵、受精至胚胎植入的全过程 3、胎盘的形成 晚期囊胚着床后,滋养层细胞分裂增殖,形成1级绒毛(初级绒毛);胚胎发育至2周末或3周初时,形成绒毛间质,称2级绒毛(次级绒毛);约在受精的第3周末,绒毛内的中胚层分化出毛细血管,形成3级绒毛,此时,胎儿胎盘循环建立,胎盘介于胎儿与母体之间,是维持胎儿宫内营养、发育的重要器官。胎盘的形成见图。 二、引起早期流产的原因 精子与卵子发育异常、胚胎染色体异常、胎盘绒毛形成异常及任何影响胚胎着床的因素均可影响胚胎发育,导致流产的发生,增加复发性流产的发病率。引起流产的常见因素有:胚胎本身的质量问题、子宫内部环境问题、全身性问题及其他因素等。 1、胚胎本身的质量问题(种子的异常) 胚胎本身的质量会影响着床的成败。种子(精子与卵子)先天性发育异常、胚胎染色体异常、受精异常均可导致流产的发生。非整倍体是胚胎反复种植失败的一个主要原因之一,大龄、卵巢功能减退、排卵障碍病史的患者,尤其是大龄不孕患者,出现胚胎染色体异常概率明显升高。 2、子宫内部环境问题(土地的异常) 种子要想种植成功,土壤也要适宜。子宫、输卵管结构及功能异常、子宫纵隔、宫腔粘连、内膜息肉、粘膜下子宫肌瘤等各种病变,会降低胚胎着床率。盆腔炎症,合并输卵管积水,炎性因子等会干扰胚胎着床。影响子宫内环境的因素,均可导致流产及RSA的发生率升高。 3、全身性因素 (1)临床没被控制的糖尿病、胰岛素抵抗、肥胖的患者,流产及复发性流产率是增加的。 (2)凝血机制异常导致胎盘局部微血栓形成,引起胎盘梗死,胚胎缺血缺氧,胚胎着床率下降,流产及复发性风险增高。如抗磷脂综合症(APS)、高同型半胱氨酸血症(HHcy)、血栓前状态等。 生命的诞生是一场缜密的程序化过程,追本溯源,探寻生命的每一步发展历程。服务于临床,造福于人类。降低临床妊娠流产的发生机率,不让流产成为复发。 高娟,副主任医师,硕士生导师,青岛大学副教授 研究生毕业于华中科技大学同济医学院妇产科生殖内分泌专业,从事妇产科及不孕不育临床工作20余年,是国内较早从事试管婴儿工作的医务人员之一。 擅长不孕不育、反复试管胚胎种植失败、复发性流产、精准保胎、多囊卵巢综合征等妇科内分泌疾病的诊断治疗。 2010始多次到武汉同济、上海第一妇婴、齐鲁医院、北京、广州多地进修学习,在不孕不育、复发性流产、精准保胎、多囊卵巢综合症等方面取得丰富临床经验,2015年创建青岛市第一个“复发性流产”专科门诊。在不孕不育、反复流产,精准保胎、多囊卵巢综合症、妇科内分泌等在诊疗技术上,采用系统的病因筛查和个性化治疗方案,在临床取得满意的疗效,受到患者高度广泛赞誉。
 高娟 主任医师 医生集团-山东 妇产科3782人已读
高娟 主任医师 医生集团-山东 妇产科3782人已读 - 早发性卵巢功能不全的临床诊断
国内外生殖会议最新资讯和精华分享之六 ——早发性卵巢功能不全的临床诊断青岛妇女儿童医院青岛大学附属妇女儿童医院 高 娟随着科技的发展,临床知识的更新,新的诊疗技术和治疗方法层出不穷,临床医师只有不断学习,更新自己的知识体系,才能更好的服务于患者。现将国内、外会议近期最新资讯和精华与大家分享,以飨读者。一、概念早发性卵巢功能不全(premature ovarianinsufficiency,POI)是指女性在40岁以前出现卵巢功能减退,主要表现为月经异常(闭经、月经稀发或频发)、促性腺激素水平升高(FSH>25U/L)、雌激素水平波动性下降。根据是否曾经出现自发月经,将POI分为原发性POI和继发性POI。1、卵巢早衰(premature ovarianfailure,POF):女性40岁以前出现闭经、促性腺激素水平升高(FSH>40U/L)和雌激素水平降低,并伴有不同程度的围绝经期症状,是POI的终末阶段。2、卵巢储备功能减退(diminishedovarian reserve,DOR):指卵巢内卵母细胞的数量减少和(或)质量下降,同时伴有抗苗勒管激素(antiMüllerianhormone,AMH)水平降低、窦卵泡数(antral folliclecount,AFC)减少、FSH水平升高。患者生育力降低,但不强调年龄、病因和月经状态。二、病因POI的常见病因包括遗传因素、医源性因素、免疫因素、环境因素等。目前,半数以上的POI患者病因不明确,称为特发性POI。1、遗传因素:遗传因素占POI病因的20%~25%,包括染色体异常和基因变异。10%~13%的POI患者存在染色体数量或结构异常,散发性POI患者的染色体异常率高于家族性患者,原发性POI患者染色体异常率显著高于继发性POI患者。(1)X染色体异常:染色体异常中X染色体异常率可高达94%,45,X及其嵌合、X染色体长臂或短臂缺失、X染色体-常染色体易位是常见的异常染色体核型。(2)常染色体异常及相关致病基因:约2%的POI患者与常染色体重排相关。已发现的致病基因包括:生殖内分泌相关基因(FSHR、CYP17、ESR1等)、卵泡发生相关基因(NOBOX、FIGLA、GDF9等)、减数分裂和DNA损伤修复相关基因(MCM8、MCM9、CSB-PGBD3等)。但中国POI患者致病基因的突变频率一般<2%,临床诊断的价值有限。2、医源性因素:常见的医源性因素包括手术、放疗和化疗。手术引起卵巢组织缺损或局部炎症、影响卵巢血液供应而导致POI。化疗药物可诱导卵母细胞凋亡或破坏颗粒细胞功能,其对卵巢功能的损害与药物种类、剂量及年龄有关。放疗对卵巢功能的损害程度取决于剂量、照射部位及年龄。年龄越大放疗的耐受性越差,越易发生POI。3、免疫及其他因素:自身免疫功能失调可能造成卵巢功能损伤,但是免疫因素究竟为原因或是结果目前尚无定论。部分POI患者伴有自身免疫性疾病,其中自身免疫性甲状腺疾病、Addison病与POI的关系最为密切。不良的环境因素、不良生活方式(包括不良嗜好)也可能影响卵巢功能。三、临床表现与诊断(一)临床表现患者可有1种或多种以下表现。1、症状:(1)月经改变:原发性POI表现为原发性闭经。继发性POI随着卵巢功能逐渐衰退,会先后出现月经周期缩短、经量减少、周期不规律、月经稀发、闭经等。从卵巢储备功能下降至功能衰竭,可有数年的过渡时期,临床异质性很高。少数妇女可出现无明显诱因的月经突然终止。(2)生育力低减或不孕:生育力显著下降;在DOR的初期,由于偶发排卵,仍然有5%~10%的妊娠机会,但自然流产和胎儿染色体畸变的风险增加。(3)雌激素水平降低的表现:原发性POI表现为女性第二性征不发育或发育差。继发性POI可有潮热出汗、生殖道干涩灼热感、性欲减退、骨质疏松、骨痛、骨折、情绪和认知功能改变、心血管症状和心律紊乱等。(4)其他伴随症状:其他伴随症状因病因而异,如心血管系统发育缺陷、智力障碍、性征发育异常、肾上腺和甲状腺功能低减、复发性流产等。2、体征:原发性POI患者可存在性器官和第二性征发育不良、体态和身高发育异常。不同病因可导致不同受累器官的病变,出现相应的伴随体征。继发性POI患者可有乳房萎缩、阴毛腋毛脱落、外阴阴道萎缩表现。3、辅助检查:(1)基础内分泌:至少2次血清基础FSH>25U/L(在月经周期的第2~4天,或闭经时检测,2次检测间隔4周);同时,血清雌二醇水平因POI早期卵泡的无序生长而升高[>183pmol/L(即50pg/ml)],继而降低。(2)经阴道超声检查:双侧卵巢体积较正常小;双侧卵巢直径2~10mm的AFC之和<5个。(3)血清AMH:血清AMH≤7.85pmol/L(即1.1ng/ml)。青春期前或青春期女性AMH水平低于同龄女性2倍标准差,提示POI的风险增加。(4)遗传、免疫相关的检查:包括染色体核型分析、甲状腺功能、肾上腺抗体等。(二)诊断1、诊断标准:(1)年龄<40岁;(2)月经稀发或停经至少4个月以上;(3)至少2次血清基础FSH>25U/L(间隔>4周)。亚临床期POI:FSH水平在15~25U/L,此属高危人群。2、病因诊断:结合病史、家族史、既往史、染色体及其他相关检查的结果进行遗传性、免疫性、医源性、特发性等病因学诊断。(三)鉴别诊断需与以下情况相鉴别:妊娠、生殖道发育异常、完全性雄激素不敏感综合征、Asherman综合征、多囊卵巢综合征(polycysticovarysyndrome,PCOS)、甲状腺疾病、空蝶鞍综合征、中枢神经系统肿瘤、功能性下丘脑性闭经、卵巢抵抗综合征(resistant ovarysyndrome,ROS)等。ROS,又称卵巢不敏感综合征(insensitive ovarysyndrome),是指原发性或继发性闭经女性(年龄<40岁),内源性促性腺激素水平升高(主要是FSH),卵巢内有卵泡存在,AMH接近同龄女性的平均水平,但对外源性促性腺激素呈低反应或无反应。——文章来源于国内生殖会议
高娟 主任医师 医生集团-山东 妇产科1809人已读 - 早发性卵巢功能不全的治疗
国内外生殖会议最新资讯和精华分享之七 ——早发性卵巢功能不全的治疗青岛大学附属妇女儿童医院 高 娟随着科技的发展,临床知识的更新,新的诊疗技术和治疗方法层出不穷,临床医师只有不断学习,更新自己的知识体系,才能更好的服务于患者。现将国内、外会议近期最新资讯和精华与大家分享,以飨读者。一、一般治疗(一)心理及生活方式干预缓解患者的心理压力,告知患者仍有偶然自发排卵的情况。健康饮食、规律运动、戒烟,避免生殖毒性物质的接触,增加社交活动和脑力活动。适当补充钙剂及维生素D,尤其是已出现骨密度(BMD)降低者。(二)遗传咨询根据家族史和遗传学检测结果评估遗传风险,对有早发性卵巢功能不全(premature ovarianinsufficiency,POI)或者早绝经家族史的女性,可借助高通量基因检测技术筛查致病基因。对家系中携带遗传变异的年轻女性建议尽早生育,或在政策和相关措施允许的情况下进行生育力保存。(三)药物治疗POI的发病机制尚不明确,目前尚无有效的方法恢复卵巢功能。1、激素补充治疗:激素补充治疗( hormone replacementtherapy,HRT)不仅可以缓解低雌激素症状,而且对心血管疾病和骨质疏松起到一级预防作用。若无禁忌证,POI患者均应给予HRT。由于诊断POI后仍有妊娠的机会,对有避孕需求者可以考虑HRT辅助其他避孕措施,或应用短效复方口服避孕药( combinedoralcontraceptives,COC);有生育要求者则应用天然雌激素和孕激素补充治疗。与COC相比,HRT对骨骼及代谢有利的证据更充分。(1)原发性POI:当POI发生在青春期前时,患者无内源性雌激素,从青春期开始至成年期间必须进行持续治疗,以利于青春期发育。因大剂量雌激素可加速骨骼成熟,影响身高,应在结合患者意愿的情况下,建议从12-13岁开始,从小剂量开始进行雌激素补充,模拟正常的青春期发育过程。必要时可联合使用生长激素,促进身高的生长。根据骨龄和身高的变化,在2~4年内逐渐增加雌激素剂量;有子宫并出现阴道流血者应开始加用孕激素以保护子宫内膜,无子宫者单用雌激素即可。当身高不再增长时,有子宫的POI患者转为标准剂量雌孕激素序贯治疗。治疗期间应监测骨龄和身高的变化,对于骨骺一直未闭合的患者,在达到理想身高后,应增加雌激素剂量,促进骨骺愈合而使身高增长停止。(2)继发性POI:治疗原则、适应证、禁忌证和慎用情况参考《绝经期管理与激素补充治疗临床应用指南(2012版)》。POI患者绝经早,长期缺乏性激素的保护,需长期用药;年轻、并发症少、风险低,是与自然绝经女性的最大区别。应遵循以下原则:①时机:在无禁忌证、评估慎用情况的基础上,尽早开始HRT。②持续性:鼓励持续治疗至平均的自然绝经年龄,之后可参考绝经后的HRT方案继续进行。③剂量:使用标准剂量,不强调小剂量,根据需求适当调整。国内常用的雌激素剂量是口服雌二醇2mg/d、结合雌激素0.625mg/d。④方案:有子宫的POI患者雌激素治疗时应添加孕激素,推荐雌孕激素序贯疗法,配伍孕激素的剂量建议为每周期口服地屈孕酮10mgd,服用12~14d;或微粒化天然黄体酮200mgd(口服或阴道置药),12~14d。无子宫或已切除子宫者可单用雌激素。如仅为改善泌尿生殖道萎缩症状时,可经阴道局部补充雌激素。⑤药物:POI患者需要HRT的时间较长,建议选用天然或接近天然的雌激素(17-β雌二醇、戊酸雌二醇、结合雌激素等)及孕激素(微粒化黄体酮胶丸或胶囊、地屈孕酮),以减少对乳腺、代谢及心血管等方面的不利影响。现有的数据显示,地屈孕酮相对于其他合成孕激素,不增加乳腺癌的发生风险。⑥随访:治疗期间需每年定期随访,以了解患者用药的依从性、满意度、不良反应,必要时调整用药方案、药物种类、剂量、剂型。2、非激素治疗:对于存在HRT禁忌证、暂时不愿意或者暂时不宜接受HRT的POI患者,可选择其他非激素制剂来缓解低雌激素症状。(1)植物雌激素:指植物中存在的非甾体雌激素类物质,主要为杂环多酚类,其雌激素作用较弱,长期持续服用可能降低心血管疾病风险、改善血脂水平、改进认知能力。(2)中医药:包括中成药、针灸、耳穴贴压、按摩、理疗等,其辅助治疗作用仍有待临床证据证实。目前,POI非激素治疗的临床证据非常有限,尚不能作为HRT的替代方案,仅作为辅助治疗或暂时性的替代治疗。3、新治疗方法:卵泡体外激活,有临床妊娠的报道,但激活效率低,临床难以普及。免疫、干细胞、基因编辑等前沿治疗方法尚处于研究阶段。(四)远期健康及并发症管理1、对骨骼健康的影响:为维持骨骼健康及预防骨质疏松,推荐行雌激素补充治疗,并应保持健康的生活方式,包括负重运动、避免吸烟以及维持正常体质量。一旦被诊断为POI,建议测定BMD。如被诊断为骨质疏松,应积极HRT治疗,以防骨质进一步丢失,必要时加用其他骨质疏松治疗药物。如果BMD持续下降,提示可能存在其他的潜在病因。2、对心血管系统的影响:POI患者发生心血管疾病的风险增加,应通过健康的生活方式减少危险因素带来的不良影响。推荐尽早HRT治疗,并且持续使用至平均的自然绝经年龄。3、其他:HRT治疗和健康的生活方式可预防和减少可能的认知功能障碍。对于存在阴道干涩不适等泌尿生殖系统症状及性交困难者,可局部使用雌激素或阴道润滑剂。二、生育相关的管理。(一)辅助生殖技术治疗目前尚无最佳的用药方案。增加促性腺激素剂量、促性腺激素释放激素拮抗剂方案、促性腺激素释放激素激动剂短方案、微刺激及自然周期方案虽一定程度上可改善辅助生殖技术(ART)治疗的结局,但均不能证实确切有效。多种预处理方案及辅助抗氧化制剂的疗效仍有待进一步证实。亚临床期POI患者接受ART治疗时,卵巢低反应的发生率、周期取消率增高,妊娠率降低。赠卵体外受精-胚胎移植(IVF-ET)是POI患者解决生育问题的可选途径。贈卵IVF-ET的妊娠率可达40%~50%。治疗前应根据病因进行系统评估,有化疗、纵隔放疗史或 Turner综合征患者,需行心血管系统和超声心动图检查;自身免疫性POI应检测甲状腺功能、肾上腺抗体;有肿瘤史的患者应接受肿瘤专科评估,排除复发的可能。(二)生育力保存主要针对POI高风险人群或因某些疾病或治疗损伤卵巢功能的女性。根据患者意愿、年齡和婚姻情况,建议合适的生育力保存方法。1、适应证:(1)肿瘤患者:需肿瘤学、生殖医学胚胎学、遗传学等多学科专家合作,充分评估肿瘤治疗和生育力保存的价值,制定和实施个体化方案,患者需充分知情相关风险及结局。(2) Turner综合征:部分 Turner综合征患者卵巢虽然可见少量卵泡,但妊娠后胎儿合并心血管畸形比例高,不适宜生育;同时卵母细胞质量差、染色体异常等情况需充分告知、评估。(3)其他:卵巢子宫内膜异位囊肿手术、药物治疗等引起的POI2、生育力保存的方法:(1)胚胎冷冻:是已婚女性生育力保存的主要方法,在有效性和安全性上具有显著的优势。但对于患有雌激素敏感肿瘤的患者需警惕控制性超促排卵(COH)造成的高雌激素暴露风险,可选择芳香酶抑制剂(如来曲唑)、自然周期等获卵方案。(2)成熟卵母细胞冷冻:为未婚女性提供了生育力保存的机会,但尚存在法律、管理、技术、伦理、安全性等问题。(3)未成熟卵母细胞体外成熟技术:适用于不能进行COH的肿瘤患者或需要即刻行肿瘤治疗的患者。但此技术在安全性、有效性上仍有待证实,建议培养成熟后冷冻。(4)卵巢组织冷冻:主要用于接受放化疗的患者,但卵巢组织冷冻仍存在管理、技术、伦理、安全性等问题。(5)促性腺激素释放激素激动剂:可用于肿瘤患者化疗时的卵巢功能保护,机制可能与降低卵巢对化疗药物的通透性或降调凋亡分子相关,其有效性仍待进一步证实。——文章来源于国外生殖会议(完)2019年10月
高娟 主任医师 医生集团-山东 妇产科1938人已读
在线服务患者 2,287位
科普文章 17篇



