科室介绍 查看全部
科室医生 查看全部
-
妇科

王良
主任医师
4.3
妇科
田其芳
主任医师
4.0
妇科
傅云峰
主任医师
3.8
妇科
赵小峰
主任医师
3.9
妇科肿瘤
朱长焜
副主任医师
3.5
妇科
郭庆云
副主任医师
3.8
妇科
周云晓
主任医师
3.8
妇科
叶寄星
主任医师
3.5
妇科
陈绣瑛
主治医师
3.4
妇科
梁翠霞
主任医师
3.3
-
妇科

王彩凤
主治医师
3.3
妇科
王颖
副主任医师
3.2
妇科
徐婉婉
医师
3.2
妇科
张郁
主治医师
3.2
妇科
金祖坚
主治医师
3.1
妇科
吴凌凌
主治医师
3.1
妇科
喻员员
主治医师
3.1
妇科
崔平
主治医师
3.1
妇科
周柱
主治医师
3.1
妇科
徐君碧
主治医师
3.1
-
妇科

张权
主治医师
3.1
妇科
马雪松
医师
3.1
妇科
胡瑛瑛
医师
3.1
妇科
彭斌
医师
3.1
生殖
孙涛
医师
2.9
科普·直播义诊专区 查看全部
- 精选 最喜欢中国人的HPV型号是什么?你中招了吗?
老大HPV52型,老二HPV16型,老三HPV58型。你中招了吗?不用奇怪。HPV病毒很常见,多达200种,其中40多种感染生殖道。有性伴侣的女性大约84.6%曾经感染HPV病毒。WHO数据显示男性约1/3曾感染HPV病毒。除了性生活传播,还可以通过母婴传播和皮肤粘膜接触传播,千万不要因为有HPV感染影响夫妻感情哦!
 金祖坚 主治医师 浙江大学医学院附属第四医院 妇科814人已读
金祖坚 主治医师 浙江大学医学院附属第四医院 妇科814人已读 - 精选 宫颈锥切术后会影响下次怀孕吗?
可能会.宫颈锥切术后由于缩短了宫颈长度,同时宫颈壁变薄,约20%术后妊娠患者存在不良妊娠结局,宫颈壁变薄,约20%术后妊娠患者存在不良结局,晚期流产的比例是非锥切者的7倍,而锥切类型、锥切大小、宫颈长度是宫颈锥切术后早产的三个高危因素。宫颈锥切的锥高越高,早产风险将越大。不过也有好消息:宫颈结构保持完好,无感染情况下,90%宫颈可恢复正常长度.术后6月复查正常即可积极备孕.
 金祖坚 主治医师 浙江大学医学院附属第四医院 妇科90人已读
金祖坚 主治医师 浙江大学医学院附属第四医院 妇科90人已读 - 精选 绝经后的你遭遇宫颈高级别病变怎么办?
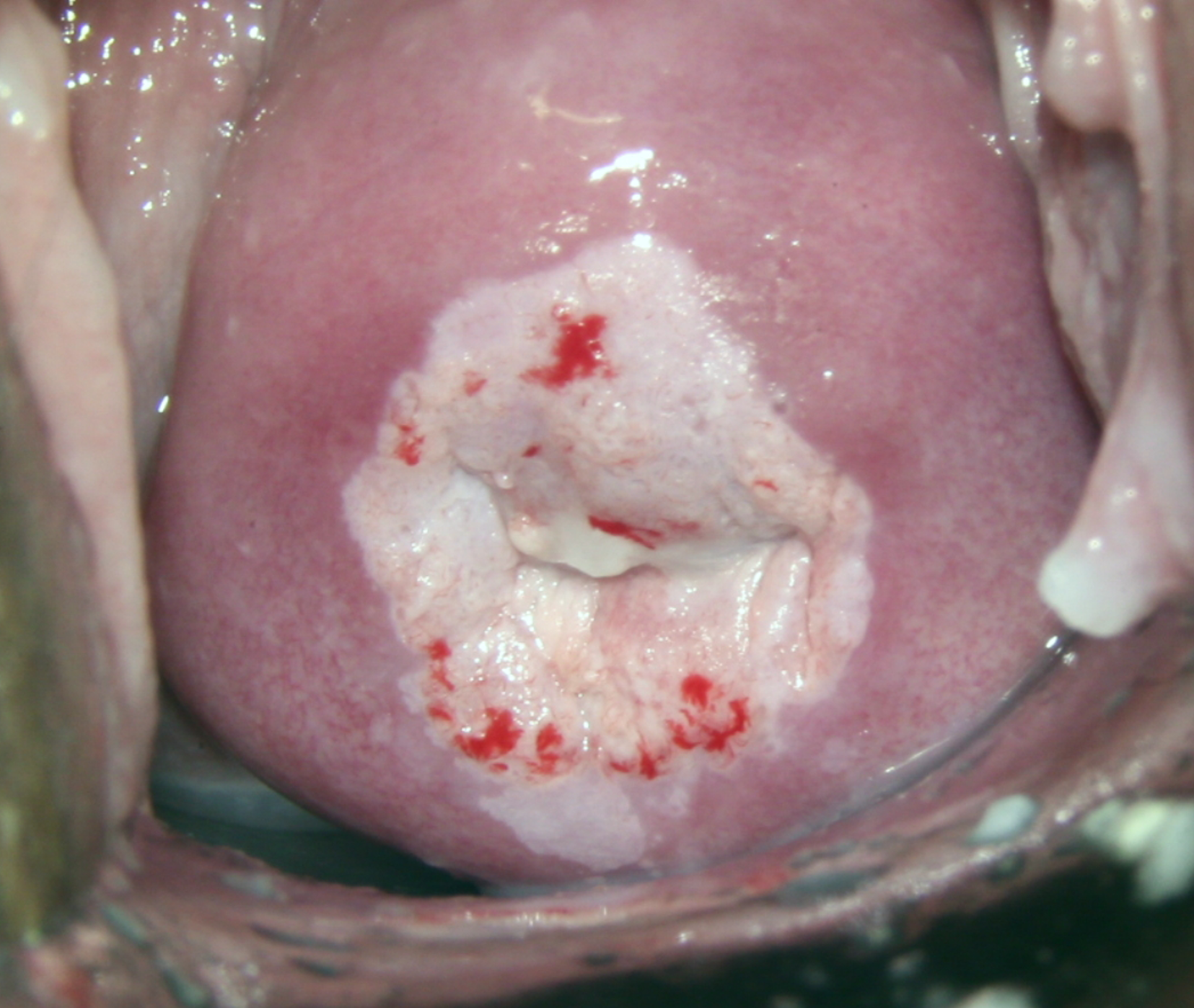
不用害怕,及时就医.规范化治疗,个性化决策,科学随访管理.治疗上简单的说:1.低级别可以短期观察,2.长期低级别需要干预,3.高级别必须要手术干预(LEEP/CKC锥切手术集诊断和治疗于一体),实在无法宫颈锥切者直接选择子宫切除.4.连续需要随访25年哦,鉴于年龄≥50岁者,连续需要随访25年,较困难,后续病变风险高,选择子宫切除也是可以接受的。5.特殊补充,推荐AIS患者进行宫颈锥切术。首选一次性完整切除,锥切深度20~25mm,锥切目标为阴性边缘,切缘阴性者首选全子宫切除术。若锥切切缘阳性,推荐二次锥切或多次锥切,无法二次锥切或切缘持续阳性者,推荐改良根治性子宫切除术或筋膜外全子宫切除术以及前哨淋巴结活检术。知识点来了:绝经后宫颈上皮内病变的特点:据WHO统计,每年新发宫颈癌约57万例,死亡31万例;中国每年新发13万例,占全球总发病例数的28%。宫颈癌的高发年龄为50岁以上,中国宫颈癌的两个高发年龄段分别为35~39岁和60~64岁,故绝经后是女性宫颈癌的第二个罹患高峰。国内研究显示,宫颈活检为HSIL(CINII/III)的患者中,绝经后女性占4.3%~6.5%。绝经后HPV感染现状:高危型HPV(high-riskhumanpapillomavirus,HR-HPV)感染是宫颈癌的主要致病原因,99%的宫颈癌与HPV感染有关,各年龄段女性对HPV普遍易感。中老年女性由于雌激素水平降低,机体免疫功能下降,HPV自然清除率降低,HR-HPV持续感染机会增加。中国常规体检人群中HR-HPV检出率为13.55%,绝经后HPV阳性率为17.20%,以HPV16型最为常见。针对:组织病理学LSILLSIL患者多为HR-HPV一过性感染,约60%的患者病变自然消退。一项多中心回顾性研究纳入434例LSIL患者,在长达5年的随访中,LSIL(CINI)进展为HSIL(CINII~III)的比例为7.4%。另外一项研究报道,LSIL患者经过24个月的随访,88.5%的患者病变消退,10.8%的患者病变持续存在,仅0.7%的患者进展为HSIL。原则上绝经后LSIL随访观察即可,无需治疗。鉴于绝经后宫颈多为III型转化区,宫颈管内存在潜在病变可能,尽管阴道镜下活检及ECC检查诊断为LSIL,但仍有一定的漏诊可能,需严格结合病理诊断前的细胞学检查结果,做到分层管理,最大程度地降低隐匿性HSIL。细胞学结果为ASC-H/HSIL/AGC或更高级别的LSIL研究数据显示,细胞学HSIL、HPV阳性患者CINIII+的即时风险为49%,细胞学HSIL、HPV阴性患者CINIII+的即时风险为25%,细胞学ASC-H、HPV阳性患者CINIII+的即时风险为26%,细胞学AGC、HPV阳性患者CINIII+的即时风险为26%。因此,细胞学为高级别检测结果而阴道镜下活检为LSIL的患者,隐匿性HSIL风险较高,诊断性切除是可接受的;2年以上持续性组织病理学LSIL可选择手术治疗或继续随访。若选择治疗,需阴道镜检查充分、鳞柱交界和病变上缘完全可见,可选择切除性治疗或消融治疗,消融治疗前需行ECC,并且组织病理学结果阴性。针对:组织病理学HSIL未经治疗的HSIL具有较高的癌变潜能,需要对组织病理学确诊的HSIL进行规范化治疗。宫颈冷刀锥切术(cold-knifeconization,CKC)和宫颈环形电切术(loopelectrosurgicalexcisionprocedure,LEEP)仍是绝经后HSIL的推荐处理方式,具有诊断和治疗双重价值;绝经后CKC或LEEP的手术难度增加,锥切术后切缘阳性率升高。(1)宫颈锥切术对于绝经后宫颈HSIL,宫颈锥切术可提供有无间质浸润的病理信息,同时实现诊断与治疗的双重效果。宫颈切除术的类型及手术范围取决于转化区的类型、病灶范围、宫颈长度等。建议I型转化区行I型切除,切除长度为7~10mm;II型转化区行II型切除,切除长度为10~15mm;III型转化区行III型切除,切除长度为15~25mm。LEEP具有疼痛感低、无需麻醉、门诊可操作、术中出血量少、无需缝扎、电凝止血即可、对宫颈形态及机能损伤较小、术后并发症少等优势,缺点是组织切缘受电环热损伤的影响,可能影响病理组织学分析;CKC获取的标本切缘清晰,不影响组织病理学分析,缺点是需要住院、手术时间长、出血量多、宫颈组织切除多,增加了术后阴道镜检查与残留及再复发的评估难度。文献报道,LEEP术后切缘总体阳性率高于CKC,但病灶残留少于CKC,病变复发率低于CKC。二者手术适应证相同,但当高度怀疑微小浸润和AIS时,优先选择CKC。绝经后多为III型转化区,LEEP术易损伤膀胱或直肠,导致宫颈管粘连及病变残留等发生风险升高。(2)子宫切除术不推荐作为绝经后HSIL的初始治疗方法。部分绝经后患者宫颈萎缩明显、穹隆消失、手术视野暴露困难、手术空间狭小、解剖结构不清,对于宫颈锥切困难者,可考虑小范围LEEP取材,以免漏诊宫颈癌。直接全子宫切除术存在术后病理升级为浸润癌、再次补充治疗的风险。有研究报道750例绝经后宫颈病变行宫颈锥切术患者,术后216例患者病理升级,绝经与锥切术后病理升级明显相关,绝经时间>5年的患者中,40.3%的患者术后病理升级。对于宫颈严重萎缩确实无法锥切的绝经后患者,在综合考虑HPV分型、宫颈及阴道萎缩情况、活检的宫颈病变是否累及腺体、切缘存在阳性的可能等因素后,谨慎选择直接全子宫切除。要求术前必须完善相关影像学检查(MRI、B超等),术中送检快速冰冻病理切片,最大程度地排除浸润癌.AIS病变常见于宫颈管,阴道镜难以观察到,且阴道镜图像无典型特征;病变呈多中心或跳跃性;HPV检测与细胞学检查的灵敏度较低,推荐组织病理学确诊的AIS患者行宫颈诊断性切除术,以排除浸润性腺癌;细胞学为AIS、AGC倾向瘤变或无特殊说明的持续性AGC,即使宫颈活检和ECC结果为阴性,仍推荐诊断性切除手术。AIS锥切术的基本要求是切缘阴性,若首次宫颈锥切切缘阳性,推荐二次锥切或多次锥切,除非已无法再次锥切。AIS锥切需保持组织的完整,以评估切缘状态,建议一刀完整切除,避免“牛仔帽”式切除或多次分割切除,切除深度应达20~25mm,残留宫颈管行ECC,手术方式首选CKC。由于宫颈AIS病变呈多中心或跳跃性,即使切缘阴性,也不能完全排除病变残留的可能,锥切术后首选全子宫切除术;若锥切切缘阳性,推荐二次锥切或多次锥切,对于无法再次切除或锥切持续阳性者,推荐改良根治性子宫切除术或筋膜外全子宫切除术以及前哨淋巴结活检术.科学随访管理:1.LSIL的随访管理LSIL初诊后未进行临床干预者应定期随访,推荐间隔6~12个月,首选HPV和TCT联合筛查或HPV单独筛查;连续2次检查均阴性,转为常规随访,HPV或TCT任何一项检查异常,建议转诊阴道镜检查,并按照相应组织学结果进行管理。2.锥切术后的随访管理(1)锥切术后切缘阴性管理:推荐治疗后6个月行HPV和TCT联合筛查,检测阴性者每年1次联合检查或单独HPV检测,直到连续3次检查均阴性,后续每3年进行一次监测,至少持续25年。宫颈上皮内病变治疗后罹患宫颈癌和其他HPV相关肿瘤的风险高于普通人群,宫颈癌的高风险在治疗后至少持续25年,50岁以上风险更高。一项对14832例宫颈锥切术患者的回顾性研究发现,年龄≥50岁的患者术后宫颈病变复发及宫颈浸润性癌的发生率明显升高。因此,年龄≥50岁者,选择子宫切除也是可以接受的。(2)锥切术后切缘阳性管理:锥切手术标本的切缘情况不作为判定术后病变残留的必要条件,但切缘阳性与病变残留相关。Dou等对119例HSIL切缘阳性患者进行回顾性分析,发现4例患者残留宫颈浸润癌,其中3例患者为绝经后。外切缘阳性者随访策略同切缘阴性者;内切缘阳性优先选择再次宫颈切除手术;有HSIL残留证据,不愿或无法再次宫颈切除或随访依从性差者,可以接受全子宫切除术。(3)子宫切除术后随访管理以HSIL、AIS为指征行子宫切除术者,术后发生阴道上皮内瘤变(vaginalintraepithelialneoplasia,VAIN)的风险明显增加,建议术后每年进行1次筛查,连续3次阴性后进行长期随访及检查,每3年1次HPV检测或TCT检查联合HPV检测,即使年龄超过65岁,也至少随访25年。
 金祖坚 主治医师 浙江大学医学院附属第四医院 妇科258人已读
金祖坚 主治医师 浙江大学医学院附属第四医院 妇科258人已读
问诊记录 查看全部
- 未避孕未孕近3年 平常月经周期30天,经期7天,轻微痛经,末次月经7.12。同... 其他都检查过。就差宫腔镜没有检查 想看一下。因为月经也不是很通畅 所以 想检查看下有没有什么问题总交流次数89已给处置建议
- 查体发现HPV 18阳性以及宫颈病变六天 组化已完成,月经干净 手术后病理报告 术后病理报告,以及什么时候去复查,注意事项,要不要继续用药 术后病理报告分析,严不严重,要不要继续用药总交流次数28已给处置建议
- Leep刀后外阴瘙痒 昨天中午张郁医生leep到手术,回家后就感觉外阴有点痒。今早... 为什么会痒?能用点什么药吗?总交流次数11已给处置建议
- 查体发现HPV 18阳性以及宫颈病变六天 组化已完成,月经干净 今天月经已经干净,下周日预约手术可以吗? 月经已经干净了,下周日手术可以吗?总交流次数41已给处置建议
- 查体发现HPV 18阳性以及宫颈病变六天 患者于2023年3月1日查体发现,HPV 18阳性随后行宫颈... 我想直接手术,可以帮我安排手术吗?
对于我hpv的活检结果给予我一定手术治疗方案总交流次数20已给处置建议
总访问量 1,328,336次
在线服务患者 704位
科普文章 48篇



