科室医生 查看全部
科普·直播义诊专区 查看全部
- 精选 了解肿瘤的发生与进展
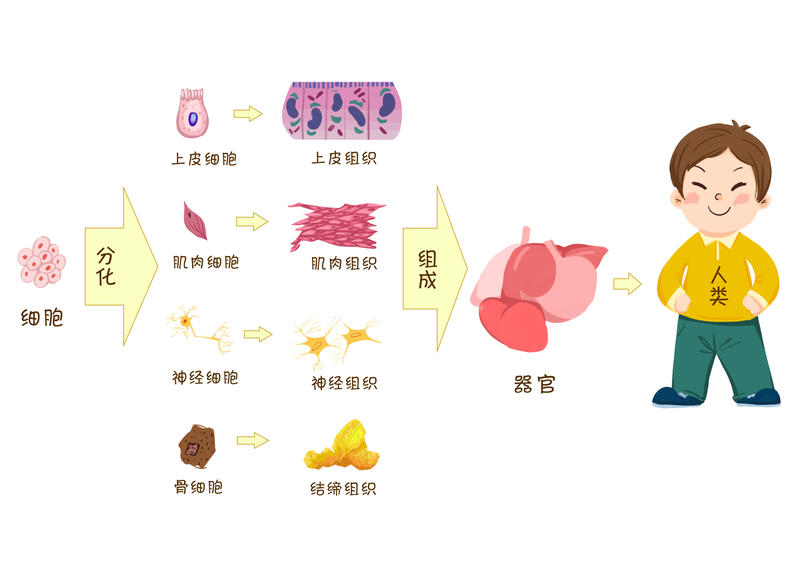
人体是由很多细胞组成,最开始是由一个受精卵不停反复分裂,从而分裂成各种各种各样的组织器官(消化系统,神经系统,泌尿系统等),而这些细胞的分裂、分化及增殖都与基因密切相关,这些基因中蕴藏的生物信息,是我们维持生命不可缺少的一部分。正常的细胞会随着自身的生长发育而增长或消亡;比如胎儿时期手指间会长出蹼一样的组织,但随着机体的增长会逐渐脱落;同样,皮肤和肠管的上皮细胞也会随着新陈代谢而死亡,逐渐被新的细胞所代替,这一系列的组织自我更新都是由基因所控制的。如果在细胞的增生、成熟分化、死亡等过程中,基因的调节功能发生异常,发生突变的或者异常的细胞将持续增长,逃避死亡而形成肿瘤。在我们的身体中,存在着一组监视和修复基因突变的功能,抑制异常细胞的增生,清除发生变异的细胞,从而维持机体的正常状态。但是,异常的细胞也可以逃避免疫系统的监视,形成对身体有害的、获得无限增长,并且具有远处转移能力的肿瘤细胞,这一过程可能需要数年。这样看来,许多肿瘤的发生机制,同样是生命诞生和延续的重要功能。正因为如此,需要常常放在心上。可以这么说,人很难避免一生不得肿瘤,但是可以通过适当的运动、多吃蔬菜水果、禁烟禁酒等可以降低获得肿瘤的几率。另一方面,我们知道肿瘤发生发展的机制后,今后可以更好的利用这些机制,提高肿瘤治疗的效果。手术治疗:通过外科手段,将肿瘤完整切除,不仅可以达到根治目的,而且可以获得肿瘤的病理分型和分期,在另一方面,完整切除肿瘤可最大的保存器官原有的功能,切除的范围不宜过大。现今,保留器官功能的手术有两种,一是传统的功能性手术,另一个就是国内外新兴的NOSES(经自然腔道取标本)手术。传统的功能性手术切除病变肠管及清扫周围淋巴结,吻合断端肠管或者腹部造瘘,尽可能的保留了肠道原有的功能;但因术后需要取出切除组织,需在腹壁开口,切口较大,对患者创伤较大,术后恢复时间长,相应的导致住院花费增加。NOSES手术,是在传统腹腔镜根治结直肠癌的基础上,通过肛门、阴道等自然腔道取出标本,不仅尽可能保留了肠道原有的功能,而且避免腹壁辅助切口,减轻患者术后疼痛,保留腹壁功能;并且腹部因为没有切口,具有良好的美容效果,对患者的术后心理状态的恢复起着很大的作用。药物疗法①化学疗法(化疗)通过使用化学治疗药物杀灭癌细胞达到治疗目的。化疗是目前治疗癌症最有效的手段之一,和手术、放疗一起并称癌症的三大治疗手段。手术和放疗属于局部治疗,只对治疗部位的肿瘤有效,对于潜在的转移病灶(癌细胞实际已经发生转移,但因为目前技术手段的限制在临床上还不能发现和检测到)和已经发生临床转移的癌症就难以发挥有效治疗了。而化疗是一种全身治疗的手段,无论采用什么途径给药(口服、静脉和体腔给药等),化疗药物都会随着血液循环遍布全身的绝大部分器官和组织。因此,对一些有全身播散倾向的肿瘤及已经转移的中晚期肿瘤,化疗都是主要的治疗手段。②内分泌治疗某些肿瘤的发生、发展、生长、增殖与内分泌激素有关,如:乳腺癌、前列腺癌、子宫内膜癌、卵巢癌、大肠癌等,用某些药物阻断激素受体或抑制激素分泌可产生治疗肿瘤的作用[8]。③分子靶向治疗分子靶向治疗,是在细胞分子水平上,针对已经明确的致癌位点(该位点可以是肿瘤细胞内部的一个蛋白分子,也可以是一个基因片段),来设计相应的治疗药物,药物进入体内会特异地选择致癌位点来相结合发生作用,使肿瘤细胞特异性死亡,而不会波及肿瘤周围的正常组织细胞,达到精确治疗肿瘤的目的。④免疫治疗免疫治疗是指针对机体低下或亢进的免疫状态,人为地增强或抑制机体的免疫功能以达到治疗疾病目的的治疗方法。免疫治疗的方法有很多,适用于多种疾病的治疗。肿瘤的免疫治疗旨在激活人体免疫系统,依靠自身免疫功能杀灭癌细胞和肿瘤组织[9]。与以往的手术、化疗、放疗和靶向治疗不同的是,免疫治疗针对的靶标不是肿瘤细胞和组织,而是人体自身的免疫系统。放射线治疗肿瘤放射治疗是利用放射线治疗肿瘤的一种局部治疗方法。放射线包括放射性同位素产生的α、β、γ射线,以及各类x射线治疗机或加速器产生的x射线、电子线、质子束及其他粒子束等。大约70%的癌症患者在治疗癌症的过程中需要用放射治疗,约有40%的癌症可以用放疗根治[10]。直肠癌放射线治疗使用较多。
 郁雷 副主任医师 哈医大二院 结直肠肿瘤外科280人已读
郁雷 副主任医师 哈医大二院 结直肠肿瘤外科280人已读 - 精选 健康小贴士016---大夫,术后怎么便血了?
结直肠癌手术后便血是临床中常见的问题,常常引起患者及家属的恐慌。今天我们就来回答一下,术后怎么便血了?术后便血常见原因: 1、卧床期间,大便干燥,排便用力;2、原有的痔疮、肛裂等肛肠疾病引起;3、术中肠腔残存的血(黑便症状);4、吻合口渗血;5、吻合口出血;6、术后半年,出现便中带血症状,需排除肿瘤复发;如何处理:术后住院期间,一旦出现便血,一定不要过于恐慌,先留好粪便标本,仔细观察大便性状(黑色还是血红色)、便血的量及便血次数,而后找医生并详细提供病史。如果是术后出现黑便等,一般是肠腔内残存的血所致,不需特殊处理,密切观察,待其自然排尽即可。少量的渗血也不需惊慌,可能是术后吻合口少量渗血,医生应用止血药物及卧床休息可以恢复。但如果出血速度快,或者出血量大,需要警惕吻合口出血,需要立即报告医生,而后进行肠镜下检查和治疗。如果术后回家半年后,出现便血等,应先进性采血、CT或肠镜等方式复查,排除疾病复发后再考虑其他原因,并到正规医院就诊。总结来说就是,术后便血,重视但不慌张!
王贵玉 主任医师 哈医大二院 结直肠肿瘤外科1093人已读 - 精选 我国溃疡性结肠炎诊治的变迁
王猛 王锡山哈尔滨医科大学附属第二医院 普外九病房【摘要】溃疡性结肠炎(ulcerative colitis, UC)是一种慢性、难治性肠道炎症性疾病,近年来在我国其发病率呈上升趋势。到目前为,我国已制订5版关于UC诊断及治疗规范,这些版本在治疗理念上不断发展变化,体现了对该病的理解不断深入。梳理我国5版UC诊断及治疗共识的变迁,有助提高临床医生对UC的认识水平。【关键词】结肠炎;溃疡性;诊断;治疗溃疡性结肠炎(ulcerative colitis, UC)是病因不十分清楚的一种慢性非特异性肠道炎症性疾病,主要侵犯直肠、结肠,是炎症性肠病(inflammatory bowel disease,IBD)的一种。到目前为,我国已制订5版关于UC诊断及治疗规范,前四版分别在1978年、1993年、2000年、2007年提出,最近是在2012年“炎性肠病诊断与治疗的共识意见”对UC诊断和治疗进行阐述。这些版本在治疗理念上不断发展变化,体现了对该病的理解不断深入。解读我国制定的5版UC诊断及治疗规范,有助提高临床医生对UC的认识水平。1 诊断标准在2007年共识中首次对诊断时限提出要求,对UC的诊断,病程必须达到4~6周以上,医生可以充分利用这段时间观察病情变化,排除感染性肠炎,大多数感染性肠病病程少于6周,可进行鉴别[1]。在UC诊断中,纤维结肠镜检查发挥越来越重要的作用。不仅可以对病灶进行观察,还可以进行活组织检查。2000 年版本首次加入了结肠镜下病变的特点,即“病变多从直肠开始,呈连续性、弥漫性分布”。2012年版本中加入了内镜下黏膜染色技术,放大内镜技术,有助于UC诊断。遇肠腔狭窄无法继续进镜时,可选择钡剂灌肠造影、CT 或MRI检查等。不宜对重症UC患者强行肠镜检查,因为这些患者肠壁菲薄,容易穿孔。2012年共识中弱化钡剂灌肠检查作用,钡剂灌肠应用率逐渐下降。相比于肠镜,它只能间接反映粘膜情况,但其在观察肠管走行和肠壁运动的顺应性等等方面有一定优势。除结肠镜检查外,B 超、CT 和MRI等检查亦有助于UC诊断及鉴别 B超可以随时评价疗效,方便经济。CT 和MRI可观察病变、肠系膜血管、淋巴结等,有助于鉴别诊断。相信将来可能会出现更先进的方法用于UC的诊断。病理检查是确诊UC 的必须检查。在先前的共识中,病理诊断只有对炎症的简单描述。到2000年,病理活检的地位在共识中凸显出来,分为对活动期和缓解期表现进行阐述,首次较详细完整地描述了UC 的黏膜病理特点,其中“隐窝炎,隐窝脓肿和隐窝结构改变”是较为特异的表现。2012年版本中强调注意是否存在隐窝上皮异型增生(上皮内瘤变) 或癌变,因为溃疡性结肠炎有癌变可能。亚太地区UC 癌变风险为0.3%~1.8%[2]。瑞典一项研究显示,UC 确诊后10 年、20 年、25 年结直肠异型增生/肠癌累积风险分别为2%5%和10%[3]鉴别诊断一直以来都是UC的难点,2007 年共识中,首次提出系统诊断流程,包括“疑诊、拟诊、确诊”。 2012年进一步强调随访的重要性。排除其他疾病的基础上,比如与感染性肠炎、肠结核、阿米巴病及抗菌药物相关性肠炎、放射性肠炎等,具有典型临床表现者为疑诊,并进一步检查,具备结肠镜和(或) 放射影像学特征者,可拟诊。再加上黏膜活检和(或)手术标本组织的病理学特征者,即可确诊UC。对于初发病例、临床表现和结肠镜及活检组织学改变均不典型者,暂不确诊,应予随访,密切观察。上述UC 诊断流程的提出,使我国UC 诊断更加科学严谨,避免了误诊的发生。2 疾病评估患者病情评估是UC诊断的重要组成部分,包括临床类型、病变范围、疾病活动性、严重程度、肠外表现及并发症等,这与治疗方案制定和疗效评估等密切相关。准确的病情分度和分期是患者获得适宜治疗的关键。新版共识中临床分型变化较大,取消了慢性持续型和暴发型,只简单分为初发型和慢性复发型[1]。UC仅约5% 表现为不间断的持续发作,约5%表现为单次急性发作后长期缓解。初发型指无既往病史而首次发作,该类型在鉴别诊断中应予特别注意,亦涉及缓解后如何进行维持治疗的考虑,慢性复发型指临床缓解期再次出现症状,临床上最常见。暴发型结肠炎,因不同国家地区概念不统一而易造成认识的混乱,2012版共识将其取消,归入重度UC中。在最新2012 年版本中UC 病变范围的分类推荐蒙特利尔分型,与欧洲克罗恩病和结肠炎组织(ECCO)2008 共识[1]、亚太胃肠病学会( APAGE) 2010 共识一致,分为E1(分布直肠),E2(左半结肠),E3(广泛结肠),这样分类是基于我国UC 患者的病变范围特点与西方相似[4],便于数据收集与统计。为更加科学地对UC严重程度进行评估,我国自1993 年版本开始引入Truelove and Witts 分度,并沿用至今。该标准具体内容包括排便次数、便血、体温、脉搏、血红蛋白及血沉等指标,实用且易于掌握。ECCO[1]/美国胃肠病学院( ACG)[5]/英国胃肠病学会( BSG)[6]均推荐根据改良Truelove 和Witts 疾病严重程度分型定义重度结肠炎。为了对UC 病情分期更加准确量化。2007 年版本引入了Sourtherland 疾病活动指数( DAI) ,也称Mayo指数,对排便次数、便血、内镜发现和医师评估4个项目进行评估计分,根据总分判定缓解期,轻度、中度或重度活动期。在2012版共识中,特别提到了UC 合并艰难梭菌或巨细胞病毒( CMV) 感染,提醒临床医师注意,重度UC 或在免疫抑制剂维持治疗病情处于缓解期患者出现难以解释的症状恶化时,应考虑到合并艰难梭菌或CMV 感染的可能。自2000 年共识开始,增加了UC 肠外表现及并发症的相关内容,可有关节、皮肤、眼部、肝、胆等系统受累;并发症可有大出血、穿孔、中毒性巨结肠、癌变等。这表明了随着研究的进展,认识到UC是一种全身免疫性疾病,病变不仅局限于结直肠,肠外表现和并发症均应积极治疗,也是随访观察的重要指标[9]。新版UC共识中诊断步骤更加完善和科学,强调相关危险因素病史采集,增加了阑尾切除术,家族史等危险因素。阑尾切除术为UC 的保护因素[8],在20 岁之前行阑尾切除术仍有相当显著的保护作用。家族史也是UC 的独立危险因素。3 疗效标准 1993年版本提出UC 的最佳治疗效果分别为“痊愈”和“近期治愈”,随着对UC 认识不断深入,从2000 年版本开始引入“完全缓解”的理念,取消了“治愈的概念”。2012年共识新增复发的概念。UC具有免疫疾病的特点,目前所采用的非手术治疗方法,只能达到诱导和维持缓解的目的,仍然有复发的可能,只有切除全部结直肠才能真正治愈UC。临床症状的缓解学者们已达成共识,但对内镜下黏膜愈合标准的研究仍有异议。目前国内外学者公认的最佳治疗目标是黏膜组织愈合,延长缓解期,减少复发,降低癌变风险。4 治疗建议自2000年版本中开始加入治疗建议,2007 、2012年版本中得以完善和发展,对药物选择时机进行阐述,解决了临床医师的疑惑,轻度活动期可选用5-氨基水杨酸制剂;中度活动期水杨酸类药物疗效不佳者,适当加量或改用糖皮质激素。对激素无效或依赖者,可使用硫嘌呤类药物。临床上,UC 治疗时常会将氨基水杨酸制剂与硫嘌呤类药物合用,但氨基水杨酸制剂会增加硫嘌呤类药物骨髓抑制的毒性[10]。对病变局限者,重视局部用药,可用栓剂、灌肠剂,口服与局部用药联合应用疗效更佳。新版共识中,增了生物制剂应用,英夫利西单抗( IFX) ,当激素和免疫抑制剂治疗无效、激素依赖或不能耐受上述药物治疗时,可考虑IFX 治疗。国外研究已肯定其疗效[11]。对重度UC治疗提出治疗流程建议,注意一般治疗,纠正水电解质及酸碱平衡紊乱,排除合并艰难梭菌或CMV感染,其次首选激素治疗,对激素治疗无效的患者转换治疗,“拯救”治疗,或直接手术治疗。在2000年版本中首次提出手术绝对指征和相对指征。新版共识中对手术病变的处理进行更详细的说明: “癌变、平坦黏膜上的高度异型增生应行全结肠切除; 平坦黏膜上的低度异型增生可行全结肠切除,或3-6个月后随访,如仍为同样改变亦应行全结肠切除; 隆起型肿块上发现异型增生而不伴有周围平坦黏膜上的异型增生,可予内镜下肿块摘除,之后密切随访,如无法行内镜下摘除则行全结肠切除。”国外数据显示,虽然有很多治疗UC有效的药物,但是约有15%-30% 的UC 患者最终需要外科治疗,而这一比例在我国不到5%。早在2005年美国的结直肠外科医师协会已经制定了一个基于循证医学的详细UC外科治疗指南[12],2014年对该指南进行更新[13]。但我国UC的外科治疗与发达国家相比仍存在较大差距,表现在手术指征、方式等多个方面,欧美等发达国家直接将UC手术指征分为急症和择期两类,摒弃了绝对指征和相对指征的含混概念,前者包括癌变、大出血、肠穿孔和中毒性巨结肠,后者包括内科治疗不满意的顽固性UC、无法耐受药物治疗副作用、肠黏膜异型增生或恶变、生长发育迟滞和严重肠外表现者等。在我国长期以来认为UC是内科治疗的范畴,治疗由内科医生主导,对外科治疗没有统一的共识和规范,往往造成内科治疗缺乏合理限度,患者常常拖延到病情较重时才考虑手术治疗,手术时机的延迟造成手术风险加大、肠造口比例增加和术后并发症的增多,这也使得外科治疗的价值没有得到准确的评价和应有的重视。UC的外科治疗是以安全有效为前提, 选择的手术方式最好能保证患者术后良好的生活质量。目前外科治疗UC主要方式有结肠部分切除,全结肠切除、回肠造口、全结肠切除、回肠直肠吻合,全结直肠切除回肠贮袋肛管吻合术(IPAA)等。IPAA可以彻底切除病变及潜在病变组织,保留了括约肌,保证患者控便功能,兼顾了患者的生活质量,是治疗溃疡性结肠炎的首选术式。发达国家的UC 诊治指南中均已明确了IPAA 可以治愈UC,术后生活质量接近正常人群。随着微创技术的发展,腹腔镜下溃疡性结肠炎手术逐步开展起来。相比开腹手术而言,腹腔镜下IPAA手术具有术后活动早、粘连少、排气早等优点。5 总结和展望我国根据自身国情,先后5次制定UC 诊治共识,为提高我国UC 的诊治水平发挥重要作用。目前我国UC内科治疗与国际接轨,诊治水平逐步接近先进,未来将在UC 的特异性诊断、预防复发和完善治疗策略等方面进行更多的研究。UC 外科治疗地位和作用日益凸显,但我国尚缺乏明确的外科应用共识,外科治疗理念与技术与国际先进水平存在很大差距。主要体现在手术干预相对较晚,只有病程迁延的患者,内科治疗无效,病情危重时才求助于外科治疗,这时患者往往身体状态差,围手术期并发症风险与死亡率较高,从而降低了对外科治疗价值的评价;外科医师没有掌握先进UC 外科治疗理念,普遍存在术式不规范问题,没有明确RP-IPAA 在UC 治疗中的地位和作用,影响了UC 外科治疗水平的提升;对UC 患者的宣教不足,可以择期手术的患者常常由于不了解病情特点而拒绝手术,当病情进展时不得不接受急诊手术治疗,肠造瘘的可能增加,影响生活质量。进一步提高我国UC 诊治水平,应制定统一的诊断评价标准,获得更多的循证医学证据,建立符合我国国情的内外科综合诊治规范;加强外科规范治疗技术和理念的推广;加强患者的宣教,提高患者接受内科和外科治疗的依从性;应建立多学科合作MDT模式,内、外科,包括感染、营养、影像、心理、护理及病理科等科室医生加强沟通合作,确定内科治疗限度和外科手术时机,从而提出个体化治疗方案,真正使UC患者受益。参考文献略临床消化病杂志 第27卷第5期第315页
王猛 主治医师 哈医大二院 结直肠肿瘤外科1663人已读
问诊记录 查看全部
- 结肠癌,病理没取出肿瘤细胞,肠镜看着不好 首先查肿瘤标志物时反应高,然后 这种情况能否马上住进咱们医院呢?我现在想转院过去总交流次数7已给处置建议
- 冠心病,上过心脏支架,高血压 6.19日做的胃肠镜检查,无其他不 王教授您好,上周末您给我父亲在大庆人民医院的手术大...总交流次数7
- 结肠癌 请教王教授下一步治疗方案 病人两个月前开始胃胀、腹胀,6月18日入院检查肿瘤标志物 c... 请问王教授治疗意见方向 目前我母亲在大庆人民医院点滴补液治疗 已做血常规,肝功,全腹CT和胸部CT,...总交流次数4
- 直肠肿瘤造瘘术后4月 患者4月前行直肠肿瘤手术及临时转流造瘘手术,现饮食正常,无腹... 有没有什么办法可以解决吻合口上方狭窄问题,使患者能够还纳!现在有肠镜报告,核磁结果明天能出来!总交流次数5
- 乳腺癌转移又导致胳膊肌肉萎缩 乳腺癌转移又导致胳膊肌肉萎...总交流次数5










