精选内容
-
哈医大一院肝脏微创外科再次应用手术机器人成功完成高难度复杂肝门部胆管癌根治性切除手术
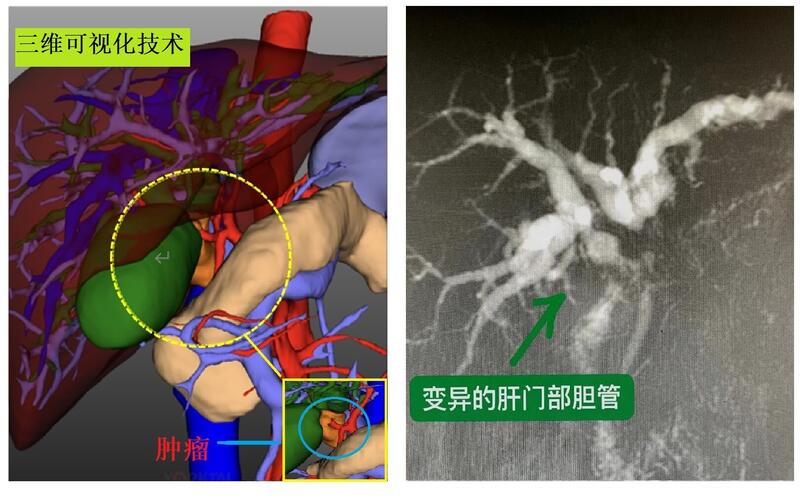
近日,哈医大一院肝脏微创外科团队在主任麻勇教授的带领下,成功完成1例合并胆道变异的高难度复杂肝门胆管癌根治切除手术,通过腹壁五个8毫米的小孔,完整切除了位于第一肝门部的胆管肿瘤,在彻底解决患者病痛的同时,利用机器人辅助操作的优势,完成了复杂胆道系统的重建。患者术后恢复顺利,无并发症,术后1周即康复出院。该类手术的多次成功开展,标志着哈医大一院达芬奇机器人肝胆外科手术已经达到国内先进水平。患者为43岁女患,既往并无乙肝或其他相关肝病病史,半月前忽然出现皮肤巩膜黄染并于当地就诊,发现肝门部有一肿瘤,经朋友推荐,慕名前来我院肝脏微创外科就诊。入院后,麻勇教授带领肝脏微创外科团队,结合患者病史,查体及相关辅助检查,术前诊断为肝门部胆管癌,病灶大小约28mm×21mm,导致胆道完全梗阻。患者影像学病例资料 进一步通过三维可视化评估技术,确定瘤体主要位于肝门胆道(见图),其与肝门部的重要脉管系统,尤其是肝动脉关系极为密切。此外,该患者存在胆道变异,在肝门部可见异常粗大的副右肝管,使得手术难度进一步提高。张女士身体羸弱,黄疸严重,如采取传统的开刀手术,单是腹部近30cm的切口就是个巨大打击,同时,张女士肝脏储备功能较差,无法接受传统大范围的肝切除。在这种情况下,麻勇教授团队制定了应用本院最先进的第四代达芬奇机器人进行微创手术切除的方案,同时运用了当前更为精准的围肝门切除技术理念,术中精细解剖了肝门部所有脉管,保住了肝右动脉,最终进行了围肝门切除、胆道切除整型重建、两处胆肠吻合、肠肠吻合、胆囊切除术、肝门部淋巴结清扫等精细操作。手术时间约5个小时,出血仅50ml。 麻勇教授介绍,肝门胆管癌虽然瘤体体积并不大,但其身处第一肝门核心位置,与肝动脉、门静脉系统的解剖关系极为密切,大大增加了手术的难度和风险。医生需要根据术前增强CT影像及三维可视化技术,对患者肝脏整体脉管结构分布及可能变异有所了解,这样才能够在手术过程中精准操作,避免损伤需要保留的脉管;同时,对于此类特殊部位的肿瘤,术中给予医生操作的空间往往十分有限,术中需要保证胆管切缘的绝对阴性及肝门部淋巴结的确切清扫方能实现肿瘤的根治性切除,而这一点正是达芬奇手术机器人手术操作的优势所在,术中可以借助机器人的四个机械臂多角度地灵活转换,在避免损伤其他脉管系统的前提下,实现胆道系统的重建及肝门部淋巴结的清扫。此外,达芬奇机器人手术系统还将术中超声技术和ICG荧光导航技术进行了整合应用,对于肿瘤边界、切缘的实时判定和精准把控具有重要意义。患者出院时与肝脏微创外科医疗团队合影 哈医大一院普外科主任孙备教授介绍,随着近年来肝胆解剖学的深入研究以及微创技术的提高,越来越多曾经被认为是微创手术“禁忌证”的疾病,也渐渐成为了微创手术的适应证。哈医大一院引进的第四代“达芬奇”机器人手术系统是对传统腹腔镜微创手术器械的重大突破。机器人的仿真机械手腕可以提供7个自由度的灵活调节,完全重现并超越人手的活动范围,让手术器械能够在狭小空间进行精细灵活的操作,同时还可以过滤人手的震颤,保障动作的安全稳健。同时,机器人可以为术者提供放大10-15倍的裸眼3D视野,能够让术者的视野更加精准和真切。这例复杂肝门胆管癌手术的成功完成就是充分利用了机器人操作精准、稳健、灵巧等特点,避免术中误伤重要血管和周围脏器,最终实现了手术收益最大化。 哈医大一院肝脏微创外科秉承以微创技术理念诊治肝胆疾病为宗旨和特色,主要致力于腹腔镜及机器人下肝、胆、脾脏良恶性疾病的微创手术治疗。科室可在腹腔镜或机器人下完成精准肝段切除、半肝切除、肝三叶切除、胆总管囊肿切除、肝癌复发再切除、联合脏器切除术、肝门胆管癌根治术、各类脾保留手术、复杂胆囊及胆道等中高难度手术,其中达芬奇机器人手术例数已达百余例,处在全国先进水平,力争实现医疗安全最大化及手术损伤最小化的有机结合,服务广大龙江患者。
 麻勇医生的科普号
麻勇医生的科普号 2022年05月20日
2022年05月20日 1034
1034
 0
0
 8
8
-
肝门部胆管癌的药物治疗
晚期肝门部胆管癌患者,全身化疗是主要治疗手段,以获得更长的生存时间。ABC-02Ⅲ期的临床试验,证实了吉西他滨联合顺铂方案在进展期胆道肿瘤中的优势,使之成为胆道肿瘤标准一线化疗方案,并在亚组分析中,发现该方案在肝门部胆管癌治疗中,比胆囊癌有更明显的生存获益。日本的一项Ⅲ期临床试验,也证实吉西他滨联合替吉奥在生存期上不劣于吉西他滨联合顺铂方案,且无需水化,是一项更加方便的治疗选择。此外,吉西他滨联合奥沙利铂或联合卡培他滨取得类似疗效,均属于一线胆道肿瘤的化疗方案。这些化疗方案不仅用于晚期胆管癌的治疗,对于胆管癌术后的辅助化疗,也有潜在的生存获益,尤其是对于淋巴结阳性以及R1切除的高危型患者。但是,对于晚期或复发性肝门部胆管癌,一线化疗方案的疗效无法令人满意,即使根据ABC-02研究结果,中位疾病无进展生存期(PFS)也仅8个月,中位总生存期(OS)11.7个月。至于肝门部胆管癌的二线化疗方案少见,2019年美国临床肿瘤协会(ASCO)公布ABC⁃06研究结果显示:奥沙利铂联合氟尿嘧啶(mFOLFOX)方案有望成为治疗胆管癌的二线化疗方案。由于面临治疗手段不足和预后不佳等问题,所以迫切需要找到新的治疗方式来突破肝门部胆管癌治疗的瓶颈。随着对肝门胆管癌基因表达谱研究的深入和二代基因测序技术的发展,已经发现了一些潜在的治疗靶点,如成纤维细胞生长因子受体2(fibroblastgrowthfactorreceptor2,FGFR2)。美国食品药品管理局(FDA)批准的首款用于治疗晚期胆管癌患者的分子靶向FGFR2抑制剂培米替尼(Pemigatinib),开启了胆管癌靶向治疗的新时代。该药于2020年5月底在美国正式上市,另外针对异柠檬酸脱氢酶1(isocitratedehydrogenase1,IDH1)靶向药依维替尼(Ivosidenib)也取得了令人可喜的疗效。但针对其他靶点,如血管内皮生长因子(Vascularendotllelialgrowthfactor,VEGF)、抗人表皮生长因子受体2(humanepidermalgrowthfactorreceptor2,HER2)等的抑制剂,目前大多是个案报道,或局限于I、II期临床试验,需要大样本多中心的临床数据加以证实。近年来随着免疫检查点的发现,特别是针对PD-1/PD-L1抗体相继问世,肿瘤免疫治疗进入了一个新的时代。KEYNOTE028是一项关于帕博利珠单克隆抗体的Ib期临床试验,招募肿瘤PD⁃L1表达阳性病人,该研究结果显示:23例胆管癌病人中,客观缓解率为17%(4/23),提示ICIs在胆管癌中的初步活性。KEYNOTE158在2020年1月公布进一步研究结果显示,帕博利珠单克隆抗体在高水平微卫星不稳定性和(或)错配修复缺乏特征的病人中,可能具有疗效(客观缓解率为41%,中位生存时间为24.3个月),具有较好的应用前景。从目前已有的研究结果来看,化疗联合靶向、免疫治疗在肝门部胆管癌中显示出良好的前景,但总体疗效尚不确切,需在体外和动物模型中进行针对性的临床前研究。根据临床前的研究效果,逐步开展多中心、大样本、随机对照临床试验加以证实。
陈炜医生的科普号 2022年03月07日
2022年03月07日 1125
1125
 0
0
 2
2
-
肝门部胆管癌的淋巴结清扫
肝门部胆管癌在胆总管旁淋巴结(NO.12b)转移的发生率最高(27.1%~42.7%),其次为门静脉周围淋巴结(NO.12p)(30.9%~35.7%)、肝总动脉旁淋巴结(NO.8)(27.3%~31.3%)和胰十二指肠后淋巴结(NO.13)(14.5%~50.0%),腹主动脉旁淋巴结(NO.16)转移率约17.3%,而腹腔干周围(NO.9)和肠系膜上血管(NO.14)周围淋巴结转移发生率低。肝门部胆管癌侵犯各组淋巴结的过程中,通常最先侵犯NO.12b淋巴结,之后再累及NO.12p、NO.13和NO.8淋巴结,最后蔓延至NO.16淋巴结淋巴结。因此,对于肝门部胆管癌,除极少数早期病例(BismuthⅠ型、乳头型、高分化等且无淋巴结转移和神经丛侵犯)理论上讲行单纯肝外胆管切除可以获得R0切除外,大多数病例需要行区域淋巴清扫。日本肝胆胰外科协会(2015年)和AJCC(2017年)发布的肝门部胆管癌TNM分期中,将区域淋巴结的定义为分布于肝十二指肠韧带内、肝总动脉周围和胰头十二指肠后上方的淋巴结(即NO.12、8和13a)。若在该区域之外发现阳性淋巴结,则归为远处转移。区域淋巴结清扫是肝门部胆管癌手术的重要组成部分,意义主要包括诊断和治疗两个方面。其诊断的意义在于可以为肿瘤分期提供确切的诊断信息,有助于判断预后并且为后续进一步辅助治疗提供病理学依据。肝门部淋巴结转移已被证实为影响肝门部胆管癌预后的重要因素。Bagante等报道,淋巴结转移阳性者1、3和5年生存率分别为62.9%、25.4%和15.4%,而淋巴结转移阴性者上述生存率分别为80.2%、44.8%和22.4%。日本名古屋大学Igami等对428例肝门部胆管癌进行回顾性研究发现,在接受了根治性切除的无淋巴结转移患者的5年生存率达60%以上,而有淋巴结转移者仅为21%,提示无论切缘情况如何,淋巴结转移是其独立预后因素。那么,超出区域淋巴结的扩大清扫,是否给患者带来益处呢?扩大淋巴清扫范围,能获得更多的淋巴结数,有助于更精确的分期和判断预后。北京大学人民医院肝胆外科总结了10年肝门部胆管癌患者的临床资料,对于术前影像学资料及术中探查发现远处淋巴结可疑转移进行有针对性扩大淋巴结清扫,发现其生存时间优于区域淋巴结清扫的患者,且并未增加术后并发症发生率。然而,更多的学者认为扩大淋巴清扫无意义,尤其是涉及腹主动脉周围的淋巴结时,由于解剖关系较复杂,手术难度增大,术中和术后并发症率的风险也明显上升。Kitagawa等在对110例肝门部胆管癌患者的回顾性研究中发现,对于肉眼可见的NO.16淋巴结转移阳性者,即使完成了扩大淋巴结清扫术,术后平均生存时间也仅为7.6个月,5年生存率为0,且总并发症发生率高达63%。扩大淋巴结清扫范围能否在保证安全性的前提下改善预后,还是仅仅能提高分期的准确性,有待开展高质量前瞻性的临床研究。参考文献1. BaganteF,TranT,SpolveratoG,etal.Perihilarcholangio-carcinoma:numberofnodesexaminedandoptimallymphnodeprognosticscheme.JAmCollSurg,2016,222(5):750-759.2. IgamiT,NishioH,EbataT,etal.Surgicaltreatmentofhilarcholangiocarcinomainthe“newera”:theNagoyaUniversityexperience.JHepatobiliaryPancreatSci,2010,17(4):449-454.3. KitagawaY,NaginoM,KamiyaJ,etal.Lymphnodemetastasisfromhilarcholangiocarcinoma:auditof110patientswhounderwentregionalandparaaorticnodedissection[J].AnnSurg,2001,233(3):385⁃392.
陈炜医生的科普号 2022年03月01日
2022年03月01日 741
741
 0
0
 0
0
-
肝门部胆管癌肝切除范围的争论
由于术前、术中很难判断肝门胆管肿瘤镜下浸润的确切长度和宽度;同时,术中胆管切缘冰冻切片检查的准确性、敏感性、特异性分别为56.5%、75.0%和46.7%,胆管切缘难以保证阴性。因此,欧美和日本学者多提倡大范围肝切除,改善患者预后。大范围肝切除可以整块切除癌细胞直接浸润的肝组织、相应的血管神经组织和肝内胆管转移癌,提高了肝门部胆管癌的R0切除率,降低复发率。同时,半肝切除后,有助显露肝门,有利于受侵肝动脉与门静脉的处理,有利于提高胆肠吻合的精准度,提高了手术安全性。对于BismuthI型和lI型的患者,联合肝切除也对提高生存期有益。IkeyamaT等总结54例I型和II型肝门胆管癌病例,认为病理类型不同,手术切除范围也相应不同。结节型或浸润型I、II型肝门胆管癌,行半肝联合尾状叶切除(18例)能确保R0根治性切除(100%),而小范围或无肝切除R0根治切除率仅为53.8%;乳头型的I、II型肝门胆管癌,只要确保切缘阴性即可,不必加行肝切除。由于大范围肝切除需牺牲大量无辜的肝实质,术后胆漏、肝功能衰竭等并发症率明显升高,同时肝门胆管癌具有局部浸润生长范围一般小于10mm的生物学特性,在兼顾肿瘤根治性切除和脏器功能保护之间平衡的基础上,部分学者提出了小范围肝切除的理念。在一些严格选择的肝门部胆管癌病例,采用小范围肝切除,可取得良好的疗效,总生存时间和复发时间与联合肝切除相当,术后并发症却显著降低。然而,由于存在胆管粘膜和/或胆管环周切除长度不够以及R0根治切除率下降的疑问,同时由于肝门显露困难,手术难度明显提高,胆道重建也困难。因此,开展小范围肝切除的单位较少,存在缺乏大样本病例的随访、疗效有待观察和有严格限制范围的适应证等弊端。 大小范围肝切除之争,实质上是如何确保肝门部胆管癌手术的胆管轴向和侧方切缘均阴性,达到R0根治性切除,这需在肝脏切除体积与围手术期根治性切除率和安全性、生活质量之间达到平衡,此外还要考虑技术推广的容易性。要达到该目的,近期可依据术前影像学检查和评估设计个体化手术方案,以及术中的再评估和决策,远期则要靠大样本、前瞻性和随机对照研究。参考文献IkeyamaT,NaginoM,OdaK,etal.SurgicalapproachtobismuthTypeIandIIhilarcholangiocarcinomas:auditof54consecutivecases. AnnSurg,2007,246(6):1052-1057.
陈炜医生的科普号 2022年03月01日
2022年03月01日 507
507
 0
0
 1
1
-
ALPPS和PVE在肝门胆管癌中的应用
联合肝脏分割和门静脉结扎的分阶段肝切除术(AssociatingLiverPartitionAndPortalVeinLigationForStagedHepatectomy,ALPPS)与门静脉栓塞术(portalveinembolization,PVE)在肝门胆管癌中的应用,哪个更好?肝门部胆管癌手术常需联合大范围肝切除,剩余肝体积和功能若不能维持机体正常生理功能,则易发生肝功能不全甚至衰竭。如果剩余肝脏无病变,其体积需大于等于全肝体积的30%;若肝脏存在病变(如梗阻性黄疸、脂肪肝、肝纤维化、肝硬化等),剩余肝体积需大于等于40%才能显著降低肝切除术后肝衰竭的发生率。若剩余肝体积达不到上述标准,可通过ALPPS或PVE两种方法来增加保留侧肝脏的体积。ALPPS既可以把供应肿瘤的入肝血流全部阻断,同时也把左右半肝之间的可能侧支循环全部阻断,结果能有效刺激预留肝脏进一步肥大,为第二次手术创造条件。其优势在于一期手术后剩余肝体积的迅速增生,扩大了肝脏的可切除范围。目前,ALPPS增加预留肝脏体积的分子机制尚无一致的意见,可能与一些炎症因子、生长因子与肝细胞增殖等有关。由于ALPPS术后较高的并发症发生率和病死率,该方法争论较大,但仍有不少专家持不同意见。肝门部胆管癌患者术后高发的并发症与其他类型肿瘤的并发症类型基本相同,多为出血、胆漏、腹腔感染、肝功能不全或衰竭等。结合现阶段ALPPS技术的发展和改进,通过采用绕肝止血带法、部分离断肝实质法、射频(微波)消融断肝法等方式,降低了手术创伤和并发症发生率。总的来说,现在ALPPS的改进趋势是,从两步开腹手术向第一步微创,第二步开腹,甚至两步微创转变。PVE通过阻断栓塞侧门静脉分支,减少栓塞侧门脉血流供应,促进栓塞侧肝叶萎缩和对侧增大,从而使不能直接手术切除的患者获得手术切除的机会。HiguchiR等通过对836例肝门部胆管癌患者的回顾分析中发现,采用剩余肝体积小于40%作为实施PVE的标准,实施后患者的剩余肝体积可以提高33%。78%的患者完成了二期手术,不能施行二期切除的患者主要原因为远处转移和局部进展,二期术后死亡率为3.7%。NaginoM等对150例术后可能剩余肝体积不足的胆管癌患者术前行PVE,使得132例成功实施根治性切除。美国肝胆胰协会一项专家共识认为,术前PVE可以提高肝门部胆管癌患者术后残肝体积,是一种安全有效的方式。然而,PVE也存在不少缺点。如PVE术后出血、肝脓肿等,术后等待肝增生的时间长,增生效果不满意,有30%以上的失败率等。部分病例在等待二期切除期间,生长因子释放可能促进肿瘤进展。肝门部胆管癌通过ALPPS或PVE来增加肝脏体积,孰优孰劣,目前还有争议。ALPPS容许在第一次术中才决定切除哪侧肝,这与PVE要求在术前决定栓塞哪侧肝不同。而PVE增生速度虽慢,但一部分恶性程度高的肿瘤可能展现出其转移潜能,从而避免一部分不必要的手术。然而不管采取何种方式,最重要的都需要考虑安全性和有效性两个方面。SchaddeE等总结了83例PVE和48例ALPPS后肝切除的临床资料,认为在安全性方面,ALPPS联合肝切除术的总体并发症发生率、死亡率都高PVE联合肝切除;有效性方面,ALPPS高于PVE。所以,究竟采用哪种增肝体积方法,术前对于肝门部胆管癌患者整体情况的筛选以及本中心的能力和经验极为重要。参考文献HiguchiR,YamamotoM.Indicationsforportalveinembolizationinperihilarcholangiocarcinoma[J].JHepatobiliaryPancreatSci,2014,21(8):542-549.NaginoM,KamiyaJ,NishioH,etal.Twohundredfortyconsecutiveportalveinembolizationsbeforeextendedhepatectomyforbiliarycancer:surgicaloutcomeandlong-termfollow-up. AnnSurg,2006,243(3):364-372.SchaddeE,ArdilesV,SlankamenacK,etal.ALPPSoffersabetterchanceofcompleteresectioninpatientswithprimarilyunresectablelivertumorscomparedwithconventional-stagedhepatectomies:resultsofamulticenteranalysis[J].WorldJSurg,2014,38(6):1510-1519.
陈炜医生的科普号 2022年02月15日
2022年02月15日 427
427
 0
0
 0
0
-
肝门部胆管癌术前胆道引流减轻黄疸的争议与策略
梗阻性黄疸是肝门部胆管癌的主要临床表现,其所致的高胆红素血症对肝功能、心肌细胞、肾小管上皮细胞等均可造成严重的损害。因此,对于合并严重梗阻性黄疸患者,多数学者认为应在术前胆道引流,减轻黄疸,提高预留肝脏的储备功能。 肝门部胆管癌术前胆道引流的方式不外乎三种:经皮经肝穿刺胆管引流术(PTCD)、内镜下鼻胆管引流(ENBD)和内镜逆行胆管支架引流(ERBD)。三种胆道引流方式各有利弊,对于选择何种胆道引流方式,目前很大程度取决于各国学者对各种引流方式经验积累,仍缺乏高级别的循证医学证据。??? 关于术前胆道引流方式与肿瘤转移之间的关系,颇有争议。Komaya K等总结了320例术前胆道引流的肝门胆管癌患者,其中168例行PTCD,152例行内镜下引流,5年生存率PTCD组(37%)明显低于内镜下引流组(44.3%),多因素分析提示PTCD是生存期短和肿瘤播散转移的独立危险因素,故推荐肝门部胆管癌术前采用ERBD方法行胆道引流。另一篇文献的研究结果类似,术前ENBD引流的患者,术后2年和5年生存率均显著高于PTCD患者,多变量分析提示PTCD 是术后肿瘤扩散的独立危险因素。 然而,这些研究都是回顾性的、非随机对照,而且这些文章常存在较大的选择偏倚,这些偏倚并不能通过单因素或多因素分析等单纯的数据分析方法来消除,因此得出结论的可靠性也降低。 要探讨不同的术前胆道引流方法在患者生存率、并发症率以及引流成功率上的区别,还需要多样本的随机对照研究来实现。但是,胆道引流的技术上有困难,而且不同医院的引流技术水平和策略也不一样,很难达到均一性。Coelen 等报道了荷兰开展的迄今唯一一项有关肝门部胆管癌术前胆道引流前瞻性、多中心、随机对照试验,但由于过高的全因(all-cause)病死率和胆管炎发病率,该研究不得不提前终止,并未得出具有指导意义的结论。 术前胆道引流如果持续时间过短,则无法实现减黄的目标;如果持续时间过长,肿瘤可能进一步发展,不仅延误手术时机,还会增加引流相关并发症的发生。引流持续时间的界定实际上就是黄疸降到什么程度可以采取手术。国内外推荐术前减黄至少持续2周以上,有文献认为梗阻性黄疸胆道引流至少4~6周,肝功能方可较为全面的恢复,但事实上缺乏高级别证据支持。也有文献认为待血清总胆红素降至85μmol/L以下时即可手术,不必降至正常。田伏洲等以引流后血清胆红素下降速度作为肝脏储备功能的判断指标并据此建立引流时间标准:胆红素平均每周递减30%以上,可能反映出患者具有良好的肝脏储备能力。因此,只要减黄后连续2周胆红素递减30%以上,即可对患者实施手术治疗。如果每周胆红素递减率小于 30%者,手术应推迟至3周以后。如果减黄后胆红素仍旧上升,在除外引流管梗阻等因素后应取消手术,因为即使行内引流术也无法达到减黄的目的。 因此,术前减黄对于高危肝门部胆管癌患者仍是必需的,有助于提高手术安全性。PTCD和内镜下胆道引流均为术前减黄安全有效的方法,不同中心根据自身经验选择最合适的方法。黄疸患者的肝脏储备能力,可根据引流后胆红素下降速率来判断。 参考文献 Komaya K, Ebata T, Yokoyama Y, et al. Verification of the oncologic inferiority of percutaneous biliary drainage to endoscopic drainage: A propensity score matching analysis of resectable perihilar cholangiocarcinoma. Surgery,2017,161(2):394-404. Higuchi R, Yazawa T, Uemura S, et al. ENBD is associated with decreased tumor dissemination compared to PTBD in perihilar cholangiocarcinoma[J]. J Gastrointest Surg, 2017, 21(9): 1506-1514. Coelen RJS, Roos E, Wiggers JK, et al. Endoscopic versus percutaneous biliary drainage in patients with resectable perihilar cholangiocarcinoma: a multicentre, randomised controlled trial.?Lancet Gastroenterol Hepatol. 2018;3(10):681-690. ewnath ME, Karsten TM, Prins MH, et al. A meta-analysis on the efficacy of preoperative biliary drainage for tumors causing obstructive jaundice.?Ann Surg, 2002,236(1):17-27 田伏洲,石力,汤礼军,等. 对恶性梗阻性黄疸术前减黄指标的再认识(附28例临床分析)[J]. 中国现代普通外科进展,2010,13(1):1-4.
陈炜医生的科普号 2022年02月13日
2022年02月13日 618
618
 0
0
 1
1
-
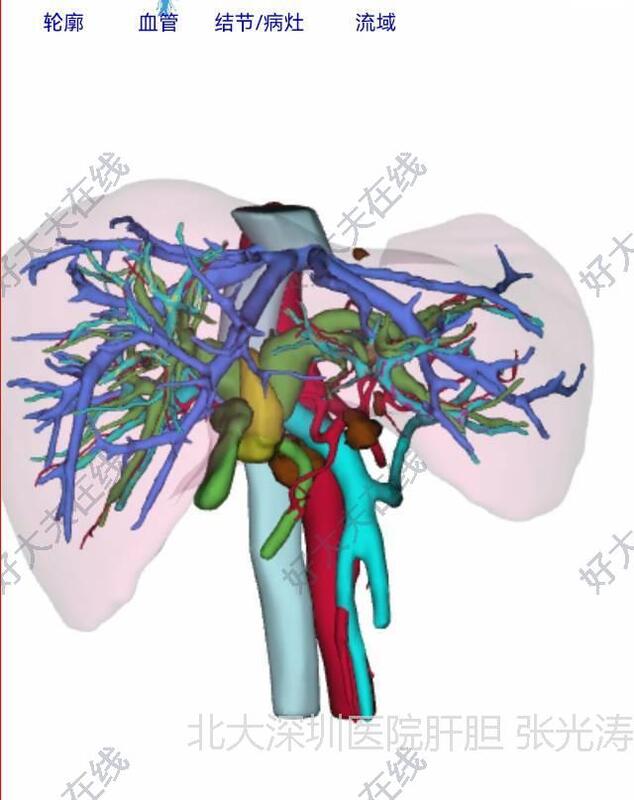
机器人肝门胆管癌根治
 张光涛医生的科普号
张光涛医生的科普号 2021年12月30日
2021年12月30日 197
197
 0
0
 0
0
-
肝门胆管癌外科治疗进展之——术前门静脉栓塞(PVE)
就肝门部胆管癌患者的生存率和生活质量而言,手术根治切除仍然优于其它治疗手段。目前,联合半肝切除、尾状叶切除已成为规范的根治术式(Bismuth II型以上),为达到多个切缘阴性,部分患者往往需要联合血管切除重建和/或更大范围的肝切除。肝切除的体积越大,患者由于残余肝体积不够而发展成术后肝衰竭的风险越大。门静脉栓塞(Portal vein embolization, PVE)作为克服这一问题的手段,自1984年Makuuchi等报告首次应用于肝门胆管癌以来,在日本和欧美已被应用于转移性肝癌、肝细胞癌和胆道肿瘤。大量的回顾性临床研究证明:PVE能够诱导非栓塞肝叶术前增大,通过增加肝脏功能储备,有助于保护病人术后免除肝功能衰竭。 近年来,PVE选择指征、门静脉入路、栓塞材料类型、并发症、未来残余肝(Future liver remnant, FLR)功能评价方法等方面争议和进展并存,仍缺乏PVE的多中心的随机对照研究。肝门部胆管癌作为PVE的特殊适应症,其选择指征和程序不应该完全等同于肝癌或结直肠癌肝转移,因为大部分肝门胆管癌患者存在胆道梗阻,一些并发胆管炎,少数还合并肝硬化、糖尿病等疾病。而在亚洲PVE的主要适应症是胆道肿瘤,其中又以肝门胆管癌居多,特别是在日本。国内肝门胆管癌术前PVE的研究正在积极开展。本文结合笔者(单位:上海东方肝胆外科医院胆道一科)截止到2010年底的40例肝门胆管癌的PVE经验进行探讨。 PVE后肝体积变化的影响因素 CT肝体积测定方法 CT是最常用的、最可靠的评价PVE前后体积变化的方法。通常扫描间隔2-10mm,通过静脉注入对比剂增强扫描,足够评价每个肝段体积。目前多采用多排CT,应用3-D最大强度投影技术,为每一肝段提供更准确的体积分析。研究肝叶体积变化的指标多表示为:PVE后体积增生/萎缩的绝对值(cm3)、非栓塞肝叶(或FLR)增生率(%),非栓塞肝叶占全肝的比例(%)等。尽管3D-CT体积测定看起来比传统的2D-CT更准确,但它仍可能产生约10%错误率。对于未来残余肝(25%-35%全肝体积)较小的边缘候选患者,这个错误可能是巨大的。笔者体会,CT体积测定无论是采用直接面积测量法还是通过软件计算,都是建立在肝脏分叶分段的解剖基础之上,要求实施测量的操作者对正常及变异门静脉、肝静脉走行比较熟悉,对于复杂血管走行的病例应该在放射科和外科医生的共同研究下确定。 CT肝体积测定时机 欧美中心肝体积复测时间多在PVE 4周以后、大部分患者为结肠癌肝转移(FLR增生时间长、无急慢性肝功能损害)。Jaeck等报告了145例PVE,在PVE后4~8周,FLR由472±20cm3增加了197±12cm3,FLR增生率48±32(4~150)%。其PVE至肝切除术间隔时间更长(2.2±0.1月)。日本报告的PVE肝体积复测时间多在PVE后3周以内,病例多数为胆道肿瘤(肝内胆管癌、肝门胆管癌、胆囊癌等),FLR 增生率低于欧美报告,但PVE至手术间隔时间较短。Nagino等报告的240例PVE(PVE前胆道梗阻采用全肝胆道引流),在PVE后平均2周,非栓塞肝叶由361±119cm3增加了约99cm3,增生率33±24(0~122)%。一般CT体积复测时间在PVE 2周或以后,选择复测的时机需要根据患者FLR体积和功能代偿增生的情况、肿瘤进展的速度等因素决定。 肝门胆管癌患者的胆道梗阻与胆管炎 来自日本的报告,一般认为肝门胆管癌患者非栓塞肝叶增生率约20%。一般来说,PVE能在14天内诱导非栓塞叶代偿性增生,并且无严重的并发症。然而,在梗阻性黄疸或胆管炎患者,增生的程度受到严重的影响,一个肝段的胆道梗阻不仅损害梗阻肝叶的细胞功能,而且损害非梗阻肝叶。为了诱导FLR体积增生到足够大,可能需要更长的栓塞与手术时间间隔。此外,患者合并肝内胆管炎,其大部肝切除术后(切除3个或以上肝段)并发症发生率和死亡率比不合并胆管炎的患者更糟糕。目前,对合并胆管炎,PVE前积极引流炎症胆管已成为共识。对于无胆管炎的肝门胆管癌患者,全肝胆道引流(Total biliary drainage, TBD)还是仅引流FLR的选择性胆道引流(Selective biliary drainage, SBD)仍然存在争议。待患者血清TB降至2-5mg/dl(34-86?mol/L)以下,PVE才能被执行。Makuuchi等首先报告了15例SBD后的PVE,仅引流非栓塞肝叶比双侧引流增生率更高。这一现象的机制需要进一步研究。根据笔者目前的40例经验,在PVE前32例采用了SBD,达到了非栓塞肝叶有效的体积增大。当单侧引流血清胆红素水平仍然很高单时,TBD可能是PVE前唯一的选择。 一些研究报告显示:胆道内引流比外引流能提供更好的肝再生环境,内引流也有助于维持肠道完整性,后者可能保持正常的肠道免疫功能、使病人更好地耐受扩大肝切除的严重影响。如果进行外引流,引流出的胆汁应该尽可能地回输。 影响肝再生能力的其它因素 在能够耐受的范围,肝脏再生的程度与它承受的损害程度成正比。显然相同范围的肝切除术比PVE更能诱导肝脏再生。同样是右半肝切除术前的右侧PVE,对边缘FLR体积比的患者可能比非边缘患者产生的增生效果更强烈。笔者前期的16例PVE研究(SBD基础上)显示,PVE后2周复测CT,非栓塞肝叶体积由PVE前892±278cm3增加了66±36cm3(P<0.01),肝增生速度5.1±2.7cm3/d。增生结果比国外报告略低,主要原因可能是非栓塞肝叶的体积比较大(48.5±12.6%)。另外,肝炎肝硬化、糖尿病、慢性酒精中毒、严重脂肪肝和营养不良、高龄、男性也被认为是限制肝脏增生的因素。 未来残余肝体积的PVE选择指征 迄今仍没有未来残肝体积明确的PVE指征。 Ladurner、Hemming等对估计残肝体积≤25%总肝体积患者施行PVE。他们只将PVE限用于预期小残余肝的患者,其通常被认为是无法耐受切除。其他研究组PVE指征为估计未来残肝的比率<30%或<40%。由于PVE明显改善术后的并发症发病率和死亡率,我们是否应该将PVE仅限用于边缘患者?假如PVE的施行带来零死亡率和最低的并发症发病率,我们能将适应症扩大到那些准备接受扩大肝切除的患者。实际上,一些中心已经将右半肝切除作为PVE的指征,可能其FLR体积比>40%。Elias等提出,如果病人经历了多个疗程的化疗,PVE的选择指征--体积比下限应该提高。甚至有学者提出肝纤维化患者的大部肝切除术前均应该施行PVE。尽管肝门胆管癌患者的肝脏基础通常比较正常,胆道梗阻如果得到适当的引流多数肝功能损害是可逆的。但是应该看到,梗阻性黄疸造成的FLR功能损害程度可以相差很大,长期胆道梗阻合并胆道感染导致的黄疸往往是混合性的,通常都存在不同程度的消化功能障碍、营养不良。特别是高龄、合并肝硬化、糖尿病的患者,严格的体积比指征可能将被拒绝行PVE的临界患者置于术后肝衰竭的危险境地。根据我们的经验,肝门胆管癌术前PVE选择标准:无肝硬化且黄疸/胆管扩张至PVE时间<8周、未来残肝/全肝<50%;有肝硬化或发现黄疸/胆管扩张≥8周、未来残肝/全肝<60%。当然另一方面,PVE前对肝门胆管癌患者进行有无急慢性肝功能损害、其它限制肝再生因素的评估尤为重要。 既然PVE的目的是为了使患者尽量免除大部肝切除术后肝衰竭的风险,那么对于FLR急性或慢性肝功能损害的患者就没有必要设定<40%限制,应该适当放宽。PVE的FLR体积比选择指征应该改变,至少不应该单纯地以体积百分比划线。术前PVE的选择最终的发展趋势必然是:合理的PVE及肝切除策略、精确的FLR功能状态评估、个体化的FLR增生潜能评估、与其它促进FLR再生方法的组和应用,还有应该为术中或术后FLR被二次打击的可能留有余地。 栓塞材料 明胶海绵、纤维蛋白胶、碘化油、氰基丙烯酸酯和无水乙醇,伴或不伴栓塞钢圈,已被用作经典的栓塞材料。迄今没有随机对照研究比较这些栓塞材料的效率。一个比较明胶海绵和无水乙醇的报告表明,由于门静脉分支再通的高发生率,明胶海绵对非栓塞叶的再生无效。Nagino报告的240例PVE中,栓塞材料初期使用的纤维蛋白胶,随后改为乙醇和栓塞钢圈相结合。尽管纤维蛋白胶的再通率稍高于乙醇加线圈(8.3% vs 5.1%),但二者的非栓塞叶增生率和栓塞叶萎缩比率没有显着差异。更改栓塞材料的原因是医保系统认为纤维蛋白胶的费用太高。无水乙醇容易灌注到窦状间隙水平并损伤窦间隙的内皮细胞,其注灌注后肝脏组织损伤的程度比其他栓塞材料更严重。乙醇能够引流到终末支肝静脉,随后进入体循环。阐明乙醇灌注副作用的进一步研究是必要的,以便确定使用乙醇的合适剂量。 近年来已发展出一些新的栓塞材料,如:N-丁基氰基丙烯酸酯(NBCA)与碘化油的混合液,聚乙烯乙醇(PVA)颗粒(非球形颗粒,355~1000微米)。临床证明是有用的。最近,小球形栓塞颗粒(三丙烯基微球,100~700微米)已成为可购商品。一份报告表明,小球栓塞颗粒栓塞增生的程度比大的非球形粒子(PVA)明显提高。这些微球的好处在于:根据准备栓塞门静脉分支尺寸选择的颗粒的大小范围比较宽。可以使用较小颗粒堵塞远侧分支,而用较大颗粒端分支堵塞近侧分支。组织学结果显示,在切除肝中,三丙烯基微球比聚乙烯乙醇能造成更多的远侧栓塞。小微球不仅可以堵塞门静脉血流,也可以通过阻断肝脏微循环中的动静脉交通支,减少动脉血流。 我们的PVE目前采用了门静脉1~2级分支单纯钢圈栓塞的方法,属于近侧永久性栓塞,无明显并发症,患者耐受性非常好,明显发热(>38.5℃)都不多见。栓塞完成后门静脉造影确认栓塞支达到完全栓塞,CT体积测定证实能够有效诱导非栓塞肝叶体积增大,术中能观察到明确的增生萎缩边界。 归根到底,栓塞材料的选择服务于希望达到的栓塞目的——高效诱导非栓塞肝叶增生、更好地被患者耐受。PVE最初的临床实施是受到了以下启发:肿瘤患者一侧门静脉支受侵后的肝叶增生萎缩现象,动物试验门静脉支结扎模拟缺血诱导的促进肝再生的结果。目前仍时有临床的研究报告门静脉支结扎有效诱导肝再生;PVE动物试验研究中,门静脉结扎也常规作为一种标准的对照方法。事实上,门静脉栓塞与门静脉结扎哪个更有效仍然存在争议。栓塞的理想模式之争在所难免。一般认为:永久栓塞优于一过性栓塞,门静脉支远侧栓塞优于近侧栓塞。但Lainas等报告的采用的明胶海绵的一过性(可逆性)栓塞同样能诱导有效的肝再生;Furrer等研究认为远侧栓塞材料造成的异物反应通过截留巨噬细胞而损害了肝再生能力。 是否有必要栓塞门静脉IV段支? 肝门胆管癌经常出现肝内胆管的侵犯,有时,广泛的肝切除(如右三叶切除)是需要的。门静脉栓塞显然是必要的,因为这些患者的预计未来残肝体积是极小的。右三叶切除时是否栓塞左内叶(IV段)分支的争议仍然存在。由于门静脉的II、III、IV段分支通常起源于门静脉脐部,单独栓塞右支后,并不希望的IV段增生必然出现,II、III段的充分增生难免受到影响。从操作角度来讲,IV段支栓塞相对困难。在一些能够进行熟练进行IV支栓塞的中心,多主张栓塞该分支。Nimura等报告的右三叶PVE采用同侧路径方法,认为对准备右三叶切除而言,右三叶门静脉栓塞比标准的右支栓塞更有用,并能够增加肝门胆管癌患者手术安全性。Madoff、Vauthey等也报告了IV段栓塞。与这些报告相反,Capussotti等报告说,扩大到IV段的栓塞不应该被常规使用,因为相近的II、III段体积增长可以通过右侧PVE简单实现。答案目前还不清楚,因为这些研究包含的样本很少,同样缺乏随机对照的研究。 PVE后FLR增生不充分怎么办? PVE后患者最终无法手术的常见原因就是FLR增生不充分和肿瘤进展。PVE后非栓塞叶充分的体积增长并不是总能实现。如果增加的数量太小,肝切除应该被放弃,即使在这些患者并不存在提示肝脏再生能力已受损害因素。肝再生受损的这类病人对PVE的反应机制尚不清楚。为这些患者我们应该选择什么样的策略作为下一步的处理?由于肝动脉缓冲反应,栓塞叶肝动脉血流显著增加,而增加得血流有助于栓塞叶保持其体积。因此,对栓塞肝叶的动脉栓塞可能是进一步提高PVE效果的方法。对PVE后体积增长不充分的患者,一些学者报告了进行续惯性同侧门静脉加肝动脉栓塞是有用的。然而,这基本上意味着栓塞叶的“原位肝切除”,并具有发展为肝脓肿的高风险。因此,这种侵入性的双栓塞指征应严格选择,而且应该随时准备通过介入的办法处理随后的肝脓肿。 选择性肝内胆管无水乙醇消融可诱导注入叶萎缩和非注入叶增生。一个大鼠实验研究表明,被选择性无水乙醇注入的70%总肝脏重量肝叶,处理14天后重量减轻至不到50%总肝脏重量。相比之下,非注入叶重量上升到原来的1.6倍。注入的乙醇通过Glisson鞘浸泡并破坏肝细胞而并不损害的门静脉和肝动脉。如果栓塞叶胆管被肿瘤与其它胆管分支完全分离,也就没有损害FLR胆管的风险,这一方法(如选择性肝内胆管无水乙醇消融)可能是实现进一步体积增大的另一种选择。这反过来提示我们,对于肝门胆管癌的患者,既然PVE后FLR增生不充分可以通过胆管消融来补救,为什么PVE前不采用SBD让栓塞肝叶始终处于淤疸状态? 肝外造血干细胞已被知晓参与肝切除后肝增殖,CD133+干细胞已被用于支持心肌组织和器官再生的治疗。Am Esch等最近报告了在PVE同时,自体CD133+骨髓细胞通过门静脉输注到肝脏。在PVE完成后,CD133+细胞选择性地应用于非栓塞肝脏门静脉支。尽管这一初步研究涉及的患者较少,所提供的数据可能大有前途。在PVE后+骨髓干细胞应用组,非栓塞叶日平均体积涨幅高于单纯PVE组。对于单纯PVE体积增加不充分的患者,这一方法可能成为将来的一个对策。 未来残余肝功能的评估 肝门部胆管由于肿瘤原发部位特殊,决定了大部分肿瘤需要联合半肝/更大范围肝切除才能达到根治;由于通常肿瘤体积不大,导致了切除的肝叶大部分是具有功能的肝实质;由于术前多数合并梗阻性黄疸,造成了FLR功能不同程度的损害。不但如此,FLR功能术中仍可能遭受联合肝门血管切除重建的缺血性损害,术后有可能受到肝脓肿、肝创面感染等并发症的二次打击,如果术前还具有肝硬化、糖尿病等影响肝再生的疾病基础,那么残留肝叶功能可能很难甚至无法代偿,出现肝功能不全甚至衰竭的机会将大大增加。因此,在肝门部胆管癌计划施行大部肝切除的围手术期(尤其术前),PVE前后充分、准确地评估FLR功能非常重要。 尽管CT体积测定是衡量FLR体积代偿的可靠指标,应该明白:PVE和大部肝切除术一样,肝再生的顺序都是功能代偿优先于体积代偿,而且前者更加灵敏。由于肝脏功能、储备功能评估的方法繁多,在不同的临床中心采用的方法不尽相同。经典实用的指标包括:TB、转氨酶、PT、Pre-Alb等。大部分血清学指标都是反映全肝功能,不便估计FLR功能。当然,对于肝门胆管癌患者,双侧胆道梗阻施行包括FLR的SBD,TB即可反应胆道引流肝叶的功能。目前一些PVE前FLR功能的估算是通过药物肝代谢试验(尤其是清除率)指标,乘以FLR占全肝的体积比例来实现的。 吲哚花青绿(靛氰绿)清除率(Indocyanine green clearance rate, ICGK) PVE后肝切除的指征,不应该简单地用未来残肝的体积来确定。一般认为,65%的肝切除对肝功能正常患者是安全的。对于慢性肝病患者,肝切除应限定于小于50-60%。靛氰绿15分钟潴留率(ICGR15)或清除率(ICGK)可能是评估未来残肝功能、确定肝切除范围最有用的方法。Kubota等提出,PVE应该用于ICGR15在10%~20%的患者。另一份报告显示, PVE后ICGR15小于16%,是大部肝切除术后并发症的一个有益的预后因素。Nimura等的研究结果显示FLR的ICGK<0.05的患者术后死亡率比>0.05者明显升高。这可能是评估FLR功能的一个简单、可靠的方法。 半乳糖人血清白蛋白闪烁显像 99 mTc二乙烯三胺五乙酸半乳糖人血清白蛋白(99mTc-GSA)肝动力单光子发射断层扫描,用以肝切除术前评估剩余肝功能是另一个有用的方法。99mTc-GSA闪烁显像可造成与不同肝细胞的特定结合,并作为一项肝功能指标。非栓塞叶不仅体积增加,而且PVE后第1周99mTc-GSA摄取也显示增加。术后肝衰竭更多地发生在99mTc-GSA明显摄取较少的患者。Kubo等报告患者非栓塞叶平均增长约30%,尽管平均体积增长不到全肝的10 %。相反,患者栓塞叶平均减幅约20%。Nishiguchi等报告的胆管癌患者类似的结果(非栓塞叶增长37%;栓塞叶减少23%)。这些结果表明,FLR的功能代偿早于体积增大。有趣的是,Uesaka等通过使用两侧分离的PTBD导管,比较栓塞叶和非栓塞叶胆道ICG排泄,观察到了类似的结果。PVE后,非栓塞叶的胆道ICG排泄占全肝排泄的百分数平均增加了20.1% ,而同时非栓塞叶体积占全肝体积的百分数只增加了8.3%。因此,FLR功能不应该简单地通过其体积来评估。 PVE改善大部肝切除术后结果的贡献 是否PVE有助于改善术后结果?如上所述,没有PVE有效性的随机对照临床研究,这个问题仍然具有争议。然而,许多报告显示了PVE对大部肝切除术后结果的好处。在Nimura等报告实施PVE后,大部肝切除术后肝衰竭发生率从33.3%下降至23.8%。与此同时,胆道肿瘤(包括胆囊癌和胆管癌)大部肝切除术后死亡率从21.9%下降至9.5%。在2001年以后,死亡率只有1.6%。 在我们前期施行的16例肝门胆管癌术前PVE研究中,在PVE后2周,TB由PVE前的83.7±40.7μmol/L下降至53.5±31.2μmol/L(P<0.01),提示肝功能明显代偿。本组钢圈PVE后,13位患者最终接受了右半肝或超半肝切除术,同期非PVE肝切除组(n=33)手术类型中,右半肝或超半肝切除术近占33.3%(11/33)。尽管两组的手术死亡率(0 vs 9.1%, P>0.05)、并发症发生率(69.2% vs 63.6%, P>0.05)均无统计学差异,但PVE组全部接受了更大范围肝切除术,而且并不增加术后肝功能不全或术后并发症的风险。 由于PVE的好处是明确的,并且剩余过小的未来残肝可能具有毁灭性的风险,因而进行PVE是否有效的随机对照研究是违反伦理的,但PVE不同的栓塞模式和材料的RCT研究是可行的。从回顾性临床研究证据来看,没有围手术期死亡率,接受和不接受PVE组之间的围手术期并发症发生率也没有统计学差异。这些结果表明,至少PVE不是一种有害的方法。应该认识到:不经过PVE准备,一些肝切除的边缘候选患者将被排除在手术治疗之外,可能手术是达到根治的唯一机会。尽管如此,我们不应该忽视PVE的副作用,这也可能减少准备手术的候选患者。 PVE的风险 一般来说,PVE被认为是一个安全的方法。轻微副作用是存在的,如轻度腹痛、低热、恶心和呕吐。AST、ALT和TB水平在PVE后也可能会升高,但升高的程度是温和的,通常酶学升高不超过PVE前基线的三倍,数值1周内回落到操作前水平。有报告PVE后一过性肝功能不全,de Baere的报告中,3.2%(6/188)出现一过性肝功能衰竭,多发生在肝硬化患者(5/6),患者恢复良好、Child分级未受影响。尚未见PVE后急性肝衰死亡的报告。我们的钢圈PVE(n=16)前和其后3d患者TB、酶学指标和PT无统计学差异,提示此方法对全肝功能影响不大。血小板计数在PVE后3d比栓塞前低(P<0.01),提示血小板消耗,可能与钢圈周围血栓形成有关。虽然报告显示PVE严重副作用并不多见,我们必须意识到PVE方法的相关风险。 PVE造成的并发症(需要特殊处理或导致住院时间延长)发生率不尽相同。de Baere等回顾性评估了188位患者PVE后的不良事件,病例包括胆管癌、肝细胞癌和结直肠癌肝转移。使用NBCA混合碘化油作为主要栓塞剂,并发症发生率12.8%(24/188)。并发症包括未来残肝灌流门静脉支血栓形成、栓塞物迁移,腹腔出血,胆道出血,包膜下血肿和肝衰竭。此外,约10%的患者,肝切除因肿瘤进展、非栓塞肝增生不充分、完全的门静脉血栓形成而取消。Kodama等也分析了PVE后并发症,并发症发生率14.9%(7/47),包括气胸、包膜下血肿,动脉损伤、假性动脉瘤、胆道出血,和非栓塞门静脉支血栓形成,尽管没有病人死亡。Nimura等报告的并发症包括一例扩展的PVE后门静脉和肠系膜静脉栓塞,该患者合并S蛋白缺乏症。该患者一个主要血管的急性栓塞可能已经引发了凝血级联效应。尽管常规的高凝状态评估是不实用的,但在这些高危组患者中,至少应该这样做。他们认为,为了尽量减少非栓塞肝叶损伤,门静脉栓塞的路径应该尽可能从同侧进行。 我们的前期16例PVE并发症发生率18.7%(3/16),为穿刺点胆漏、少量钢圈移位。出现PVE胆漏的患者顺利接受了经皮穿刺腹腔引流;PVE钢圈移位2例,1例1枚钢圈移位至S4主支,术前S4主支血流未受影响,CT证实于PVE后1.2月(肝切除术后0.5月)出现S4主支栓塞,但同时伴有其他小支代偿增粗,随访至PVE后14.3月未发现其他分支的扩展栓塞。另1例2枚钢圈移位至S3支,随访至PVE后12.5月(肝切除术后11.7月)S3支仍然通畅。此两位患者手术后恢复。全部16例PVE均未出现栓塞靶静脉的再通,未出现肝脏局部坏死液化。 PVE反应性的循环生长因子释放可能会加速肿瘤的进展。在高度进展期肿瘤的患者,这可能会加速肿瘤临床分期的进展,致使患者无法手术。当然PVE前的肿瘤分期和可切除性的充分评估应该被充分重视。PVE的滥用可能明显延长了术前准备时间,提供了肿瘤分期扩展的机会,同样达不到根治切除的目的。 对于肝门胆管癌患者,如何实现安全可靠、高效快捷的PVE方法尚待同道们共同努力。
王炜煜医生的科普号 2021年11月29日
2021年11月29日 547
547
 0
0
 0
0
-
什么是肝胆管癌?
肝胆管癌是指发生在肝内胆管癌以及肝外胆管癌,具体分别阐述如下:第一、肝内胆管癌可发生于肝内任何一级胆管,约占原发性肝癌的20%,一般发生于60岁以上的老年人。其发病因素与肝寄生虫、肝胆管结石、炎症性肠病、原发性肝硬化性胆管炎、EB病毒感染等有一定的关系,临床上的表现为全身无力、腹痛、消瘦,如肿瘤侵及肝门部胆管则会出现梗阻性黄疸,甚至会出现胆汁性肝硬化。临床中以手术治疗为主,预后不良,平均存活时间不足两年。第二、肝外胆管癌,包括左右肝管、肝总管、胆囊管和胆总管,其发病率略少于胆囊癌。60岁以上人群多见,在溃疡性结肠炎、硬化性胆管炎、华支睾吸虫感染以及一些先天性胆管畸形,如先天性胆管扩张、胆管囊肿、多囊肝疾病中发病率增高。临床上是以梗阻性黄疸、体重下降、腹痛为主,也常因继发性胆管感染而出现发热。
谢峰医生的科普号 2021年03月20日
2021年03月20日 3083
3083
 0
0
 2
2
-
肝门胆管癌晚期怎么治疗?
肝门胆管癌晚期的治疗,以胆管引流,解除黄疸为主。因患者的胆道遭受阻塞,需运用引流法将梗阻解除,其治疗方式有两种,其一为通过胆道系统,经口腔放入十二指肠镜,在胆管内放置塑料或金属的支架,使胆汁能重新流入十二指肠,此种方法在医学上称为ERCP;另一种方法为PDCD,即通过肝脏穿刺到胆管进行引流。两种方式均能将胆汁通过梗阻部位引流出,达到降低黄疸的目的。
谢峰医生的科普号 2021年02月23日
2021年02月23日 1920
1920
 1
1
 0
0
肝门胆管癌相关科普号

王坚医生的科普号
王坚 主任医师
上海市第六人民医院
肝胆胰外科
3308粉丝22.9万阅读

程庆保医生的科普号
程庆保 主任医师
海军军医大学第三附属医院
肝胆外科
543粉丝15.1万阅读

熊先泽医生的科普号
熊先泽 主任医师
四川大学华西医院
肝胆胰外科
1万粉丝2.8万阅读
-
 推荐热度5.0刘厚宝 主任医师上海中山医院 胆道外科
推荐热度5.0刘厚宝 主任医师上海中山医院 胆道外科胆管癌 72票
胆囊癌 43票
胆结石 21票
擅长:擅长胆囊癌、肝门胆管癌、肝内外胆管癌、壶腹部癌等胆道肿瘤的诊治;胆囊结石、胆囊息肉、胆囊腺肌症、肝胆管结石、胆总管囊肿的微创手术;胆管损伤与狭窄的修复及胃肠道肿瘤手术等治疗 -

 推荐热度4.7章爱斌 主任医师浙江大学医学院附属第一医院 肝胆胰外科
推荐热度4.7章爱斌 主任医师浙江大学医学院附属第一医院 肝胆胰外科肝癌 422票
胆管癌 84票
胰腺癌 60票
擅长:1,早期肝癌的手术治疗,及中晚期肝癌以免疫治疗和分子靶向药物治疗为基础的系统治疗,为部分不可手术的病人创造手术机会。 2,胆管癌的手术治疗和系统治疗,提高胆管癌手术切除率,降低手术后复发率。 3,胰腺癌及壶腹部癌的手术治疗,以超低的胰漏发生率提高病人围手术期安全性。 4,肝胆良性疾病的手术治疗及微创手术治疗。 -
 推荐热度4.6李慧锴 副主任医师天津医科大学肿瘤医院 肝胆肿瘤科
推荐热度4.6李慧锴 副主任医师天津医科大学肿瘤医院 肝胆肿瘤科肝癌 277票
胆管癌 72票
胰腺癌 63票
擅长:擅长肝胆胰恶性肿瘤的外科及综合治疗,尤其擅长以外科治疗为主的中晚期肝癌、胆道恶性肿瘤的转化治疗、局部进展期胰腺癌的综合治疗。擅长肝段切除术、半肝切除术、肝三叶切除术、肝门部胆管癌根治术、胆囊癌根治术、胰十二指肠切除术及全胰切除术的手术及围术期处理。




