精选内容
-
病例分享 - 上皮样血管内皮瘤 第7例
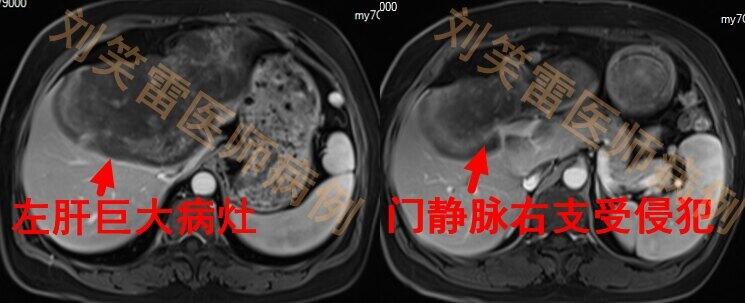
刘笑雷中日友好医院病史简介:患者女性,50岁,2021年7月因“胸部及上腹部疼痛”就诊于当地医院,行腹部核磁检查发现左肝部巨大肿瘤性病变,进一步行PET/CT等影像学检查,考虑肝内胆管细胞癌伴血管侵犯。行超声引导下穿刺活检,并经外院病理会诊,确诊为肝上皮样血管内皮瘤。患者肝内病灶为多发,最大一处病灶位于左半肝,最大径约16cm,并且侵犯大血管,手术无法切除,如下图:2021年8月患者就诊于我门诊,考虑到患者瘤体巨大,单药干扰素起效较慢,因此建议患者西罗莫司联合干扰素治疗。治疗3个月后复查,肝内病灶有缩小,治疗6个月时,肝内病灶显著缩小,最大径从16cm缩小至11cm,效果显著,如下图:由于患者除左肝最大病灶外,肝内还有多处小病灶,手术难以根治性切除,因此建议患者继续西罗莫司联合干扰素治疗,如下图:病例点评:该患者确诊后治疗方面并没有走弯路,而是直接选择了目前在肝脏上皮样血管内皮瘤方面最有效的两种药物。在之前的科普文章中,我详细介绍过两种药物治疗上皮样血管内皮瘤的临床结果及各自的优缺点,结合这个患者的情况,我再跟大家一起分析一下。西罗莫司治疗上皮样血管内皮瘤的临床研究是欧洲学者最先进行报道的,2016年他们首先报道了17例患者使用西罗莫司的结果,2021年再次报道了38例患者使用西罗莫司的结果。西罗莫司治疗上皮样血管内皮瘤的疾病控制率(疾病控制率指治疗期间肿瘤稳定或缩小的患者比例)较高(75.7%),但有效率较低(有效率指治疗期间肿瘤缩小的患者比例),仅为10%左右。由此可见大部分患者使用西罗莫司后,疾病仅能维持稳定,出现肿瘤缩小的患者较少。干扰素治疗上皮样血管内皮瘤的临床研究结果,是由我在2021年进行了报道,我们总结了42例患者使用干扰素后的治疗效果,其中疾病控制率81%,有效率52.4%,均好于西罗莫司。但在我们实际临床观察中发现,干扰素的起效较慢,对于一些病情严重的患者,治疗效果不好。因此对于一些病情较重或进展较快的患者,我都建议西罗莫司联合干扰素治疗。从目前的治疗情况看,该方案的治疗效果很可能优于单药西罗莫司或单药干扰素治疗,是疾病处于进展期患者的首选方案。
 刘笑雷医生的科普号
刘笑雷医生的科普号 2022年03月19日
2022年03月19日 1404
1404
 0
0
 12
12
-
病例分享 - 上皮样血管内皮瘤 第5例
刘笑雷 中日友好医院病史简介:患者男性,32岁。2016年1月体检发现肝内多发占位,2016年4月肝穿刺活检确诊上皮样血管内皮瘤。2016年4月行腹腔镜下肝多发病灶切除(共12处),手术前肝内病灶如下图:术后3个月复查时(2016年7月),发现肝内出现多个新发病灶如下图:患者选择观察病灶变化,未做任何治疗。2017年-2019年间,肝内病灶逐渐增大,如下图:2019年患者与我联系后,建议干扰素治疗。患者干扰素治疗6个月后肝内病灶出现明显缩小,如下图所示。患者目前身体情况良好,仍在干扰素治疗中。病例点评:上皮样血管内皮瘤的主要特点就是多发病灶、累及多个器官。绝大多数肝脏原发的上皮样血管内皮瘤诊断时,均是肝内多发病灶,单发病灶的患者非常少,而且常伴有肺转移、骨转移。但是病灶多或多器官转移,并不代表疾病很严重,这也是上皮样血管内皮瘤不同于其他恶性肿瘤的地方。我在临床上经常遇见肝、肺多发病灶的上皮样血管内皮瘤无任何症状,保持着正常的工作和生活状态。由于肝内多发病灶,导致手术很难根治性切除,而残留的病灶在手术后容易加速进展。从该患者的情况可以看出,即使切除了12个病灶,术后3个月即出现多个复发病灶,因此对大多数肝上皮样血管内皮瘤患者而言,手术切除并不适合。另外,从该患者观察期间的病灶变化也可以看出,上皮样血管内皮瘤是会进展的,文献报道的自行退缩或保持稳定的病例非常少,在我这里长期随访的100多名上皮样血管内皮瘤患者中,能自行退缩或保持不变的仅有2人。因此对于大多数上皮样血管内皮瘤患者而言,药物治疗需要尽早开始,除非是病灶非常小又暂时不适合药物治疗的患者。该患者在2019年就诊后,开始使用干扰素治疗,且治疗6个月后即出现病灶缩小,治疗效果非常好。但大多数患者干扰素治疗起效时间均在1年左右,目前与干扰素治疗效果相关的指标还不明确,需要通过进一步观察、总结和研究。
 刘笑雷医生的科普号
刘笑雷医生的科普号 2022年03月06日
2022年03月06日 1564
1564
 0
0
 13
13
-
病例分享 - 上皮样血管内皮瘤 第4例
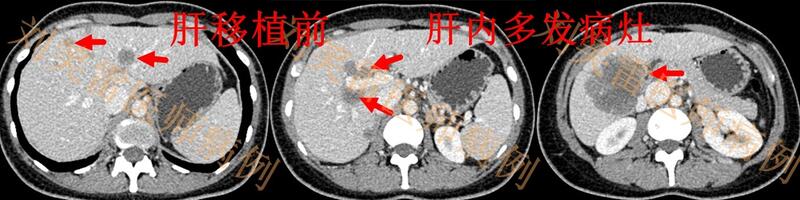
刘笑雷 中日友好医院病史简介:患者女性,30岁。2019年底常规体检发现肝脏占位,2020年1月经肝穿刺活检确诊上皮样血管内皮瘤,增强CT显示肝内多发病灶。2020年3月于外院行肝移植手术。移植前肝内病灶如下图:术后抗排异方案:普乐可复+吗替麦考酚酯,半年后更换为西罗莫司+吗替麦考酚酯。2020年4月至8月服用索拉非尼,预防肿瘤复发,服药期间因副作用大,剂量减半,但副作用仍难以接受。2020年9月改用仑伐替尼,服用至2021年9月停药。术后11个月复查时,肝内未见明显复发病灶,如下图2022年1月核磁共振显示肝内多发复发病灶,原移植医院建议二次肝移植。患者与我联系后,建议将西罗莫司加量,观察3个月,再决定是否联合干扰素治疗。肝内复发病灶如下图:病例点评:欧洲和美国分别有一项针对接受肝移植治疗的肝脏上皮样血管内皮瘤患者进行的回顾性研究,其报道的肝移植后远期效果较好。但该两项研究均缺乏患者术前的详细资料,对肝上皮样血管内皮瘤进行肝移植的手术时机和适合群体,并没有明确说明。在我多年来的临床观察中,所看到的接受肝脏移植的上皮样血管内皮瘤患者,其预后均不理想。肝上皮样血管内皮瘤生长部位多在肝表面,容易发生腹腔种植转移,这种情况在多名患者的腹腔镜探查手术中得到了证实。患者如果在病情的终末期极有可能合并腹腔种植转移,尤其是有大量腹水的患者,此时接受肝移植治疗,术后复发的概率很大。我遇见的多例患者均是这是这种情况,移植术后生存期不到1年。该例患者移植前病情不重,肝移植是可以考虑的治疗选项。但经过我们多年的研究,发现干扰素对肝上皮样血管内皮瘤的治疗效果较好,且远期生存率高于文献报道的肝移植的远期生存率。因此对于处在疾病早期阶段的肝上皮样血管内皮瘤患者,肝移植不太适合。从该患者的治疗结果同样可以看出,即使在疾病早期阶段接受肝移植,术后复发概率仍很大,再次移植的效果很可能依然不好。基于患者的特殊情况,我目前建议患者先加大西罗莫司的剂量,因为西罗莫司本身就是肝移植术后的常用抗排异药物,同时还兼具治疗上皮样血管内皮瘤的效果。对于是否联合干扰素,我目前还有顾虑。干扰素对移植肝是否有影响目前还没有直接经验,只是在文献中看到1例移植术后复发的患者,干扰素治疗后病灶好转。如果西罗莫司治疗效果不好,可以再考虑尝试西罗莫司联合干扰素的治疗方案,但需要密切监测移植肝的功能状态。
 刘笑雷医生的科普号
刘笑雷医生的科普号 2022年03月03日
2022年03月03日 1140
1140
 2
2
 12
12
-
病例分享 - 上皮样血管内皮瘤 第2例
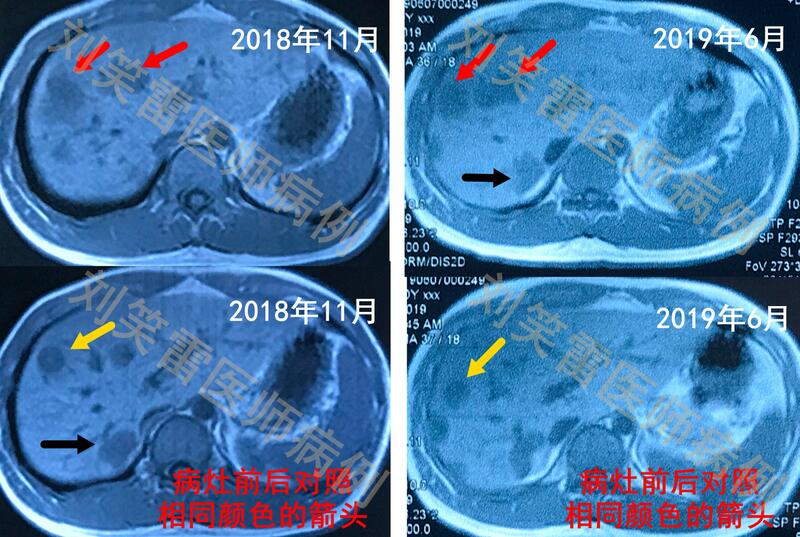
刘笑雷 中日友好医院 病史简介:患者男性,22岁,2018年9月体检时发现肝脏多发占位,无任何不适症状。于外院行PET/CT、增强核磁等检查,均考虑肝脏恶性肿瘤可能性大,同时发现腰椎转移灶。肝脏及腰椎病灶均行穿刺病理检查,确诊上皮样血管内皮瘤。2018年11月开始干扰素治疗,300万单位,隔日皮下注射。治疗早期有发热、疲乏等不适症状,2周后症状逐渐缓解。随访至2019年6月,肝内大部分病灶无明显变化,个别病灶略有增大,总体评价为病情稳定。如下图: 由于肿瘤评价为稳定,继续选择干扰素治疗,观察至2020年10月,复查核磁提示肝内病灶有缩小。继续使用干扰素治疗,观察至2021年11月,肝内病灶明显缩小,部分病灶消失。患者目前仍在干扰素治疗中,累计干扰素治疗时间已超过3年,除早期使用干扰素时出现发热症状,后期无明显不良反应,目前身体状态良好,日常生活、工作均正常。如下图: 病例点评:该患者比较幸运,确诊上皮样血管内皮瘤后,在治疗方面并没有走弯路,直接选择了干扰素治疗。干扰素的主要作用机制是通过激活自身免疫系统,通过自身的免疫细胞去攻击肿瘤细胞,而不是直接作用于肿瘤细胞,因此从治疗机制上考虑,应该不存在耐药情况(个人推测,仍需要基础实验及临床观察的验证)。经过多年的临床观察和总结,我发现干扰素治疗上皮样血管内皮瘤有一些特殊的地方,很多患者干扰素治疗早期病灶无明显缩小,甚至有少许增大,而随着治疗时间的延长,逐渐起效、病灶开始缩小。通过病例总结,干扰素起效的时间一般都在治疗1年以后。该患者的治疗情况也符合这种规律,干扰素治疗7个月时,肝内病灶无明显缩小,个别病灶还略有增大。由于当时(2019年)关于西罗莫司的最新研究结果尚未报道,而且患者总体治疗效果评价是肿瘤稳定,因此建议患者继续使用干扰素治疗。而在随后的随访观察中,发现干扰素逐渐发挥了作用,病灶开始缩小,有些病灶消失。患者目前干扰素使用时间已超过3年,无明显的不良反应,也验证了干扰素长期使用的安全性。
 刘笑雷医生的科普号
刘笑雷医生的科普号 2022年02月13日
2022年02月13日 1188
1188
 0
0
 12
12
-
病例分享 - 上皮样血管内皮瘤 第1例
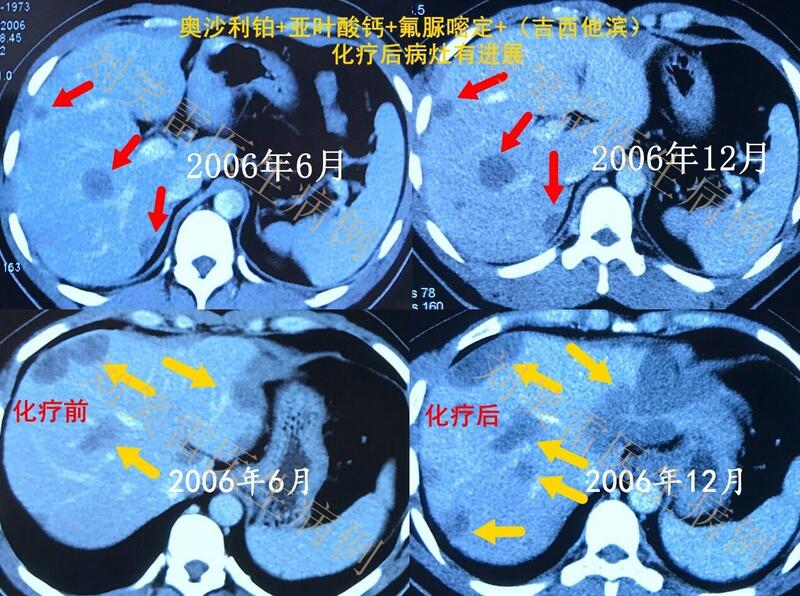
刘笑雷中日友好医院病史简介:患者男性,33岁,因“反复有上腹疼痛1年”于2006年6月行B超、CT、MRI检查发现肝内多发占位,PET/CT提示:肝内多发结节性高代谢病灶,考虑肝脏多发性转移病灶;双肺内多个小软组织结节,未见浓集影,考虑为双肺多发转移灶。2006年6-7月行超声引导下肝穿刺2次,病理检查未能明确诊断。2006年8-9月于外院按肝脏转移癌进行化疗(奥沙利铂+氟脲嘧定+亚叶酸钙+吉西他滨)。化疗无效,化疗后肝内病灶有进展,见下面两图,均为化疗前后腹部增强CT对照:2007年1月将2次肝穿活检玻片送病理会诊,确诊为“肝上皮样血管内皮瘤”。2007年10月、11月共在外院行介入栓塞治疗,具体方案为:肝动脉介入碘油栓塞+平阳霉素。介入治疗无效,介入治疗后可见肝内病灶持续增大,可见下图分析:2009年3月开始使用干扰素a治疗,300万单位,隔日注射。干扰素治疗后,肝内病灶明显缩小、消失,效果明显,可见下图分析:2011年-2018年,经干扰素治疗后,肝内病灶已基本消失,此段时间以规律复查为主,肝内无明显复发病灶,见下图:病例点评:在该患者确诊上皮样血管内皮瘤的时代,国内外医学界对该病都明显缺乏认识,国外主要的治疗经验都来源于肝移植病例的总结。而在药物治疗领域,国外只有单个病例的治疗报道,且报道的疗效都不够理想,那时尚无大规模的临床研究。从该患者的治疗经过可以看出,对于肝脏上皮样血管内皮瘤,按照消化道系统恶性肿瘤进行化疗效果很差,化疗期间肿瘤明显进展。而按照肝癌进行介入治疗,也同样没有效果,介入后肿瘤明显增大。患者偶然的治疗选择,采用了干扰素a治疗,临床效果非常好,经过2年左右的治疗,曾经肝内多发的大大小小病灶全部消失。由于该病极其罕见,该患者的治疗经历,也为后面所接诊的上皮样血管内皮瘤患者提供了极其宝贵的参考经验。该患者从2006年诊断上皮样血管内皮瘤,至今已有16年的时间,随访至2021年,肝内病灶无复发,达到了临床治愈的效果,结果非常让人欣慰。
 刘笑雷医生的科普号
刘笑雷医生的科普号 2022年02月07日
2022年02月07日 1916
1916
 2
2
 22
22
-
第八期:上皮样血管内皮瘤 – “捉摸不定”的靶向药物
刘笑雷 中日友好医院 普外科上皮样血管内皮瘤来源于血管内皮,既往多项研究显示肿瘤组织内可能出现血管内皮生长因子(vascular endothelial growth factor ,VEGF)的高表
刘笑雷医生的科普号 2021年08月24日
2021年08月24日 4736
4736
 2
2
 20
20
-
第七期:肝上皮样血管内皮瘤 – 介入栓塞并不适合
刘笑雷 中日友好医院 普外科肝脏介入栓塞治疗是采用在不开刀暴露病灶的情况下,在血管、皮肤上作直径几毫米的微小通道,或经人体原有的管道,在影像设备(血管造影机、透视机)的引导下对病灶局部进行治疗的创伤较小的治疗方法。目前主要用来治疗肝癌,因为肝癌大多是肝动脉供血,而介入栓塞可以通过堵塞肿瘤血管,导致肿瘤缺血坏死,同时还可以注入化疗药物,进行局部灌注化疗,从而使肿瘤缩小或延缓其进展。在肝癌治疗领域,介入栓塞的效果已得到充分的肯定。肝脏上皮样血管内皮瘤与肝癌不同,介入栓塞治疗并不适合,因为从肿瘤生长机制和对化疗的反应上,两者有本质区别。首先,与肝癌组织不同,肝脏上皮样血管内皮瘤并不是由肝动脉供血,而是一种缺乏血供的肿瘤,进行肝动脉系统的栓塞并不能阻止肿瘤的生长;其次,在第三期文章中我已详细讲述过,细胞毒性化疗药物对上皮样血管内皮瘤无任何作用,只会增加副作用,导致病人的免疫力降低。我们在临床上看到的曾接收过介入栓塞治疗的上皮样血管内皮瘤患者,没有一例有效果,而且在介入治疗后肿瘤出现了进展。同时在检索文献时,也没有介入栓塞可以有效治疗肝脏上皮样血管内皮瘤的文献报道。图示:一名肝脏上皮样血管内皮瘤患者,介入治疗后碘化油并未沉积在病灶内(黄色箭头),且介入治疗后短期内出现新发病灶(红色箭头)为什么介入栓塞治疗没有效果,还会有这么多患者被建议进行介入治疗呢?主要原因是上皮样血管内皮瘤是一种极其罕见的肿瘤,大多数医生对它缺乏认识,因此只能借用从其他类型肿瘤治疗中获取的经验,其结果必定是不理想的。这一期的内容本来并没有在计划中,但因为在临床中还是看到许多患者接收了介入治疗或正在考虑要不要做介入治疗,所以才写了这篇文章。到这一期为止,关于上皮样血管内皮瘤的治疗方面,我已经为大家总结了很多内容,在此我想提醒各位病友的是:对于上皮样血管内皮瘤这个病,“知道不能做什么,比知道需要做什么更重要”。我在临床上见到的疾病进展加速的患者,大部分都是在接收了不适合的治疗后出现的。由于该病罕见,大部分医生缺乏经验,且目前没有同一规范,因此更容易出现“五花八门”的治疗建议。我建议各位病友,治疗上首先要选择有临床证据的方法,哪怕是某一治疗方法的十几例患者治疗经验。在已有临床证据的方法尝试过无效后,再考虑尝试其他未经临床证实的治疗方法或药物。(由于介入栓塞并无治疗有效的文献报道,本期文章无参考文献)
刘笑雷医生的科普号 2021年08月17日
2021年08月17日 1880
1880
 4
4
 21
21
-
第六期:上皮样血管内皮瘤 – 干扰素-a的治疗价值
刘笑雷 中日友好医院 普外科干扰素-a是机体免疫细胞产生的一种细胞因子,是机体受到病毒感染时,免疫细胞通过抗病毒应答反应而产生的一组结构类似、功能接近的低分子糖蛋白。干扰素在机体的免疫系统中起着非常重要的作用。干扰素有很多亚型,其中最大的一类亚型是干扰素-a。干扰素-α具有三个功能:广谱抗病毒作用、免疫调节作用、抗肿瘤作用。干扰素-a作为一种免疫疗法已被用于治疗血液系统恶性肿瘤,同时干扰素-a也被报道可用于上皮样血管内皮瘤的治疗,可以减缓肿瘤进展或预防肿瘤复发、转移,另有报道干扰素-a可以用于治疗肝移植后转移性上皮样血管内皮瘤。干扰素-a还可以激活免疫细胞、抑制血管形成和诱导细胞因子从而抑制癌细胞生长。但关于干扰素-a治疗上皮样血管内皮瘤的既往文献报道中,大部分为个案报道或病例数较少的临床研究。图示:1名36岁男性肝脏上皮样血管内皮瘤患者,干扰素-a治疗18个月后,肝内部分病灶缩小、消失在对该病进行研究的早期阶段,我们通过对50名肝脏上皮样血管内皮瘤患者进行回顾性研究发现,在接受干扰素-a治疗的6名患者中,4名患者出现肿瘤缩小,1名患者肿瘤完全消失,1名患者肿瘤保持稳定,显示出良好的治疗效果。随后,我们开始对肝脏上皮样血管内皮瘤患者推荐使用干扰素-a,并进行定期随访。截至2021年4月,共有 42 名病情处于进展期肝脏上皮样血管内皮瘤患者接受了干扰素-a的治疗。我们在随访研究中发现,其中22名患者经过干扰素-a治疗肿瘤出现缩小或完全消失,客观缓解率达52.4%,12名患者干扰素-a治疗期间肿瘤保持稳定,总体疾病控制率为81.0%。根据我们所了解的情况,这是迄今为止文献报道的对肝脏上皮样血管内皮瘤患者最有效的治疗药物。此外,既往文献报道的肝移植治疗后患者5年生存率为70-83%,本研究中肝脏上皮样血管内皮瘤患者的 5 年生存率超过90%。同时,在本研究中干扰素-a长期治疗的安全性得到了充分验证,本研究中干扰素-a的中位治疗时间为19 个月,未观察到严重副作用,大多数患者在治疗初期容易出现发热反应,但确实有少数患者在干扰素-a治疗期间出现血小板减低、免疫性甲状腺炎等情况,需暂停干扰素治疗。干扰素-a治疗肝脏上皮样血管内皮瘤的具体机制尚不明确,我们分析干扰素-a并不直接作用于肿瘤细胞,而很可能是通过免疫调节来抑制肿瘤进展。临床上经常可以观察到,大部分治疗有效的患者,是在干扰素治疗6个月或1年后,才逐渐出现肿瘤缩小。因此,对于病情严重的患者,例如肿瘤负荷严重、瘤体大、合并腹水、腹痛严重等,并不适合干扰素-a的单药治疗,而应考虑联合其他药物同步治疗。对于其他部位的上皮样血管内皮瘤干扰素-a治疗是否有效,仍需进一步研究验证,目前尚无大样本临床研究结果。本文所述的研究内容,已整理成专业学术论文等待发表。 参考文献LiuXL (本文作者), et al. Outcomes of hepatic epithelioid hemangioendothelioma with different managements: a retrospective investigation. Eur Rev Med Pharmacol Sci. 2021;25(12):4274-4282.Galvao FHF, et al. Interferon alpha-2B and liver resection to treat multifocal hepatic epithelioid hemangioendothelioma: a relevant approach to avoid liver transplantation. Transplant Proc. 2005; 37: 4354-4358.Zhang L,et al. Interferon-alpha-based immunotherapies in the treatment of B cell-derived hematologicneoplasms in today's treat-to-target era. Exp Hematol Oncol. 2017; 6: 20.Calabrò L, et al. Primary hepatic epithelioid hemangioendothelioma progressively responsive to interferon-alpha: is there room for novel anti-angiogenetic treatments? J Exp Clin Cancer Res. 2007; 26: 145-150.Radzikowska E, et al. Pulmonary epithelioid haemangioendothelioma – interferon 2-alpha treatment – case report. Pneumonol Alergol Pol. 2008; 76: 281-285.Asmana NR. Human interferon alpha-2b: a therapeutic protein for cancer treatment. Scientifica (Cairo). 2014; 2014: 970315. Nadia Yousaf, et al. Systemic treatment options for epithelioid haemangioendothelioma: the Royal Marsden Hospital experience. Anticancer Res.2015 Jan;35(1):473-80.
刘笑雷医生的科普号 2021年08月10日
2021年08月10日 3463
3463
 7
7
 24
24
-
第四期:上皮样血管内皮瘤 - 手术、射频、移植
刘笑雷 中日友好医院 普外科手术切除是治疗上皮样血管内皮瘤的主要手段之一,文献报道肝脏上皮样血管内皮瘤患者手术切除后5年生存率超过70%。但大部分患者确诊后,并不适合手术治疗,因为确诊时已合并全身多部位转移。手术目的是为了完整切除所有肿瘤病灶,如果所有病灶无法完全切除,那手术治疗的结果会很差,可能会出现早期复发或疾病加速进展。我们在临床上见到多例肝脏上皮样血管内瘤患者(如下图1所示),手术后肿瘤复发或加速进展,我个人分析其原因可能为以下两点:1.肝内肿瘤多发,手术未能完全切除所有病灶,或是有些微小病灶术前影像(CT或核磁)未能发现,导致术中遗漏;2.肝脏手术后,肝细胞再生机制启动,其中部分参与肝脏再生的细胞因子(EGFR、VEGF等)对上皮样血管内皮瘤的生长具有促进作用。图1 1名女性肝脏上皮样血管内皮瘤患者,外科手术切除肝内病灶(白色箭头指示处为手术后遗迹),术后20个月发现肝内多发、较大新发病灶(红色箭头所示为肝内新发病灶)鉴于上皮样血管内皮瘤患者绝大多数在确诊时,已合并多发病灶、或多器官转移,最终能接受手术切除的患者仅占一小部分。文献报道的手术切除后效果虽然较好,但术前一定要对病情评估准确,确保所有病灶完全切除。如果接受了遗留部分病灶的“减瘤手术”而非“根治手术”,患者术后很容易复发,甚至出现病情的加速进展。射频消融作为微创的治疗手段,适合肝脏病灶较小的患者,对于5cm以下的病灶,其治疗效果与手术切除类似。对于上皮样血管内皮瘤而言,射频消融的治疗原则与手术切除相似,即一定在确保所有病灶可完全消融的情况下再进行。如果只消融了部分病灶,余下的病灶可能会出现加速进展的情况(如下图2所示)。我们在临床上曾见到多例患者在射频消融后出现疾病的快速进展,其主要原因与手术后复发相似:肿瘤残余与肝再生因子被激活的双重作用。而且由于肝内病灶特别容易在肝表面生长,射频消融的难度较大,因此对于大部分患者而言,射频消融并不合适,仅有少部分单发病灶或病灶数较少的患者可以尝试。图2 1名女性肝脏上皮样血管内皮瘤患者,射频消融后肝内病灶复发(红色箭头所示为肝内新发病灶)肝移植一直被作为治疗肝上皮样血管内皮瘤的根治性手段,尤其是对于肝内多发病灶无法手术切除的患者。文献报道的移植后5年生存率超过80%,提示移植治疗的效果较好。但在我们所进行的研究中,接受以干扰素为基础的综合治疗的患者,其5年生存率超过90%,好于文献报道的肝移植术后的数据。即使两者的结果相似,由于干扰素治疗费用低、无手术相关风险、不需要长期口服抗排异药物,其优势显而易见。还有一点需要注意,肝移植的手术时机如何选择?我们曾见到2例肝脏上皮样血管内皮瘤患者在疾病终末期接受肝移植手术,短期内复发,1年内死亡。虽然没有大样本的病例报道,但对于疾病已属终末期的患者(大量胸腹腔积液、广泛转移等),我们不建议肝移植治疗。而对于其他相对早期的患者,由于药物治疗上的进展,以及肝移植手术的高额费用和手术风险,肝移植对于上皮样血管内皮瘤的治疗价值在逐步下降。参考文献LiuXL (本文作者), et al. Outcomes of hepatic epithelioid hemangioendothelioma with different managements: a retrospective investigation. Eur Rev Med Pharmacol Sci. 2021;25(12):4274-4282.Nadia Yousaf, et al. Systemic treatment options for epithelioid haemangioendothelioma: the Royal Marsden Hospital experience. Anticancer Res.2015 Jan;35(1):473-80.Mohamad A Chahrour,et al. Treatment and Prognosis of Hepatic Epithelioid Hemangioendothelioma: A SEER Database Analysis. World J Surg.2021 May 17.doi: 10.1007/s00268-021-06165-6.Na BG, et al. Post-resection prognosis of patients with hepatic epithelioid hemangioendothelioma. Ann Surg Treat Res. 2021, 100(3): 137-143.Rodriguez JA, et al. Long-term outcome following liver transplantation for hepatic hemangioendothelioma: the UNOS experience from 1987 to 2005. J Gastrointest Surg. 2008; 12(1):110-6Quirino Lai,et al. Hepatic Epithelioid Hemangioendothelioma and Adult Liver Transplantation: Proposal for a Prognostic Score Based on the Analysis of the ELTR-ELITA Registry. Transplantation.2017 Mar;101(3):555-564.
刘笑雷医生的科普号 2021年07月26日
2021年07月26日 2083
2083
 6
6
 23
23
-
第三期:上皮样血管内皮瘤化疗是否有效?
刘笑雷 中日友好医院 普外科上皮样血管内皮瘤是一种相对惰性的肿瘤,大部分患者进展缓慢。根据既往的文献报道,不同部位的上皮样血管内皮瘤预后有一定差异,来源于软组织的上皮样血管内皮瘤预后相对更好,而肺部的上皮样血管内皮瘤预后相对较差,肝脏的介于两者之间。因此,在是否选择化疗的问题上,要结合患者的原发部位以及病情严重程度综合考虑。既往的文献报道显示,很多细胞毒性化疗药物如:阿霉素类、环磷酰胺、奥沙利铂、氟脲嘧定、紫杉醇、卡培他滨等,对于上皮样血管内皮瘤的治疗效果都非常不好。在接受上述化疗药物的患者中,大部分患者仍有疾病进展,或仅在短期内能保持病情稳定,极少患者会出现肿瘤的缩小。我们在实际工作中,也见到很多传统化疗方案无效的患者(如图1所示)。图1:肝脏上皮样血管内皮瘤患者接受化疗后(奥沙利铂+氟脲嘧定+亚叶酸钙)肝内病灶明显增大、增多同时由于化疗药物的毒副作用较大,化疗会导致患者身体虚弱、免疫力低下,患者反而容易出现肿瘤进展,导致患者预后变差。即使化疗期间病情稳定,由于患者副反应大,化疗很难长期维持,而停药后病情可能会加速进展。在提及上皮样血管内皮瘤采用化疗的文献报道中,很多患者接受化疗后的生存期不足1年。因此在目前缺乏客观临床依据的情况下(尚无任何大样本临床研究支持化疗),对于上述细胞毒性化疗药物,我们不建议作为上皮样血管内皮瘤患者的初始治疗方案,仅作为“一线”药物(如干扰素、西罗莫司、贝伐珠单抗及其他靶向药物)治疗无效时的最后尝试。由于上皮样血管内皮瘤来源于血管内皮细胞,因此很多医生推测血管内皮生长因子(vascular endothelial growth factor ,VEGF)在肿瘤进展中发挥重要作用,而贝伐珠单抗(bevacizumab)是一种重组人源化免疫球蛋白G1(IgG1)单克隆抗体,可以抑制VEGF的生物学作用,包括影响血管的渗透性、增生以及内皮细胞迁移与存活,达到抑制肿瘤血管生成、生长以及转移的效果。在一项针对上皮样血管内皮瘤及血管肉瘤的研究中,贝伐珠单抗治疗后17%的患者出现肿瘤缩小,50%的患者肿瘤保持稳定。另外有多个关于贝伐珠单抗治疗肺上皮样血管内皮瘤的病例报道,治疗后患者出现肿瘤缩小或保持稳定。因此,贝伐珠单抗在上皮样血管内皮瘤的治疗中具有很好的前景,但目前仍缺乏大规模的临床研究,多数文献仅为单个病例或数个病例的报道,临床证据尚不充足。由于上皮样血管内皮瘤患者的病情差异很大,不同部位的肿瘤预后也有差异,因此对于化疗的选择应结合患者具体情况来决定。从我们既往的经验考虑,肝脏上皮样血管内皮瘤对干扰素的治疗反应较好,目前应作为治疗的首选,而细胞毒性的化疗药物由于毒副作用大,且没有效果,已不再做为治疗上的选择。贝伐珠单抗可作为干扰素或西罗莫司治疗失败后的“二线”治疗方案。肺上皮样血管内皮瘤病情进展相对较快,对于部分病情严重的患者,可尝试包含贝伐珠单抗的化疗方案,或是作为干扰素、西罗莫司或其他靶向药物治疗失败后的“二线”治疗方案。(备注:由于上皮样血管内皮瘤尚无相关临床治疗指南,文中所提“一线”、“二线”治疗方案,仅代表作者个人观点。)参考文献Sumit Gaur,Alireza Torabi,Thomas J O'Neill. Activity of angiogenesis inhibitors in metastatic epithelioid hemangioendothelioma: a case report. Cancer Biol Med.2012 Jun;9(2):133-6.Tugba Akin Telli,Ilker Nihat Okten,Tuba Basoglu Tuylu,et al. VEGF-VEGFR pathway seems to be the best target in hepatic epithelioid hemangioendothelioma: A case series with review of the literature. Curr Probl Cancer.2020 Oct;44(5):100568.LiuXL (本文作者), et al. Outcomes of hepatic epithelioid hemangioendothelioma with different managements: a retrospective investigation. Eur Rev Med Pharmacol Sci. 2021;25(12):4274-4282.Bo Ye,Wang Li,Jian Feng,et al. Treatment of pulmonary epithelioid hemangioendothelioma with combination chemotherapy: Report of three cases and review of the literature Oncol Lett.2013 May;5(5):1491-1496.Young Hak Kim,Michiaki Mishima,Aya Miyagawa-Hayashino. Treatment of pulmonary epithelioid hemangioendothelioma with bevacizumab. J Thorac Oncol.2010 Jul;5(7):1107-8.Zaher Lakkis,Stefano Kim,Eric Delabrousse,et al. Metronomic cyclophosphamide: an alternative treatment for hepatic epithelioid hemangioendothelioma. J Hepatol.2013 Jun;58(6):1254-7.Min S Park,Vinod Ravi,Dejka M Araujo. Inhibiting the VEGF-VEGFR pathway in angiosarcoma, epithelioid hemangioendothelioma, and hemangiopericytoma/solitary fibrous tumor. Curr Opin Oncol.2010 Jul;22(4):351-5.Xiu-Qin Zhang,Heng Chen,Shu Song,et al. Effective combined therapy for pulmonary epithelioid hemangioendothelioma: A case report. World J Clin Cases.2020 May 26;8(10):2009-2015.Augustine Lau,Steve Malangone,Myke Green,et al. Combination capecitabine and bevacizumab in the treatment of metastatic hepatic epithelioid hemangioendothelioma. Ther Adv Med Oncol.2015 Jul;7(4):229-36.Ayako Mizota,Kohei Shitara,Takayuki Fukui. Bevacizumab chemotherapy for pulmonary epithelioid hemangioendothelioma with severe dyspnea. J Thorac Oncol.2011 Mar;6(3):651-2.M Agulnik,J L Yarber,S H Okuno,et al. An open-label, multicenter, phase II study of bevacizumab for the treatment of angiosarcoma and epithelioid hemangioendotheliomas. Ann Oncol.2013 Jan;24(1):257-63.
刘笑雷医生的科普号 2021年07月19日
2021年07月19日 2883
2883
 2
2
 17
17
相关科普号

刘斌医生的科普号
刘斌 副主任医师
广西医科大学附属肿瘤医院
骨软组织外科
1072粉丝49.8万阅读

许清泉医生的科普号
许清泉 主任医师
北京大学人民医院
泌尿外科
3466粉丝40.5万阅读

武志祥医生的科普号
武志祥 副主任医师
上海交通大学医学院附属新华医院
小儿外科
1498粉丝3.1万阅读
-
 推荐热度5.0刘笑雷 副主任医师中日医院 普外科·肝胆胰外科二部
推荐热度5.0刘笑雷 副主任医师中日医院 普外科·肝胆胰外科二部上皮样血管内皮瘤 41票
胆结石 15票
肝血管瘤 3票
擅长:血管内皮瘤 肝血管瘤 胆管癌 胆囊癌 胰腺癌 肝癌 -

 推荐热度3.8张晓伟 副主任医师复旦大学附属肿瘤医院 肿瘤内科
推荐热度3.8张晓伟 副主任医师复旦大学附属肿瘤医院 肿瘤内科软组织肿瘤 50票
化疗 30票
黑色素瘤 21票
擅长:实体肿瘤化疗和靶向,免疫等药物治疗,尤其软组织肉瘤,骨肉瘤,恶性黑色素瘤,皮肤肿瘤,胃癌,肠癌,食管癌,胰腺胆道肿瘤,原发不明多原发肿瘤,头颈鳞癌等常见肿瘤的诊治。 -
 推荐热度3.7朱继业 主任医师北京大学人民医院 肝胆外科
推荐热度3.7朱继业 主任医师北京大学人民医院 肝胆外科肝癌 8票
肝移植 2票
肝肿瘤 2票
擅长:肝癌、肝移植 胆道胰腺肿瘤




