科室介绍 查看全部
科室医生 查看全部
-
牙体牙髓科

王成坤
主任医师 副教授
4.1
牙体牙髓科
张志民
主任医师 教授
副院长
牙体牙髓科
李贺
主治医师
4.9
牙体牙髓科
李勋
主治医师
3.9
牙体牙髓科
高心
主任医师 教授
3.7
牙体牙髓科
张颖丽
主任医师 教授
3.6
牙体牙髓科
胡晓春
主任医师 教授
3.6
牙体牙髓科
孙淑芬
副主任医师 副教授
3.4
牙体牙髓科
洪伟
副主任医师 副教授
3.4
牙体牙髓科
刘玉艳
副主任医师 副教授
3.4
-
牙体牙髓科

王金蕊
副主任医师 副教授
3.4
牙体牙髓科
刘霞
副主任医师 讲师
3.3
牙体牙髓科
林闽
主治医师 讲师
3.3
牙体牙髓科
洪丽华
主治医师 讲师
3.3
牙体牙髓科
孟秀萍
主治医师 讲师
3.3
牙体牙髓科
任运佳
主治医师
3.3
牙体牙髓科
张红
主治医师
3.3
牙体牙髓科
王家凤
主治医师
3.3
牙体牙髓科
赵洪岩
主治医师
3.3
牙体牙髓科
高爽
主治医师
3.3
-
牙体牙髓科

郑鹏
医师
3.2
牙体牙髓科
李玉娇
医师
3.2
牙体牙髓科
刘莉
医师
3.2
牙体牙髓科
焦珊
医师
3.2
牙体牙髓科
李天博
医师
3.2
科普·直播义诊专区 查看全部
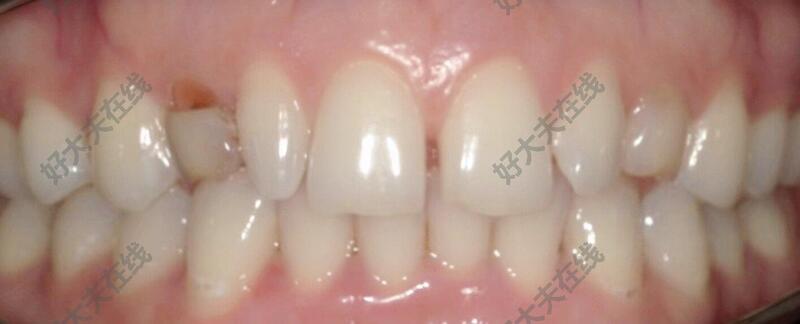
- 精选 牙齿缺损变色伴间隙
治疗前 患者因右上乳牙缺损变色伴上前牙间隙,牙齿形态不良来诊,当地给出方案需要拔除种植,患者寻求最佳治疗方案来诊 治疗后 治疗后即刻 患者非常满意,改变了患者牙齿美观问题,乳牙的一度松动问题以及牙齿外形整齐度等,告知3个月后需要二次抛光处理。整个过程历时50分钟,美学修复后,患者面容整体年轻度及美学效果大大提升,期待为更多前牙发育不良,期待变美的患者来诊。
 李贺 主治医师 吉林大学口腔医院 牙体牙髓病科59人已读
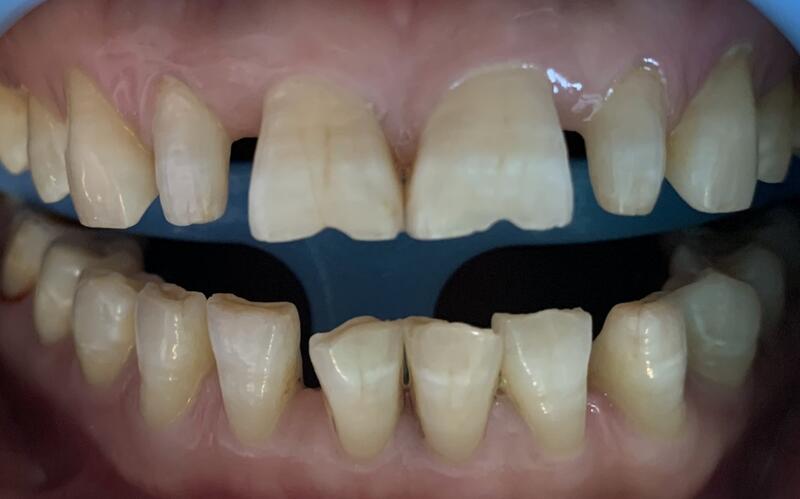
李贺 主治医师 吉林大学口腔医院 牙体牙髓病科59人已读 - 精选 最近又做了两例美学修复,解决患者多年困扰,很是欣慰
治疗前 治疗后 我想说的是,前牙微创树脂美学修复需要的更多的是医生的耐心与技巧,患者的配合与领悟,以及后续长期随访的决心,优点:不进行牙齿预备,保护天然牙齿,改变牙齿形态,可塑型及可重复性强,目前最为微创的美学修复方式。缺点:可能需要患者谨慎使用,避免前牙切割硬物,半年左右定期随访观察。目前近两年已进行数十例病例的随访,疗效很好,毕竟几个小时就轻松解决牙齿形态是件很有成就感的事情,所以希望帮助越来越多的患者解决美观问题。 一个小时,轻松中解决间隙问题,将左下前牙瓜子豁一并处理,患者很是满意
 李贺 主治医师 吉林大学口腔医院 牙体牙髓病科1418人已读
李贺 主治医师 吉林大学口腔医院 牙体牙髓病科1418人已读 - 载辛伐他汀微球缓释软膏促进牙槽骨缺损再生修复的实验研究
辛伐他汀是羟甲基戊二酸单酰辅酶A还原酶的抑制剂,是目前临床用于降低胆固醇、预防心血管疾病的常用药物。Mundy等首次报道他汀类药物能诱导成骨细胞和骨髓细胞中的骨形成蛋白2(Bone morphological protein2,BMP-2)基因的表达,说明其具有提高骨密度,促进成骨的作用。通过局部应用载辛伐他汀支架增加拔牙窝内TGF-β、BMP-2和VEGF信号分子的表达促进成骨,加速和提高新骨形成的速度与质量,可有效地防止拔牙后牙槽嵴的吸收【1】。另外观察发现,辛伐他汀对损伤造成的牙周组织吸收具有抑制作用并促进缺损组织再生【2】,说明辛伐他汀对牙周组织再生和重建具有积极作用。辛伐他汀口服给药经过肝脏首过代谢后,其生物利用度仅为2.4%,骨组织的吸收则更少;而大量应用辛伐他汀却会导致肌毒性和肝毒性等毒、副作用【3】,加重患者的痛苦和经济负担,因此,不能满足临床应用的要求 。载辛伐他汀支架材料【1】虽然可部分地提高辛伐他汀的生物利用度,降低毒、副作用,但该载辛伐他汀支架材料的缓释效果不是很理想,临床操作不方便,需要进一步改进剂型。本研究是将本实验室制备的载辛伐他汀缓释、控释微球(发明专利号:ZL200810050306.2)与适当赋形剂、防腐剂结合制成可注射性缓释软膏。以大鼠切牙拔牙窝为检测新骨形成的模型,将软膏注入拔牙窝,通过钼靶摄影测量和组织学观察来评价可注射性缓释辛伐他汀软膏促进牙槽骨缺损再生修复的效果。1材料和方法1.1可注射性软膏的合成 实验组(缓释软膏1):精确称取本实验室制备的载辛伐他汀缓、控释微球干燥粉末0.1g(含辛伐他汀0.01g),明胶0.2g,甘油1ml,去离子水2ml。室温下,超声混合均匀呈凝胶状,密封入注射器中。分别以辛伐他汀干燥粉末0.01g和PLGA空白微球粉末0.1g代替载辛伐他汀缓、控释微球干燥粉末,其余成分及工艺相同合成其他相应软膏(缓释软膏2和空白软膏)。所有的软膏经钴60照射消毒、灭菌,4℃保存、备用。1.2动物实验108只清洁级雄性Wistar大鼠(吉林大学实验动物中心),体重(180g±5g)。在22℃,40%湿度,12小时日光循环条件下,自由进食,饮水,标准饲料喂养。大鼠随机分为:①缓释软膏(1)组;②缓释软膏(2)组;③空白软膏组。每组36只。在0.3ml/kg的速眠新注射液(军事医学科学院长春军事兽医研究所)全麻下,拔除右下颌中切牙,实验组和对照组拔牙窝内分别注满相应的软膏,外敷以牙周塞治剂。术后禁食水2小时。喂饲软食2天,连续3天给予氨苄青霉素钠(60mg/kg)。于术后1,2,5,8,11,14周各组分别随机取6只动物,速眠新(0.3ml/kg)麻醉后,采用4%多聚甲醛通过MINI型灌流泵进行恒速灌流固定。固定完全后,分离下颌骨置于4%多聚甲醛内加强固定24小时。1.3 下颌骨标本的钼靶摄影应用钼靶摄影机 (Sitto,IMS公司)对去除软组织的下颌骨标本进行摄影,投照参数为29kv,8-11mAs ,照片通过扫描仪EPSON3490扫描(参数设置:48位全彩,1200dpi),保存图像以备分析。应用图像分析软件IPP6.0(Media Cybermetics,美国)对各组图像的切牙拔牙窝范围的灰度值进行对比分析,评价拔牙窝内骨密度改变的情况。1.4 组织学观察下颌骨标本放入10%EDTA溶液中脱钙,垂直于下颌骨长轴切取从下颌第一磨牙近中邻面至其远中3mm处的连同部分下颌第一磨牙的颌骨组织块,常规脱水、浸蜡、包埋、切片,厚5μm,HE染色,光镜观察。1.5 统计学分析应用统计分析软件SPSS13.0对测定数据进行t检验,以P<0.0 5为差异具有统计学意义。2结果2.1 载辛伐他汀缓释、控释微球干燥粉末(图1)与赋形剂、防腐剂加工合成后成为均匀、稳定的凝胶体,室温放置无沉淀(图2)。该凝胶在37℃下具有一定的流动性,可经由注射器软针头将软膏充分注射到所需部位,操作方便。2.2 动物术后安静,在笼中可自由活动。拔牙窝周围牙龈、粘膜无红肿等异常表现。术后2天可正常进食水, 5天可见拔牙窝表面牙周敷料脱落,完全为上皮组织覆盖。2.3 每个下颌骨标本的钼靶摄影照片经IPP6.0软件分析的结果如图3所示。术后1周,实验组和空白组拔牙窝骨密度接近,未见明显的差别(P>0.05);2周和5周,缓释软膏(2)组的骨密度明显高于缓释软膏(1)组和空白组(P<0.05);5周后,缓释软膏(2)组的骨密度随时间的增加而逐渐降低,空白组从术后1周至14周,骨密度经历先降低后逐渐增加的过程;而缓释软膏(1)组在整个实验周期内的骨密度均较接近,除第2周外,其余时间点间无明显差异(P>0.05)。2.4组织学观察组织学观察发现,随时间的延长,拔牙窝内新生骨小梁的宽度及密度逐渐增加,可见骨改建表现。术后1周,各组间无明显差别,拔牙窝内有炎性细胞浸润。术后2周,缓释软膏(2)组可见较稀疏的编织骨,周围可见成骨细胞;缓释软膏(1)组拔牙窝骨壁邻近区域有少量新骨形成;空白软膏组有少量新骨形成伴有炎性细胞浸润。术后5周,缓释软膏(2)组牙槽窝内可见较密集新生骨;缓释软膏(1)组牙槽窝内可见新生骨增加,并有骨岛形成;而空白软膏组形成的新骨较少且分散,仅限于牙槽窝骨壁附近,伴有炎性细胞浸润。术后8周,缓释软膏(1)组可见致密的编织骨,缓释软膏(2)组牙槽窝内可见新生骨,但较稀疏;空白软膏组周围有较多稀疏的新骨形成。术后11周,缓释软膏(1)、(2)组拔牙窝内均被新生的编织骨代替,但缓释软膏(1)组较(2)组新生骨表面骨沉积线明显,骨小梁更致密。术后14周,缓释软膏(1)组较(2)组新生骨沉积线明显,骨小梁致密,数量多。空白软膏组牙槽窝周边有较多骨小梁形成,牙槽窝内骨小梁较稀疏讨论自体骨移植修复骨组织缺损常导致继发损伤,而且塑形性较差,限制了广泛应用,特别是在较大的骨组织缺损情形下。羟基磷灰石和磷酸三钙植入骨缺损区,缺乏骨诱导性,降解速率与骨形成速率不协调,其应用效果也不理想。PLGA等可生物降解材料降解速率和物理性能可控,但只依靠骨传导成骨,骨形成作用有限。应用骨髓间充质干细胞、转基因技术及骨组织工程【4】等技术治疗骨缺损方面的研究是目前研究的热点之一,但因生物安全性、操作复杂及造价昂贵而不被患者广泛接受。因此,方便、安全、经济、实用的骨组织缺损修复、治疗技术将具有广阔的应用前景。他汀类药物在临床上被广泛应用于降低胆固醇,治疗高脂血症和动脉硬化。体内、外研究发现他汀类药物具有激活成骨细胞、促进骨形成的作用【5,6】。本研究利用实验室前期制备的载辛伐他汀缓释微球为功能成份、配制操作方便的可注射性软膏,应用于大鼠切牙拔牙窝,通过牙槽窝愈合过程中的新骨形成情况来评价载辛伐他汀缓释软膏的成骨效应。通过调节温度,可注射性软膏具有一定的流动性,可经由注射器将软膏充分注满拔牙窝;软膏又具有一定的稳定性,在缺损区可保持一定时间以充分发挥促进成骨的作用。本研究所应用的载体材料及赋形剂等可逐渐降解成羟基乙酸和丙酸,进入三羧酸循环, 最终以CO2和H2O的形式排出体外【7】不影响骨代谢,而且可为新形成的骨组织继续生长提供空间。拔牙窝的愈合过程中主要表现为血凝块的机化,成骨细胞分化、成熟,骨基质的分泌、矿化,类似于骨组织缺损的修复过程。本研究利用大鼠切牙拔牙窝的骨愈合过程评价合成软膏的成骨效应。由于大鼠等小动物的骨组织密度较低,利用对少量矿化组织较敏感的钼靶射影能够更好地分辨细小的骨小梁等微观结构的变化,而且对照射的组织破坏较小,不影响后续的研究。拔牙窝的组织学特征变化的趋势与骨密度改变的情况相对应,术后1周各组间无明显的差别, 说明拔牙窝内的血凝块机化过程是拔牙窝愈合、骨组织修复的必要准备阶段。空白组牙槽窝的骨密度变化与拔牙窝的正常愈合过程类似,先有骨吸收、密度减低的阶段,后逐渐提高,说明骨形成增加。缓释软膏(2)组内的功能药物辛伐他汀仅需扩散和渗透经过明胶等环节,具有较弱的缓释效应,可较快速地发挥药效,牙槽窝内骨密度表现为先逐渐增强后又逐渐减弱,这可能与辛伐他汀初始浓度较大、成骨作用较强,后期随药物的代谢、消耗而减少,局部的药物浓度降低、成骨作用减弱有关。缓释软膏(1)组的功能成份--辛伐他汀需经扩散和渗透等环节释放出来,需要较缓释软膏(2)组更长的时间才能发挥药效,表现为2、5周的促进成骨作用低于缓释软膏(2)组,随着缓释软膏(2)组的辛伐他汀药物浓度降低,而缓释软膏(1)组的辛伐他汀始终以接近匀速地释放,促进成骨的优势逐渐显现出来,5周后牙槽窝的骨密度逐渐提高,新生的骨小梁逐渐增多、增宽。骨缺损修复过程中既有骨形成也有骨吸收【8,9】,在本研究中拔牙窝内新生骨小梁的宽度及密度随时间的延长、药物的作用及代谢而有增减说明骨缺损修复是包括骨形成和骨吸收的骨改建过程。空白组的炎症反应较其余组明显,说明辛伐他汀具有一定的抗炎作用【10】。如将缓释软膏(1)、(2)组合并(复合软膏)应用于拔牙窝,其促进成骨的效应是否更佳有待进一步研究。本实验室合成的可注射性缓释辛伐他汀软膏制备工艺简单,应用方便,通过缓慢释放功能药物,为新骨的形成提供诱导因子又能为新骨生长提供支架,兼具骨传导和骨诱导的双重作用,促进新骨形成;同时,辛伐他汀具有一定的抑菌作用。研究表明可注射性缓释辛伐他汀微球软膏可有效促进牙槽骨缺损的骨再生修复。参考文献1.吴哲,孙宏晨,刘树泰,等。聚乳酸-羟基乙酸-辛伐他汀对拔牙术后剩余牙槽嵴吸收影响的实验研究。 中华口腔医学杂志,2006,41(12):747-750.2.刘树泰,孙宏晨,臧光祥,等。Simvastatin抑制实验性牙周组织吸收的体内研究。实用口腔医学杂志, 2008,24(1):145-1473. Grigioni F, Carigi S, Potena L, et al. Long-Term Safety and effectiveness of statins for heart transplant recipients in routine clinical practice. Transplantation Proceedings.2006,38 (5 ):1507–15104. 杨耀武,毛天球,王磊,等。鸵鸟骨转化多相钙磷陶瓷用于组织工程支架修复颅骨缺损实验研究。北京口腔医学,2007,15(2):84-905.Copaja M, Venegas D, Aranguiz P,et al.Simvastatin disrupts cytoskeleton and decreases cardiac fibroblast adhesion, migration and viability.Toxicology 2012,294(1): 42–496.Hu H, Sung A, ZhaoG,et al. Simvastatin enhances bone morphogenetic protein receptor type II expression. Biochem and Biophy Res Comm. 2006,339 (1) :59–647.Zolnik BS, Burgess DJ. Effect of acidic pH on PLGA microsphere degradation and release. J Controlled Release 2007,122(3):338-3448. Henriksen K, Neutzsky-Wulff A V,Bonewald L F,et al. Local communication on and within bone controls bone remodeling. Bone .2009,44 (6) :1026–10339.Ong K L,Day J S,Kurtz S M,et al. Role of surgical position on interface stress and initial bone remodeling stimulus around Hip resurfacing arthroplasty. J Arthroplasty.2009, 24 (7):1137-114210.Djaldetti M, Salman H, BergmanM,et al. Effect of pravastatin, simvastatin and atorvastatin on the phagocytic activity of mouse peritoneal macrophages. Experimental and Molecular Pathology .2006,80 (2) :160 – 164
李祥伟 主任医师 中山大学附属第五医院 口腔科3793人已读
问诊记录 查看全部
- 门牙缝隙大,过小牙 门牙缝隙变大,不确定是否蛀牙,两颗过小牙 请问是否可以树脂修复门牙牙缝和过小牙,不想磨牙贴片烤瓷牙,门牙可能有蛀牙,大概费用是多少,谢谢医生总交流次数10已给处置建议
- 慢性根尖周炎 慢性根尖周炎 能保住牙吗总交流次数12已给处置建议
- 牙齿咬合有痛感 吃的硬质食品,上颚右侧后槽牙,咬合感觉牙龈不适,感觉有痛感两... 是什么原因,需要用什么药缓解总交流次数2已给处置建议
- 大牙掉了一半,里面应该漏神经了,孕17周 牙疼,里面大牙掉了一半,应该是漏神经了,时不时的疼,现在已经... 这种情况怎么处理?能取神经吗或者治疗吗?总交流次数11已给处置建议
- 牙齿发黄,龋齿 牙齿发黄,发黑,不知道应该怎么 大夫现在宝宝的牙齿应该怎么处理总交流次数13已给处置建议
总访问量 289,238次
在线服务患者 119位
科普文章 7篇



