科室介绍 查看全部
科室医生 查看全部
-
妇科肿瘤

邵淑丽
主任医师
科主任
妇科肿瘤
赵宏伟
副主任医师 副教授
3.4
妇科肿瘤
孙立新
主任医师
3.3
妇科肿瘤
武晓红
主任医师
3.3
妇科肿瘤
闫丽隽
主任医师
3.3
妇科肿瘤
魏丽军
主任医师
3.3
妇科肿瘤
赵瑞霞
主任医师
3.3
妇科肿瘤
王晓燕
主任医师
3.3
妇科肿瘤
程玉英
主任医师
3.3
妇科肿瘤
孟祥兰
主任医师
3.3
-
妇科肿瘤

赵旭晔
副主任医师
3.3
妇科肿瘤
郑曙民
主任医师
3.3
妇科肿瘤
韩海琼
主任医师
3.3
妇科肿瘤
武燕
副主任医师
3.2
妇科肿瘤
郭勇峰
副主任医师
3.2
妇科肿瘤
韩江
副主任医师
3.2
妇科肿瘤
耿海燕
医师
3.2
妇科肿瘤
张晓燕
医师
3.2
科普·直播义诊专区 查看全部
- 精选 宫颈癌诊治
?《中国癌症杂志》2021年第31卷第6期 474 欢迎关注本刊公众号 CHINAONCOLOGY 2021 Vol.31 No.6 ·指南与共识· 子宫颈癌诊断与治疗指南(2021年版) 中国抗癌协会妇科肿瘤专业委员会 [关键词] 子宫颈癌;诊断;治疗;指南 DOI: 10.19401/j.cnki.1007-3639.2021.06.06 中图分类号:R737.33?文献标志码:A?文章编号:1007-3639(2021)06-0474-16 ?子宫颈癌发病率居女性生殖系统恶性肿 瘤第2位,根据世界卫生组织(World Health Organization,WHO)的数据,全球每年有新增 病例53万,约25万女性因子宫颈癌死亡,其中发 展中国家女性因子宫颈癌死亡人数占全球女性因 子宫颈癌死亡人数的80%。在西方发达国家,由 于人乳头瘤病毒(human papilloma virus,HPV) 疫苗的使用和子宫颈癌筛查的普及,子宫颈癌发 病率缓慢下降;在中国,每年新增子宫颈癌病例 约14万,死亡病例约3.7万。 本指南适用于子宫颈鳞癌、腺癌、腺鳞癌及 子宫颈小细胞神经内分泌肿瘤(neuroendocrine carcinoma of the cervix,NECC)。其他特殊 病理学类型,如透明细胞癌、肉瘤等发病率低, 国际、国内尚未就诊断与治疗方法达成共识,因 此,本指南不包括这些少见病理学类型的诊治, 部分诊治可参照本指南。在临床实践中,根据医 院的设备、技术条件以及患者的病情,国际上推 荐采用最适合的符合指南的方法诊治患者。对于 病情复杂的子宫颈癌,临床医师应灵活应用指 南,不适用于本指南的情况下建议参考高级别循 证医学证据及研究结果,并鼓励参加临床试验。 1 分期 1.1 分期规则 子宫颈癌分期规则采用国际上统一使用 的国际妇产科联盟(International Federation of Gynecology and Obstetrics,FIGO)2018年分期 (表1)、TNM分期作为参考(表2)[1]。FIGO 2018年子宫颈癌分期与2009年分期相比,主要有 以下不同: 1 因存在取材和病理“伪影”误差,微小浸 润癌的分期不再考虑病变宽度。 2 IB期根据子宫颈病变的最大直径细分为 IB1、IB2和IB3期。 3 由于淋巴结受累其预后更差,所有伴淋 巴结转移的病例归为IIIC期,若仅有盆腔淋巴结 阳性,则为IIIC1期;若腹主动脉旁淋巴结也受 累,则为IIIC2期,分期规则还指出,添加符号标 明影像学评估为“r”,已获得病理学确诊的为 “p”。因此,FIGO 2018年子宫颈癌分期规则为 临床结合影像学及病理学诊断结果的分期。 分期需注意以下4点: 1 需2名及以上高年资医师共同查体明确 临床分期,有条件时最好在麻醉状态下行盆腔 检查。 2 分期有分歧时以分期较早的为准。 3 允许影像学和病理学检查结果用于分期。 4 微小浸润癌诊断必须根据子宫颈锥切标本 由有经验的病理科医师作出诊断。 1.2 分期前检查 子宫颈癌治疗前分期很重要,应全面检查评 估患者的病情及身体状态,避免遗漏转移病灶, 以下检查应作为常规检查: 1 子宫颈活检。镜下浸润必要时行子宫颈锥 切及子宫颈管搔刮术以明确组织病理学诊断及病 变范围。 2 妇科检查仍然是临床分期的主要依据。 3 分期为IIB期以上或有相关的临床症状或 必要时,需行肾图、膀胱镜、肠镜检查。 4 血清鳞状上皮细胞癌抗原(squamous cell 《中国癌症杂志》2021年第31卷第6期 carcinoma antigen,SCCA)(对子宫颈鳞癌)、 糖类抗原125(carbohydrate antigen 125,CA125) (对子宫颈腺癌)检查。 5 胸CT、盆腔及上下腹(含腹主动脉旁) 平扫+增强MRI或CT,无条件者可行上下腹超 声检查和胸部CT,建议IB1期以上有条件者行 PET/CT检查。 6 子宫颈HPV定性或定量检测。 7 肿瘤相关基因检测可选择。 1.3 临床分期 遵照FIGO 2018年分期原则,子宫颈癌FIGO 临床分期见表1,TNM分期采用美国癌症联合会 (American Joint Committee on Cancer,AJCC) 第9版,具体见表2。 1.4 影像分期 FIGO 2018年分期把影像学检查结果纳入分 期,盆腔和(或)腹主动脉旁淋巴结受累,无论 肿瘤的大小与范围(采用r标记),IIIC1r表示只 有盆腔淋巴结转移,IIIC2r表示腹主动脉旁淋巴 结转移。对于IB3、IIA2~IVA期的子宫颈癌患 者,可采用影像学评估分期,根据影像学评估淋 475 巴结是否阳性决定下一步治疗方案。影像学提示 盆腔淋巴结阳性,腹主动脉旁淋巴结阴性,可选 择下列一种治疗方式:1 盆腔全量同步放化疗+ 后装腔内放射治疗±腹主动脉旁淋巴结放疗;2 腹主动脉旁淋巴结切除,建议术后影像学检查确 定淋巴结已充分切除,照射范围需根据临床和影 像学结果决定;3 病理学检查结果证实腹主动脉 旁淋巴结阳性,选择延伸野全量放化疗+后装腔 内放射治疗。影像学分期提示盆腔淋巴结阳性, 腹主动脉旁淋巴结阳性,直接选择延伸野全量放 化疗+后装腔内放射治疗。影像学分期盆腔及腹 主动脉旁淋巴结均阴性,可选择盆腔全量同步放 化疗+后装腔内放射治疗。 1.5 手术分期 对于IB3、IIA2~IVA期的子宫颈癌患者也 可以采用手术病理学分期,不论肿瘤的大小与范 围(采用p标记),IIIC1p表示只有盆腔淋巴结转 移,IIIC2p表示腹主动脉旁淋巴结转移。采用腹 主动脉旁淋巴结切除±盆腔淋巴结切除的手术分 期(2B级证据),淋巴结切除上界至肠系膜下动 脉水平,建议分期术后行影像学检查明确的淋巴 ??分期 I IA IAl IA2 IB IB1 IB2 IB3 II IIA IIA1 IIA2 IIB III IIIA IIIB IIIC IIIC1 IIIC2 IV IV1 IV2 表 1 子宫颈癌的临床分期(FIGO 2018年分期) 描述 癌症仅局限于子宫颈(扩散至子宫体者不予考虑) 显微镜下诊断的浸润癌,最大浸润深度≤5.0 mma 间质浸润深度≤3.0 mm 间质浸润深度>3.0 mm而≤5.0 mm 最大浸润深度>5.0 mm的浸润癌(大于IA期的范围);病变局限在子宫颈,病变大小为肿瘤最大直径b 间质浸润深度>5.0 mm而最大径线≤2.0 cm的浸润癌 最大径线>2.0 cm而≤4.0 cm的浸润癌 最大径线>4.0 cm的浸润癌 子宫颈癌侵犯至子宫外,但未扩散到阴道下1/3或骨盆壁 累及阴道上2/3,无子宫旁浸润 浸润癌最大径线≤4.0 cm 浸润癌最大径线>4.0 cm 子宫旁浸润,但未达骨盆壁 癌症累及阴道下1/3和(或)扩散到骨盆壁和(或)导致肾积水或无功能肾和(或)累及盆腔和(或)腹主动脉旁淋巴结 癌症累及阴道下1/3,未扩散到骨盆壁 扩散到骨盆壁和(或)肾积水或无功能肾(明确排除其他原因所致) 盆腔和(或)腹主动脉旁淋巴结受累(包括微小转移)c,不论肿瘤的大小与范围(采用r与p标注)d 只有盆腔淋巴结转移 腹主动脉旁淋巴结转移癌症已扩散超出真骨盆或已累及膀胱或直肠黏膜(活检证实)。出现泡状水肿不足以诊断为IV期 扩散至邻近的器官 转移至远处器官 ??a:所有的分期,都可以利用影像学和病理学检查结果来辅助临床所见而判定肿瘤的大小与浸润深度。病理学检查结果优于影像学与临床 判别。b: 脉管受累不改变分期。不再考虑病灶的横向范围;c:孤立的肿瘤细胞不改变分期,但需要记录下来d: r与p的加入是为了标注诊 断IIIC期的依据来源。例如:假如影像提示盆腔淋巴结转移,则分期为IIIC1r期,当病理学检查确诊后,就成为IIIC1p期。影像学的检查手 段、病理学诊断技术都应该记录下来。 476 中国抗癌协会妇科肿瘤专业委员会 子宫颈癌诊断与治疗指南(2021年版) ?原发肿瘤(T) 淋巴结转移(N) 远处转移(M) 表 2 AJCC(第9版)TNM分期 描述 原发肿瘤不能评估 原位癌 肿瘤局限于子宫颈 镜下可见浸润性癌,浸润深度≤5.0 mm 浸润深度≤3.0 mm 浸润深度>3.0 mm,但≤5.0 mm 临床可见的局限于子宫颈的肿瘤;或镜下可见超出T1a的范围(淋巴脉管侵犯不改变 分期,水平浸润宽度不再纳入分期) 肿瘤间质浸润>5.0 mm和肿瘤最大径≤2.0 cm 肿瘤最大径>2.0 cm,但≤4.0 cm 肿瘤最大径>4.0 cm 肿瘤侵犯超出子宫颈,但未达到盆壁或者阴道下1/3 肿瘤侵犯阴道上2/3,无子宫旁浸润 肿瘤最大径≤4.0 cm 肿瘤最大径>4.0 cm 有子宫旁浸润,但未达盆壁 肿瘤侵犯至盆壁,和(或)阴道下1/3,和(或)引起肾积水或无功能肾 肿瘤侵犯阴道下1/3,但未达到盆壁 肿瘤侵犯盆壁,和(或)引起肾积水或无功能肾 活检证实侵犯膀胱或直肠黏膜或肿瘤扩散至临近器官 (大疱性水肿病例不列为IVA期) 区域淋巴结中的孤立肿瘤细胞≤0.2 mm或单个淋巴结横截面中的单个肿瘤细胞 或肿瘤细胞簇≤200个 仅盆腔淋巴结转移 盆腔区域淋巴结转移(>0.2 mm,但最大径≤2.0 mm) 盆腔区域淋巴结转移(最大径>2.0 mm) 腹主动脉旁淋巴结转移,含或者不含盆腔淋巴结转移 腹主动脉旁区域淋巴结转移(>0.2 mm,但最大径≤2.0 mm),含或者不含 盆腔淋巴结转移 腹主动脉旁区域淋巴结转移(最大径>2.0 mm),含或者不含盆腔淋巴结转移 远处转移(包括腹股沟淋巴结转移、腹腔内病灶、肺、肝或骨转移;不包括 ?盆腔或主动脉旁淋巴结或阴道转移) 显微镜下证实远处转移(包括腹股沟淋巴结转移、腹腔内病灶、肺、肝或骨转移; ?不包括盆腔或主动脉旁淋巴结或阴道转移) ?TX Tis T1 T1a T1a1 T1a2 T1b T1b1 T1b2 T2 T2a T2a1 T2a2 T2b T3 T3a T3b T4 TX, T0, TX, T0, 任何T N0(i+) T1-T3 N1 N1mi N1a T1-T3 N2 N2mi N2a 任何N M1 cM1 pM1 ?结充分切除,具体照射范围需根据临床和影像学 表现决定:1 手术分期病理学检查提示淋巴结阴 性,采用盆腔全量放化疗+后装腔内放射治疗。 2 手术分期病理学检查提示盆腔淋巴结阳性,腹 主动脉旁淋巴结阴性(IIIC1p期),选择盆腔全 量放疗+后装腔内放射治疗+含铂药物同步化疗。 3 手术分期病理学检查提示腹主动脉旁淋巴结阳 性(IIIC2p期),需行全身检查排除远处转移, 若无远处转移选择延伸野全量放疗+后装腔内放 射治疗+含铂药物同步化疗;若存在远处转移, 选择系统性全身治疗及个体化治疗。 对于IB3、IIA2~IVA期的子宫颈癌患者影 像学分期提示盆腔淋巴结阳性,腹主动脉旁淋巴 结阴性,也可再次选择腹主动脉旁淋巴结切除手 术病理学分期,如果手术分期病理学检查提示腹 主动脉旁淋巴结阴性,采用盆腔全量放疗+后装 腔内放射治疗+铂类药物同步化疗;如果腹主动 脉旁淋巴结阳性,选择延伸野全量放疗+后装腔 内放射治疗+铂类药物同步化疗[2]。 《中国癌症杂志》2021年第31卷第6期 2 子宫颈癌病理类型 子宫颈癌的病理类型遵照妇科肿瘤WHO分类 (2020版)原则[3],具体见表3。 3 治疗 3.1 基本原则 子宫颈癌治疗方法主要有手术治疗和放疗, 化疗广泛应用于与手术、放疗配合的综合治疗和 晚期复发性子宫颈癌的治疗。目前靶向治疗、免 疫治疗及其联合治疗可用于复发或转移子宫颈 癌的全身系统性治疗。子宫颈癌综合治疗不是几 种方法的盲目叠加,而应有计划地分步骤实施, 治疗中根据手术结果和放疗后肿瘤消退情况予以 调整,原则上早期子宫颈癌以手术治疗为主,中 晚期子宫颈癌以放疗为主,化疗为辅。放疗适用 于各期子宫颈癌,外照射可采用前后对穿野、盆 腔四野、三维适形、调强放疗。适形放疗和调强 477 放疗已应用于临床,由于子宫颈癌后装腔内放疗 的剂量学特点,具有不可替代性。手术治疗适用 于分期为IA期、IB1、IB2、IIA1的患者, IB3期及IIA2期首选推荐同步放化疗,在放疗 资源缺乏地区可选择手术。对于未绝经的患者, 特别是年龄小于40岁的患者,放疗容易引起盆 腔纤维化和阴道萎缩狭窄,早于IIB期、无手术 禁忌证者可选择手术治疗。手术入路推荐开腹手 术或经阴道手术,对于IA1期无脉管侵犯患者 可选腔镜微创手术。目前化疗广泛适用于子宫 颈癌治疗,采用以铂类药物为基础的单药或联 合化疗,化疗中可联合贝伐珠单抗治疗。而对 于二线治疗,可以选用靶向治疗或免疫治疗, 例如,程序性死亡[蛋白]配体-1(programmed death ligand-1,PD-L1)阳性或微卫星高度不稳 定(microsatellite instability-high,MSI-H)/错配 ?表 3 子宫颈恶性肿瘤主要病理类型及分类原则(2020 WHO)[3] 病理类型及分类 鳞状上皮肿瘤(squamous epithelial tumours) 低级别鳞状上皮内病变(low-grade squamous intraepithelial lesion) 宫颈上皮内瘤变,1级(cervical intraepithelial neoplasia, grade 1) 高级别鳞状上皮内病变(high-grade squamous intraepithelial lesion) 宫颈上皮内瘤变,2级(cervical intraepithelial neoplasia, grade 2) 宫颈上皮内瘤变,3级(cervical intraepithelial neoplasia, grade 3) 鳞状细胞癌,HPV相关(squamous cell carcinoma, HPV-associated) 鳞状细胞癌,非HPV相关(squamous cell carcinoma, HPV-independent) 鳞状细胞癌,非特异性(squamous cell carcinoma, NOS) 腺体肿瘤及前驱病变(glandular tumours and precursors) 原位腺癌,非特异性(adenocarcinoma in situ, NOS) 原位腺癌,HPV相关(adenocarcinoma in situ, HPV-associated) 原位腺癌,非HPV相关(adenocarcinoma in situ, HPV-independent) 腺癌,非特异性(adenocarcinoma, NOS) 腺癌,HPV相关(adenocarcinoma, HPV-associated) 腺癌,非HPV相关,胃型(adenocarcinoma, HPV-independent, gastric type) 腺癌,非HPV相关,透明细胞型(adenocarcinoma, HPV-independent, clear cell type) 腺癌,非HPV相关,中肾管型(adenocarcinoma, HPV-independent, mesonephric type) 腺癌,非HPV相关,非特异性(adenocarcinoma, HPV-independent, NOS) 内膜样腺癌,非特异性(endometrioid adenocarcinoma, NOS) 癌肉瘤,非特异性(carcinosarcoma, NOS) 腺鳞癌(adenosquamous carcinoma) 黏液表皮样癌(mucoepidermoid carcinoma) 腺样基底细胞癌(adenoid basal carcinoma) 未分化癌,非特异性(carcinoma, undifferentiated, NOS) 混合性上皮-间叶肿瘤(mixed epithelial and mesenchymal tumours) 腺肉瘤(adenosarcoma) ??NOS: Non otherwise-specified 478 中国抗癌协会妇科肿瘤专业委员会 子宫颈癌诊断与治疗指南(2021年版) ?修复缺陷(deficient mismatch repair,dMMR)的 患者可选择程序性死亡[蛋白]-1(programmed death-1,PD-1)抑制剂(如派姆单抗)[4-6]。 NTRK基因融合阳性的患者可以选用拉罗曲替尼 或恩曲替尼。治疗方式的选择取决于本地区现有 的设备、妇科肿瘤医师的技术水平以及患者的一 般状况、年龄、愿望、肿瘤分期和肿瘤标志物检 测结果,治疗前应进行充分的医患沟通。 3.2 子宫颈癌的手术治疗 3.2.1 手术分型 子宫颈癌手术治疗方式包括保留生育功能 手术、不保留生育功能手术、盆腔廓清术和腹主 动脉±盆腔淋巴结切除分期手术。保留生育功能 手术包括子宫颈锥切术和经腹或经阴道根治性子 宫颈切除术。不保留生育功能手术采用Querleu- Morrow(QM)分型,包括筋膜外子宫切除术 (A型)、改良根治性子宫切除术(B型)、根 治性子宫切除术(C型)和超根治性子宫切除术 (D型)[7]。C型手术又分为保留膀胱神经(C1 型)和不保留膀胱神经(C2型)。根治性子宫 切除手术方式推荐开放性手术[8-9]。放疗后盆腔 中心性复发或病灶持续存在可选择盆腔廓清术, 包括前盆腔廓清术、后盆腔廓清术和全盆腔廓清 术。关于盆腔淋巴结的处理,可选择双侧盆腔淋 巴结切除或前哨淋巴结显影。QM分型见表4, Piver分型见表5。 表 4 Querleu-Morrow (QM)分型 ?QM分型 A型 B型 C型 C1型 C2型 D型 Piver分型 I型 II型 III型 IV型 V型 术式 ?有限的根治性子宫切除术,在输尿管和子宫颈之间切断侧方子宫旁组织,腹侧和背侧子宫旁组织贴近子宫切除,约切除 5 mm,切除阴道<10 mm。适用于:1 病灶<20 mm、盆腔淋巴结阴性、无深肌层侵犯、无脉管受侵的低危的IB1期子 宫颈癌;2 个别放化疗结束后的晚期子宫颈癌,改良式根治性子宫切除术,在输尿管隧道处切断侧方子宫旁组织,不 切除 下腹下神经,在子宫直肠反折腹膜处切除背侧子宫旁组织,切除部分腹侧子宫旁组织。在子宫颈或肿瘤下方10 mm处切除 阴道,也称 B1型手术;B2型手术是B1+子宫颈旁淋巴结切除 经典的根治性子宫切除术,于髂内血管内侧切除侧方子宫旁组织;近直肠水平切断骶韧带、近膀胱水平切断膀胱子宫颈 韧带、膀胱阴道韧带,完全游离输尿管,根据阴道受侵的范围调整阴道切除的长度。适用于深肌层受侵的IB1期、 IB2~II A 期或偏早的II B期子宫颈癌 保留神经的根治性子宫切除术,分离出背侧的自主神经后切除背侧子宫旁组织;暴露下腹下神经丛,在切除侧方子宫旁 ?组织时仅切除盆丛的子宫支;膀胱阴道韧带内的盆丛的膀胱支予以保留,故只切除腹侧子宫旁组织的内侧,暴露输尿管 ?下方的下腹神经,保留膀胱支 不保留自主神经的根治性子宫切除术,在直肠侧方切断下腹下神经丛、骶内脏神经;分离出尿管后,近膀胱壁处切除腹 ?侧子宫旁组织(膀胱阴道韧带),不保留下腹神经丛里的膀胱支;切除侧方子宫旁组织时沿着髂内血管的内侧至盆壁。 ?在骶骨水平切除背侧子宫旁组织。该型仅适用于因解剖原因不能保留盆腔自主神经者 侧盆扩大切除术,D1型近盆壁切除所有的子宫旁组织,包括下腹、闭孔血管。可适用于IIB 期子宫颈癌;D2型即盆腔脏器 廓清术(LEER术),范围包括D1+临近的筋膜/肌肉组织。适用于侧方复发的肿瘤 ??子宫动脉 子宫颈筋膜外侧 与输尿管交汇处结扎 髂内动脉起始部结扎 必要时于盆壁结扎髂 ?内动脉 结扎髂内动脉 表 5 Piver 分型 手术范围 主韧带 宫骶韧带 子宫颈筋膜外侧 子宫颈筋膜外侧 从中间切断 靠近子宫切断 全部切除 近骶骨处切断 全部切除 近骶骨处切断 全部切除 近骶骨处切断 阴道 子宫颈筋膜外侧 切除上1/3 切除上1/2 切除3/4 切除3/4 淋巴结 适应证 ??不切除 IA1期 选择性切除 IA2期 肿大的淋巴结 常规行盆腔 IB1期 淋巴结清扫术 常规行盆腔 淋巴结清扫术 常规行盆腔 淋巴结清扫术 中央型复发 中央型复发累及远 ?端输尿管或膀胱 ? 《中国癌症杂志》2021年第31卷第6期 3.2.2 前哨淋巴结显影 在早期病例中应用,可以避免系统的盆腔 淋巴结切除。肿瘤直径<2.0 cm时检测率和显影 效果最好[10-11]。前哨淋巴结显影推荐用于经选 择的I期子宫颈癌患者手术。具体操作为在子 宫颈3和9点或3、6、9、12点位置注射染料或放 射性胶体99mTc(图1)。注射染料采用直观观 察有色染料,注射99mTc采用γ探测器,吲哚菁绿 (indocyanine green,ICG)采用荧光摄像。病 理科医师对前哨淋巴结(sentinel lymph nodes, SLN)进行超分期可提高微小转移的检出率。 ICG能识别出比蓝色染料更多的SLN[12]。 图 1 子宫颈染料及标记注射点示意图 3.2.3 各期子宫颈癌手术治疗 详见3.5各期子宫颈癌的治疗选择建议。 3.3 子宫颈癌放疗 各期子宫颈癌都适合放疗,包括各种病理学 类型,患有内科疾病不能耐受手术的CIN III可以 选择单纯腔内放疗。但对于年轻的早期子宫颈癌 患者,考虑到对卵巢功能的保护,主要采用手术 治疗或卵巢移位以后的盆腔放疗。 3.3.1 一般性原则 子宫颈癌放疗包括远距离体外照射(体外 照射)和近距离放疗,两者针对的靶区不同,外 照射主要针对子宫颈癌原发灶和盆腔蔓延及淋巴 转移区域,近距离放疗主要照射子宫颈癌的原 发病灶区域。应有足够的剂量以保证疗效,与 此同时也需要最大限度地保护邻近正常组织, 提高患者生存质量。需要根据患者一般状况、 肿瘤范围以及治疗单位放疗设备条件、患者意 愿来选择放疗方式。体外放疗可选择前后二野 传统照射技术,或精确放疗技术如三维适形放 疗(three-dimensional conformal radiotherapy, 3D-CRT)、适型调强放疗(intensity-modulated radiotherapy,IMRT)、容积调强放疗 479 (volumetric modulated arc therapy,VMAT)、 螺旋断层放疗(TOMO)等。腔内照射可选择二 维、三维或四维技术。外照射不能取代后装治疗 在子宫颈癌根治性放疗中的作用。 子宫颈癌的放疗剂量根据分期不同而有所 差别。A点总剂量为盆腔体外照射联合后装治疗 换算后的总的生物等效剂量,对于早期(IA 期及病灶小于1.0 cm的IB1期)子宫颈局部肿 瘤小的患者,也可以单独接受后装腔内治疗, 特别是对外照射放疗(external beam radiation therapy,EBRT)有相对禁忌证者。A点常给予 60~65 Gy的等效剂量。EBRT与腔内近距离放疗 (intracavitary radiotherapy,ICRT)联合方案也 是这类患者的一种选择。局部肿瘤大或晚期患者 A点总剂量≥85 Gy[常规2 Gy分次放射的生物等 效剂量(equivalent dose in 2 Gy/f,EQD2)]。 治疗剂量应根据治疗过程中的患者症状、盆腔检 查及影像学检查等获得的肿瘤变化及时调整,采 用个体化放疗方案。根治性放疗应尽量在8周内 完成。无化疗禁忌患者,放疗过程中需要接受铂 类药物为基础的同步化疗。 3.3.2 体外照射 体外照射主要针对子宫颈癌原发灶和盆腔蔓 延及淋巴转移区域,要求在5~6周内完成,尽量 避免放疗时间延长。强调不能以任何体外照射方 式替代后装放疗。 3.3.2.1 体外照射靶区设定 子宫颈癌放疗靶区的设定应根据妇科检查 情况和影像学检查(如CT、MRI、PET/CT)确 认,应包括子宫、子宫颈、子宫旁和上1/3阴道 (或距阴道受侵最低点下2.0 cm,IIIA期患者包 括全部阴道)以及盆腔淋巴引流区,如闭孔、髂 内、髂外、髂总、骶前;如果腹股沟区淋巴结、 腹主动脉旁淋巴结转移,该区域也应包括在照射 野内。 3.3.2.2 照射野设定 采用X线模拟定位机或CT、MRI模拟定位机 定位。 (1) 盆腔等中心照射:包括下腹及盆腔, 设前后野等中心垂直照射。上界在L4~L5间 ?? 480 中国抗癌协会妇科肿瘤专业委员会 子宫颈癌诊断与治疗指南(2021年版) ?隙,下界在闭孔下缘或肿瘤下界以下至少 2.0 cm,侧界在真骨盆最宽处向外1.5~2.0 cm, 同时,应用铅块[有条件者用多叶光栅技 术(multi-leave collimators,MLC)]遮挡 正常器官。每次盆腔中平面处方剂量为1.8~ 2.0 Gy,每周4~5次。盆腔等中心照射可分两阶 段完成,第1阶段为全盆腔等中心照射,DT量为 20~30 Gy,2~3周完成;第2阶段建议行影像学复 查,可根据情况重新定位,中间遮挡照射,全盆 腔中间遮挡4.0 cm×(8.0~12.0)cm,以降低危及 器官膀胱和直肠的受量,给后装治疗提供剂量空 间,DT量为20~25 Gy(EQD2),2~3周完成。 (2) 四野箱式照射:即盆腔前后两野照射加 两个侧野照射,主要适用于特别肥胖的患者拟 增加子宫旁或淋巴引流区的剂量。上界在L4~L5 间隙,下界在闭孔下缘或肿瘤下界以下至少 2.0 cm,侧界在真骨盆最宽处向外1.5~2.0 cm。两 侧野前缘达耻骨联合(包括髂外淋巴引流区), 后缘在S2~S3骶椎交界水平(包括骶前淋巴引流 区),如子宫颈原发灶大,宫骶韧带受累,后缘 可达S3~S4骶椎水平,应用铅块或MLC技术遮挡 正常器官。每天四野同时照射,一般给予B点DT 量为45~50 Gy(EQD2),4~5周完成。 (3) 腹主动脉旁野(延伸野)照射:髂总或主 动脉旁淋巴结转移时需行延伸野照射,照射野的 宽度一般为6.0~8.0 cm,长度依据淋巴结转移的 范围予以个体化设计。建议DT量为40~45 Gy, 4~5周,每天1次,1.8~2.0 Gy,照射时要注意保 护肾脏和脊髓。对腹主动脉旁淋巴引流区的照 射,建议采用适形或调强精确放疗技术。 3.3.2.3 射线选择 根据采用的放疗技术、照射野数以及医疗 机构的设备、防护条件而选择射线。射线能量越 高,其穿透能力越强,需要的防护条件越高,前 后二野照射可选择 10~15 MV X射线,多野照射 可选择6~10 MV X射线。 3.3.2.4 精确放疗 精确放疗技术实施均基于靶区的精确定位, 包括靶区准确定义、针对治疗中靶区变化和器官 移动的应对、摆位及质量控制,其中合理的靶区 勾画是治疗成败的关键,也直接影响放疗并发症 的发生与否[13-15]。建议行MRI或PET/CT检查以 保证照射靶区覆盖受侵子宫旁及转移淋巴结组 织,同时最大限度地保护直肠、小肠、膀胱等危 及器官。子宫颈癌的靶区包括大体肿瘤区(gross tumor volume,GTV)、临床靶区(clinical target volume,CTV)和计划靶区(planning target volume,PTV)。 (1) GTV:指临床可见的肿瘤灶靶区,一般诊 断手段,如妇科检查、CT、MRI、PET/CT,能 够确定具有一定形状和大小的病变范围,包括原 发病灶、转移淋巴结和其他转移病灶。理论上, 子宫颈癌行广泛性子宫切除术+淋巴结切除术后 没有GTV。未行手术切除者,GTV应包括子宫颈 和受累的阴道、子宫体、子宫旁、转移淋巴结及 其他转移病灶。 (2) CTV:包括肿瘤临床靶区和亚临床靶区。 CTV主要包括盆腔原发肿瘤区和淋巴引流区,亚 临床灶靶区为肿瘤可能侵犯的范围。 盆腔原发肿瘤区对于未行子宫切除者包括 肿瘤、全子宫(子宫颈+子宫体)、部分阴道、 子宫旁或阴道旁软组织;对于已行子宫切除 者包括残存肿瘤、阴道残端、上段阴道(3.0~ 4.0 cm)、阴道旁或瘤床软组织。淋巴引流 区[16]包括闭孔、髂内、髂外、髂总±腹主动脉 旁淋巴结引流区。对于影像学诊断子宫颈间质 受侵的患者,应包括骶前淋巴引流区;如果髂总 淋巴结、腹主动脉旁淋巴结有转移则需行腹主动 脉旁淋巴引流区照射,其靶区上界要求达肾血管 水平;如果转移淋巴结超过肾血管水平,则根据 受侵淋巴结范围决定上界;肿瘤侵及阴道下1/3 时,靶区需包括全阴道及双腹股沟淋巴引流区。 需要特别指出的是,应建立考虑膀胱体积变化 的内靶区(internal target volume,ITV),若在 制订计划时发现直肠过度扩张,应考虑再次行 CT、MRI模拟定位。 (3) PTV:确定PTV的目的是确保临床靶区得 到规定的治疗剂量。PTV应包括CTV、照射中患 者器官运动和由于日常摆位、治疗中靶位置和靶 体积变化等因素引起的扩大照射范围。子宫颈癌 《中国癌症杂志》2021年第31卷第6期 体外照射由CTV外放一定距离形成PTV,目前没 有统一标准。 (4) 处方剂量:外照射处方剂量约45~ 50 Gy,对于转移淋巴结可采用同步加量照射 或后程加量,根据转移淋巴结大小,增加剂量 10~15 Gy,总剂量可达55~65 Gy。加量照射时需 要注意保护临近正常组织。 3.3.3 近距离放射治疗 近距离放射治疗主要照射子宫颈癌的原发区 域,在子宫颈癌治疗中占有重要地位。根据情况 选择传统二维后装或图像引导的三维后装治疗。 3.3.3.1 剂量率 根据后装治疗时放射源对A点剂量的贡献速 率分为低剂量率(low dose rate,LDR)、中剂量 率(middle dose rate,MDR)和高剂量率(high dose rate,HDR)。目前,国内多使用HDR后装 治疗机。A点剂量以传统剂量分割及LDR近距离 治疗为依据。对于近距离放疗,设定为一个4~ 7 Gy/h的LDR。应用HDR近距离放疗应当依据线 性二次方程定义HDR的A点剂量,即转化成生物 等效LDR的A点剂量。如30 Gy的HDR的A点剂 量被分割为5次照射,等同于采用LDR的A点的 40 Gy剂量(剂量率换算参考第4版《肿瘤放射治 疗学》)。 3.3.3.2 腔内放疗剂量 应与体外照射剂量统筹考虑,一般给予A 点剂量20~42 Gy,体外联合腔内放疗总剂量 (EQD2)大于75 Gy,每次5~7 Gy,每周1次, 腔内后装治疗当天不进行体外照射。体外照射 联合腔内治疗A点的EQD2因期别而异,IA2 期应达到75~80 Gy(EQD2),IB1、IB2和 IIA1期达到80~85 Gy,IB3、IIA2和IIB~IVA 期≥85 Gy(EQD2),采用不同剂量率后装 机治疗时,应进行生物剂量转换(腔内剂量以 体外常规分割等效生物剂量换算),同时注意 对膀胱及直肠剂量的监测,避免膀胱及直肠 的过高受量。正常组织的限定剂量为:直肠 2 cc≤65~75 Gy;乙状结肠2 cc≤70~75 Gy;膀胱 2 cc≤80~90 Gy。 3.3.3.3 后装治疗时机 通常在外照射开始后,子宫颈口便于暴露时 481 进行,在子宫颈条件允许原则下应尽早进行,最 好与体外照射同步进行,以缩短总放疗时间。最 常用的传统二维后装治疗采用剂量参数系统包括 A、B点及膀胱和直肠点的剂量。 3.3.3.4 三维后装治疗 子宫颈癌近距离治疗中采用图像引导的三维 治疗计划有明显优势,可以提高局控率、肿瘤特 异性生存率和总生存率。采用CT或MRI进行定 位,扫描范围从髂前上嵴(或子宫底上3.0 cm) 至坐骨结节下缘,层厚3 mm。对于无法行MRI定 位的单位,可进行CT扫描定位,但需要参照定 位前MRI扫描图像。 靶区、危及器官(organ at risk,OAR) 勾画,参考ICRU89号文件:以MRI-T2加权像 上的高信号及灰色信号加上妇科查体病灶确 定为GTV。CTV分3类:肿瘤高危临床靶区 (CTV-THR),包括整个子宫颈和后装治疗时 残留的可见肿瘤及查体和MRI确定的残留病 变组织。肿瘤中危临床靶区(CTV-TIR),包 括GTV-Tinit的范围映射在近距离治疗时影像上 的区域,及CTV-THR基础上外扩的总和。肿 瘤低危临床靶区(CTV-TLR)代表来自原发肿 瘤潜在的连续或非连续的具有临床下病灶扩 散的危险区域。建议以D90、D100评估CTV-THR 和CTV-TIR的剂量,以V150、V200评估高剂量 体积;以D1cc、D2cc评估OAR的耐受剂量。 A点剂量仍需报告,作为评价靶区剂量的参 考。以CTV-THR确定处方剂量,剂量至少达到 80 Gy,对于肿瘤体积大或退缩不佳病灶,应 该≥87 Gy。OAR限定剂量为:直肠2 cc≤65~ 75 Gy;乙状结肠2 cc≤70~75 Gy;膀胱 2 cc≤80~90 Gy。当腔内近距离治疗无法满足上 述剂量要求时,可考虑联合组织间插植放疗。 3.3.3.5 特殊情况后装治疗 对于子宫切除术后患者(尤其是阴道切缘 阳性或肿瘤近切缘者),可采用阴道施源器后装 治疗作为体外放疗的补充。以阴道黏膜表面或阴 道黏膜下5 mm处为参照点,高剂量率192Ir剂量为 20~24 Gy(EQD2)。对于子宫颈外生型大肿瘤, 特别是出血较多者,体外放疗前可先给予后装治 疗消瘤止血,肿瘤表面出血多采用阴道施源器, ? 482 中国抗癌协会妇科肿瘤专业委员会 子宫颈癌诊断与治疗指南(2021年版) ?以阴道黏膜表面为参考点,一般给予10~12 Gy。 3.3.4 OAR的耐受剂量 子宫颈癌放疗邻近器官的耐受剂量:子宫颈 癌放疗的OAR包括膀胱、直肠、结肠、骨髓、皮 肤、小肠、输尿管等,一般用TD5/5表示最小放射 耐受量,表示在治疗后5年内,预计严重并发症 发生率不超过5%。 3.3.5 根治性放射治疗时间控制 子宫颈癌放射治疗包含体外照射和腔内照 射,总时间应控制在7~8周内。 3.3.6 各期子宫颈癌的放疗 3.3.6.1 IA1期子宫颈癌的放疗 IA1期子宫颈癌的放疗以后装腔内治疗为 主,如果子宫颈锥切标本无淋巴脉管间隙浸润 (lymphovascular space invasion,LVSI),可单独 行后装治疗,子宫颈锥切标本有LVSI,后装治疗 ±盆腔外照射,参考点A点的EQD2为60~65 Gy。 3.3.6.2 IA2、IB1、IB2、IIA1期子宫颈癌 的放疗 采用盆腔外照射+后装治疗,盆腔外照射 45~50 Gy,后装治疗+外照射给予A点的EQD2为 75~85 Gy(EQD2)。 3.3.6.3 IB3、IIA2、IIB~IVA期子宫颈癌的放疗 放疗前必须进行盆腔淋巴结状况的评估, 建议用影像学评估或手术评估确定放射野,盆腔 45~50 Gy的体外放射剂量,局部病灶可以在图像 引导下加量10~15 Gy。如腹主动脉旁淋巴引流区 需加量,应在影像引导下予以45~50 Gy照射, 局部病灶可缩野加量10~15 Gy。对于子宫颈局 部病灶,后装治疗+外照射给予A点总剂量85 Gy 以上。放疗中应该有2~3次临床和影像学疗效评 估,必要时重新定位,以确定个体化治疗剂量。 3.3.6.4 IVB期子宫颈癌的放疗 IVB期子宫颈癌的放疗为姑息性治疗,剂量 基本同IVA期子宫颈癌治疗剂量,但由于有直肠 或膀胱侵犯,应尽量采用个体化放疗。 3.3.6.5 其他部位寡转移病灶 对于腹股沟、颈部淋巴结、肺、肝等寡转移 病灶,可以考虑根治性放疗。 采用SBRT给予1~5分次的较高剂量照射;照 射野内复发病灶的再程放疗可以考虑采用SBRT 技术[17]。 3.3.7 术后放疗 子宫颈癌术后放疗包括子宫颈癌根治术后放 疗及单纯性全子宫切除术后意外发现的子宫颈癌 的放疗。由于术后粘连,肠管的活动度变差,容 易导致肠道局部受量过大,推荐调强放疗等立体 照射技术,盆腔剂量45~50 Gy[15],建议在术后 8周内完成。放射野可根据术后病理学检查结果 来确定。有髂总或腹主动脉旁淋巴结转移者,腹 主动脉旁淋巴引流区也应给予(50±5)Gy的照 射剂量,阴道切缘阳性或近切缘者,应增加后装 近距离治疗,推荐柱状施源器阴道黏膜下0.5 cm 5.5 Gy×2次,或阴道黏膜面6.0 Gy×3次。详见 3.6.1 子宫颈癌根治术后辅助放疗。 3.4 子宫颈癌的化疗 子宫颈癌化疗以顺铂为基础的联合化疗或单 用顺铂化疗为主。目前主要适用于同步放化疗、 新辅助化疗和姑息化疗。同期放化疗一般采用顺 铂单药,不能耐受顺铂者可采用卡铂或可选择 的含铂联合化疗。新辅助化疗主要用于IB3或 IIA2期,即肿瘤直径≥4.0 cm的局部晚期子宫颈 癌术前化疗,一般2~3个疗程。新辅助化疗可以 提高局部控制率和手术切净率,但不能改善子宫 颈癌的预后,且术后病理学高危因素易被掩盖, 原则上不推荐使用。晚期及复发性子宫颈癌初 始化疗首选含铂类药物联合化疗+贝伐珠单抗的 联合方案,如顺铂/卡铂+紫杉醇/紫杉醇脂质体+ 贝伐珠单抗,也可选择顺铂+紫杉醇/紫杉醇脂质 体、拓扑替康+紫杉醇/紫杉醇脂质体等联合化疗 方案。接受化疗或化疗后出现疾病进展时,对于 PD-L1阳性或MSI-H/dMMR患者首选派姆单抗。 派姆单抗也可用于无法切除或转移性的高肿瘤突 变负荷(tumor mutation burden-high,TMB-H) 肿瘤,而拉罗曲替尼、恩曲替尼用于NTRK基因 阳性肿瘤(表6)。 3.5 各期子宫颈癌的治疗选择建议 3.5.1 IA1期子宫颈癌治疗 ?应根据患者是否有生育要求选择治疗方法。 有生育要求者:可采用子宫颈锥切术,子 宫颈锥切标本无脉管浸润,切缘至少达3 mm阴 性距离为适应证,如果切缘阴性(边缘没有浸润 《中国癌症杂志》2021年第31卷第6期 483 ?同步放疗 表 6 鳞状细胞癌、腺癌或腺鳞癌化疗方案 复发或转移性疾病 一线单药化疗 首选方案 顺铂 其他推荐方案 卡铂/紫杉醇 (紫杉醇脂质体) 卡铂/ (紫杉醇脂质体) ?一线联合化疗 二线化疗 首选方案 派姆单抗 (PD-L1阳性或MSI-H/dMMR) 其他推荐方案 贝伐珠单抗 白蛋白结合型紫杉醇 紫杉醇脂质体 多西他赛 5-氟尿嘧啶 吉西他滨 异环磷酰胺 伊立替康 丝裂毒素 培美曲塞 拓扑替康 长春瑞滨 ?首选方案 首选方案 顺铂 顺铂/紫杉醇/贝伐珠单抗 卡铂/紫杉醇(紫杉醇脂质体)?/贝伐珠单抗 卡铂 其他推荐方案 (患者不能耐受顺铂) 顺铂/紫杉醇(紫杉醇脂质体) 顺铂/紫杉醇 卡铂/紫杉醇(紫杉醇脂质体) (个体化选择) (对于之前接受过顺铂治疗的 患者) 拓扑替康/紫杉醇/贝伐珠单抗 性癌或高度鳞状上皮内病变)可选择观察,如果 切缘阳性,则推荐再次锥切或行子宫颈切除术。 有脉管浸润时,首选子宫颈根治性切除术+盆腔 淋巴结切除术(或SLN显影),手术先行盆腔淋 巴结切除,送快速冷冻切片病理学检查或快速石 蜡切片病理学检查。有转移者,应改行改良根治 性子宫切除术(B型);无转移者,行根治性子 宫颈切除术。次选子宫颈锥切+盆腔淋巴结切除 (或SLN显影),锥切切缘至少有3 mm的阴性距 离,如果切缘阳性,推荐再次锥切或行子宫颈切 除术。对于NECC、胃型腺癌或恶性腺瘤患者, 不支持其保留生育能力。 无生育要求者:IA1期无LVSI,行子宫颈锥 切术,确认锥切切缘阴性。不能手术者可选择观 察,可行手术者选择筋膜外子宫切除术(A型)。 如切缘阳性可考虑重复锥切活检以更好地评估浸润 深度以排除IA2/IB1期病变;或选择筋膜外或改 良根治性性子宫切除术(B型)+盆腔淋巴结切除术 (切缘为癌时淋巴结清扫为2B类证据)(或SLN显 影)。如果患者伴有淋巴血管受侵,行改良根治性 子宫切除术(B型)+盆腔淋巴结切除术(或SLN显 影)。对于不能手术的患者或拒绝手术的患者可选 择近距离治疗±外照射。根据正常组织的耐受性、 放疗分割方法和靶区大小调整方案。A点剂量一般 为60~70 Gy(EQD2)。 3.5.2 IA2期子宫颈癌治疗 IA2期子宫颈癌治疗仍可根据是否有生育要 求选择。 有生育要求者:行根治性子宫颈切除术+盆 腔淋巴结切除术,术中先行盆腔淋巴结切除, 送冷冻切片或快速石蜡切片检查,有淋巴结转移 者,改行根治性子宫切除术(C型)±腹主动脉 旁淋巴结取样(髂总淋巴结阳性或疑有腹主动脉 旁淋巴结转移者);淋巴结无转移者,行根治性 子宫颈切除术(子宫颈病变距切缘大于8 mm)。 无生育要求者:行改良根治性子宫切除术 (B型)+盆腔淋巴结切除术,年龄小于45岁者可 切除输卵管、保留双侧卵巢。 有手术禁忌、无生育要求者可选择根治性放 疗。近距离放疗±盆腔外照射,A点的EQD2一 般为70~80 Gy(EQD2)。 3.5.3 IB1、IB2及IIA1期子宫颈癌治疗 有生育要求者:IB1期可行根治性子宫颈 切除术(C型)。IB2期肿瘤直径为2.0~4.0 cm 者,推荐行经腹根治性子宫颈切除术(C型)。 术中先行盆腔淋巴结切除,送术中快速冷冻切片 病理学检查,如无转移,根治性子宫颈切除术 (C型)+盆腔淋巴结切除术±腹主动脉旁淋巴 结切除(可考虑行SLN显影:阳性和可疑均送术 中快速冷冻切片病理学检查);如有转移,应考 虑放弃手术改行根治性放疗或行根治性子宫切除 术(C型)+盆腔淋巴结切除术±腹主动脉旁淋 巴结切除。NECC和胃型腺癌被认为不适用此种 手术。 ? 484 中国抗癌协会妇科肿瘤专业委员会 子宫颈癌诊断与治疗指南(2021年版) ?无生育要求者可选择:1 根治性子宫切除 术(C型)+盆腔淋巴结切除(1类证据)±主动 脉旁淋巴结切除(2B类证据),可考虑行SLN 显影。绝经前如双侧卵巢正常,45岁前,可保留 双侧卵巢。根治性子宫切除术的标准术式是开腹 (1类证据)。2 有手术禁忌证或拒绝手术者, 可行盆腔外照射+阴道近距离放疗±含铂药物的 同期化疗。 3.5.4 IB3和IIA2期 (1) 盆腔外照射+含顺铂方案的同步化疗+近距 离治疗(传统方法为75~80 Gy至总A点)[A点 的EQD2≥85 Gy(EQD2),B点为40~50 Gy] (EQD2,首选)。对于阴道侵犯明显的患者, 必要时可加用阴道塞进行后装腔内放疗,黏膜 下0.5 cm处给予20~30 Gy(EQD2)。同时治疗 根据正常组织耐受性、分割和靶体积大小进行 调整[18-22]。 (2) 根治性子宫切除术(C型)+盆腔淋巴结 切除±主动脉旁淋巴结取样(肿瘤较大、怀疑或 已知有盆腔淋巴结疾病的患者)。首先进行盆腔 淋巴结切除术,如果淋巴结阴性,进行根治性子 宫切除术。如果淋巴结阳性,选择放化疗。不推 荐术前以铂类药物为基础的新辅助化疗,根治性 术后应根据病理学高危/中危因素选择放疗或同 步放化疗。 根治性子宫切除术后如有病理学高危因素 (淋巴结转移,子宫旁或手术切缘受累),首选 同步放化疗,时间在手术后6周内完成。目前有 研究结果显示,同步放化疗前化疗(紫杉醇+顺 铂),放疗后2个周期化疗与同步放化疗效果相 当[23-24],可用于放疗资源紧张的地区。 (3) 盆腔外照射+含顺铂方案的同步化疗+近 距离治疗+选择性子宫切除术(根治性放疗后子 宫颈病灶残存)。 初次放化疗后是否推荐辅助子宫切除术存在争 议,目前为3类证据推荐[25-26]。放疗后辅助子宫切除 术能改善盆腔控制,但不能改善总生存率[27-29]。对 于因疾病范围或子宫解剖学关系不能充分覆盖近距 离放疗的患者,可以考虑采用此方法。 3.5.5 IIB~IVA期子宫颈癌治疗 采用铂类药物为基础的同步放化疗,可选 择周化疗或3周化疗。常规放疗剂量:肿瘤直径 ≥4.0 cm,A点应达到85 Gy(EQD2)及以上, IIIB期患者B点应达到45~50 Gy(EQD2)。对于 盆壁受侵明显的患者,必要时可高适形缩野局部 盆腔加量10~15 Gy。对于阴道侵犯明显的患者, 建议采用三维后装放疗。放疗范围包括已知及可 疑肿瘤侵犯的部位。放疗中应该有2~3次临床和 影像学检查疗效评估,必要时重新定位,以确定 个体化治疗剂量。治疗结束后评估,进入随访; 若局部病灶持续存在或局部复发,考虑全身治疗 (化疗、靶向治疗、免疫治疗)、姑息性支持治 疗、子宫切除术或盆腔廓清术。推荐手术在放疗 后3个月左右评估,充分知情后决定。 免疫治疗可用于晚期或复发的子宫颈癌。免 疫治疗患者检出相关的分子标志物才能取得较高 的缓解率(包括PD-L1+、MSI-H、TMB-H等)。 其他药物靶向治疗和生物制剂仍然需要更多的临 床研究数据支持,鼓励参加相关的临床试验。 3.5.6 IVB期子宫颈癌 (1) 寡转移病灶,若适合局部治疗,可考虑局 部切除±个体化放疗,或局部消融治疗±个体化 放疗,或个体化放疗±全身系统性治疗,也可考 虑综合治疗。在进行盆腔局部放疗的同时,应加 强以铂类药物为基础的联合化疗,并针对转移灶 进行个体化治疗,加强对症治疗、营养治疗、止 痛治疗,以控制病情进展,改善生存质量。 (2) 全身广泛转移者,应进行全身系统性治疗 及最佳支持治疗,参加临床试验。 靶向治疗药物在IVB期患者中得到广泛应用, 以贝伐珠单抗为代表。贝伐珠单抗可应用于复发 晚期的子宫颈癌[30],通常与铂类药物/紫杉醇或 铂类药物/拓扑替康等联合使用,应用前仔细评估 患者胃肠道/泌尿生殖系统毒性的风险[31-33]。 3.6 子宫颈癌根治术后辅助治疗 3.6.1 子宫颈癌根治术后辅助放疗 (1) 术后病理学检查结果显示存在高危因素: 子宫颈癌根治术后存在淋巴结阳性、切缘阳性或 子宫旁阳性任一个高危因素均需补充放疗。术后 补充盆腔放疗+铂类同步化疗(1类证据)±阴道 近距离放疗,无髂总或腹主动脉旁淋巴结转移, 仅行盆腔照射;髂总、腹主动脉旁淋巴结转移, 《中国癌症杂志》2021年第31卷第6期 照射需包括腹主动脉旁淋巴引流区,如果盆腔淋 巴结多枚阳性,腹主动脉旁淋巴结清扫阴性,可 不延伸放射野,如未做腹主动脉旁淋巴结清扫, 可选择延伸放射野;如有腹主动脉旁淋巴结转移 者,还需进一步明确有无其他部位的远处转移。 (2) 术后病理学检查结果显示存在中危因素: 病理学类型和肿瘤浸润范围是重要因素,鳞状细 胞癌,需按Sedlis标准[34]来决定是否进行辅助 治疗,IB~IIA期子宫颈癌患者行根治性子宫切 除术后补充放疗或放化疗者,腺癌预后更差。因 此,腺癌或腺鳞癌患者术后是否补充治疗应参照 “四因素模式”[35-36],如肿瘤≥3.0 cm、浸润 子宫颈外1/3、间质脉管间隙见癌栓、腺癌/腺鳞 癌,术后病理学因素中,有以上4个中危因素中 的2个以上,应当辅助治疗。任何病理学类型, 病灶近切缘应当考虑辅助放疗[37]。 (3) 术后放化疗应遵循的原则: 1 术后存在高危因素者,补充治疗可选择同 步放化疗。 2 子宫颈癌术后放疗野设计应覆盖瘤床和 引流淋巴结区域在内的盆腹腔,通常剂量为45~ 50 Gy。 3 适型调强放疗(intensity-modulated radiotherapy,IMRT)是一种先进和精细的放射 治疗技术,有条件应用者可减少放疗的毒性及不 良反应。 4 对于切缘阳性或肿瘤靠近切缘者、肿瘤直 径大于4.0 cm或深间质浸润、子宫旁或阴道受累 者可采用阴道残端近距离放疗。 5 对于广泛的LVSI,需加铂类药物为主的 化疗加阴道残端近距离放疗。 3.6.2 意外发现子宫颈癌的术后治疗 因良性疾病进行单纯子宫切除术后病理学检 查意外发现子宫颈癌(仅包括鳞癌、腺癌、腺鳞 癌和NECC),由于手术范围不足,绝大多数患 者术后需接受进一步的治疗。 对这一类患者首先需明确病理学诊断,对 于病理学诊断不清者,尤其是无法判断IA1或 IA2期、是否有LVSI、切缘情况不明等,需明 确病理学诊断后制定治疗措施。其次,需进行全 面检查评估,包括手术范围、查体、血生化检 485 查和影像学检查。影像学检查包括盆腹腔CT、 肺CT及盆腔MRI,有条件者可行PET/CT检查, MRI对软组织有较高的识别度,可判断盆腔有无 病灶残留,CT和PET/CT有助于发现淋巴结问题 和是否有远处转移。根据病理学、影像学检查结 果,结合当地技术条件及患者具体情况选择以下 治疗方案: (1) 术后病理学诊断结果为IA1期,无 LVSI,术后可密切随访。 (2) 术后病理学诊断结果为IA1期且 LVSI(+)、IA2、IB1期及以上者,根据不同的 情况,可选择不同的后续处理方式,手术切缘的 情况与后续治疗方案的选择密切相关。 (3) 切缘和影像学检查均呈阴性,选择:1 盆腔放疗+阴道残端近距离放疗±含铂药物的同 步化疗;2 若子宫标本的病理学检查无Sedlis标 准中术后补充放疗的指征,可行根治性子宫旁切 除术+阴道上段切除+盆腔淋巴结切除±腹主动 脉旁淋巴结切除。再次术后病理学检查阴性,建 议随访;再次术后病理学检查结果提示淋巴结阳 性、手术切缘阳性或子宫旁阳性,则需辅助盆腔 放疗±阴道残段近距离放疗+同期化疗。 (4) 若病理学检查结果显示切缘阳性,或影像 学检查提示有明显肿瘤残留或盆腔淋巴结肿大,或 者子宫标本病理学检查有Sedlis标准中术后放疗的 指征,应行盆腔放疗+同步含铂化疗+阴道残端近距 离放疗。 (5) 意外发现子宫颈癌的患者在术后选择二次 手术治疗,需考虑手术后病理学检查结果、患者 对再次手术的耐受能力和当地医疗水平,作出综 合判断。虽然手术+术后放疗对意外发现的子宫 颈癌是可行的,但预后比直接广泛子宫切除差, 由于瘢痕、粘连形成和解剖学改变,手术难度增 加。第二次手术的优势在于适于部分早期年轻患 者,有望通过再次手术治愈,手术后无需辅助放 疗,可保留卵巢功能和阴道功能,避免放疗的不 良反应,有助于提高患者的生活质量。对评估术 后放疗概率大的病例,不推荐手术和放疗方式的 叠加,建议选择盆腔放疗+同期化疗。 3.7 复发性子宫颈癌的治疗 对复发性子宫颈癌进行治疗之前,尽量行复 ? 486 发病灶活检以明确复发或PET/CT证实复发。 3.7.1 局部复发的治疗 局限于子宫颈或阴道的子宫颈癌局部复发, 可针对复发部位进行以临床治愈为目标的治疗。 3.7.1.1 既往无放疗史或复发灶位于既往放疗野外 (1) 可手术切除病灶,手术后再行个体化的外 照射治疗±含铂药物化疗方案±近距离放疗。 (2) 不能耐受手术者或不接受手术者,外照射 放疗±同步化疗和(或)近距离放疗。 (3) 对于初始治疗后短期复发的患者,以全 身系统性治疗为主,按照复发性子宫颈癌系统 治疗选用化疗,鼓励参加临床试验和做相关基因 检测。 (4) 治疗后再复发者,选择化疗、靶向治疗、 支持治疗、免疫治疗,鼓励患者参加临床试验和 做相关基因检测。 3.7.1.2 既往有放疗史或复发病灶位于既往放疗 野内 (1) 中心性复发可选择手术治疗,手术应以临 床治愈为目的。最可能从手术中获益的患者:盆 腔中央复发,无侧盆壁固定或相关肾积水;无病 间期较长;复发肿瘤直径小于3.0 cm。 1 盆腔廓清术(前盆腔、后盆腔、全盆腔) ±术中放疗(无术中放疗条件者可考虑放射性 粒子植入放疗(3类证据),应同时进行盆底重 建,术后制订有关社会心理学及性心理学的康复 计划。 2 复发病灶直径<2.0 cm并经仔细评估的病 例,可行子宫切除术或近距离放疗。 (2) 不适合手术切除的患者,可予全身系统性 治疗、免疫治疗或插植放疗等。 (3) 非中心性复发治疗:1 针对肿瘤局部放 射治疗±化疗;2 切除肿瘤±术中放射性粒子植 入放疗(3类证据);3 以铂类药物为基础的联 合化疗,联合贝伐珠单抗;4 PD-1/PD-L1单抗 (单用或联合化疗);5 支持治疗;6 鼓励患 者参加临床试验。 (4) 治疗后再复发者可采用全身系统性治疗、 支持治疗、免疫治疗和参加临床试验。 3.7.2 远处转移复发的治疗 (1) 复发灶为多病灶或无法切除者,选择化 中国抗癌协会妇科肿瘤专业委员会 子宫颈癌诊断与治疗指南(2021年版) 疗、免疫治疗(PD-1/PD-L1单抗,单用或联合化 疗)、放射治疗。 (2) 病灶可切除者选择: 1 病灶切除±放疗。 2 化疗:一线化疗推荐以铂类药物为基础的 联合治疗,首选顺铂+紫杉醇加用血管生成抑制 剂贝伐珠单抗;一线治疗后疾病进展及不适合联 合化疗的患者,采用单药治疗,如卡铂、白蛋白 结合型紫杉醇、培布珠单抗。 3 PD-1/PD-L1单抗治疗。 4 参加临床试验。 3.8 妊娠期子宫颈癌的处理 3.8.1 诊断方法同非妊娠期子宫颈癌 3.8.2 评估 (1) 肿瘤评估:组织病理学类型、FIGO分 期、影像学检查(超声或MRI)诊断有无淋巴结 转移和肿瘤标志物(SCCA)。 (2) 胎次、妊娠阶段、胎儿的发育情况。 (3) 总体治疗原则:治疗方案应与产科医师、 患者及亲属充分沟通,综合考虑子宫颈癌的恶性 程度、孕周及胎儿发育情况,严密监测患者病情 发展及产科情况。应充分了解患者及其家属对妊 娠的期望等,在决定治疗方案前,患者及其家属 享有充分的知情权,结合肿瘤评估结果,选择是 否保留胎儿和恰当的治疗方式,获得患者及其家 属的知情同意。对各妊娠时期的子宫颈癌尚没有 成熟的方案,国际妇科肿瘤协会(International Gynecologic Cancer Society,IGCS)和欧洲妇 科肿瘤协会(European Society of Gynaecological Oncology,ESGO)2014年专家共识认为,在不 保留胎儿和生育功能时,处理同非妊娠期子宫 颈癌。 ???按照不同分期和孕期的治疗建议: 1 妊娠早期(孕20周以内),除子宫颈癌 IA1期外,不建议患者继续妊娠。 2 IA1期患者应严密监测,每8周行1次阴 道镜检查,必要时子宫颈活检,直至妊娠结束开 始治疗。无LVSI可行子宫颈锥切并行子宫颈环扎 术(低级别证据)。 3 妊娠中期(孕20~孕28周)要求继续妊 娠、IIB期以内者,可继续妊娠。IIB期以上 ? 《中国癌症杂志》2021年第31卷第6期 者,不建议继续妊娠。IB2期及IB3期继续妊 娠患者考虑行新辅助化疗,新辅助化疗可以维持 至孕34~35周。对于妊娠中期的处理目前争议较 大,应充分评估风险和尊重患者选择权。 4 妊娠晚期(孕28周以上)诊断子宫颈癌, 无论患者期别,患者要求继续妊娠者在孕34周、 胎儿肺成熟后采用剖宫产结束妊娠为宜,再根据 分期制订相应的治疗方案:IA、IB1期患者可 在剖宫产同时行根治性子宫切除术+淋巴结切除 术,避免放疗引起的纤维化,并保留卵巢功能; 根治性手术后如果需要行放疗的患者,可在切口 愈合后进行;IIB期以上的子宫颈癌患者,结束 妊娠后按分期选择同期放化疗。 3.9 NECC的治疗 该类肿瘤侵袭性强、易发生早期转移、预后 较差,对化疗相对敏感,这些对患者的诊治具有 重要意义。相对于子宫颈鳞癌、腺癌、腺鳞癌患 者,NECC有如下几个特点: 1 有别于其他常见类型子宫颈癌,NECC的 病理学诊断主要基于形态学改变,而无论免疫组 织化学结果如何。 2 初治评估及治疗过程使用:胸部/腹部/盆 腔的CT+脑部MRI,或颈部/胸部/腹部/盆腔/腹股 沟PET/CT+脑部MRI,以排除脑转移。 3 不推荐NECC患者保留生育功能。 4 IB3/IIA2期不推荐直接手术治疗。 5 NECC对化疗相对敏感,局部晚期患者可 行新辅助化疗。 6 无论首选手术还是首选放疗,治疗后所有 患者均推荐补充全身系统性治疗,化疗和同步放 化疗推荐首选使用顺铂+依托泊苷,若患者不能 耐受顺铂,可采用卡铂+依托泊苷。 7 放宽手术后补充放疗的指征。 8 对于新辅助治疗、术后辅助治疗,以及 出现疾病复发或转移的病例,一线推荐首选顺 铂+依托泊苷或卡铂+依托泊苷,二线推荐方案 与鳞状细胞癌/腺癌/腺鳞癌的一、二线推荐治疗 一致。 4 随访 4.1 随访间隔 治疗结束2年,每3~6个月随访1次,治疗结 487 束3~5年,每6~12个月随访1次。根据患者疾病复 发风险进行年度复查。 4.2 随访内容 随访内容包括:全身体格检查、妇科检查、 鳞癌抗原、细胞角蛋白等肿瘤标志物检测和子宫 颈或阴道残端细胞学、人乳头瘤病毒检查。必要 时行阴道镜检查及活体组织病理学检查、胸片、 胸部CT、盆腔MRI、超声、全身浅表淋巴结超声 检查。根据症状、体征怀疑复发时可进行相关实 验室、影像学检查,如血常规、血尿素氮、肌酐 等。根据检查结果,必要时行阴道镜检查及活体 组织病理学检查、胸片、胸部CT、盆腔MRI、超 声、全身浅表淋巴结超声检查。 [参 考 文 献] [1] OLAWAIYE A B, BAKER T P, WASHINGTON M K, et al. The new (version 9) American Joint Committee on Cancer tumor, node, metastasis staging for cervical cancer[J]. CA Cancer J Clin, 2021. Epub ahead of print. [2] DELARA R, YANG J, BUCKNER-PETTY S, et al. Surgical or imaging lymph node assessment in locally advanced cervical cancer: a systematic review and meta-analysis[J]. J Gynecol Oncol, 2020, 31(6): e79. [3] WHO Classification of tumours Editorial Board. Female Genital Tumours. WHO Classification of Tumours, 5th edition, vol. 4 [M]. Lyon: IARC Press, 2020: 8. [4] MINION L E, TEWARI K S. Cervical cancer-state of the science: from angiogenesis blockade to checkpoint inhibition [J]. Gynecol Oncol, 2018, 148(3): 609-621. [5] CHUNG H C, SCHELLENS J H M, DELORD J P, et al. Pembrolizumab treatment of advanced cervical cancer: updated results from the phase 2 KEYNOTE-158 study[J]. J Clin Oncol, 2018, 36(15_suppl): 5522. [6] MARABELLE A, LE D T, ASCIERTO P A, et al. Efficacy of pembrolizumab in patients with noncolorectal high microsatellite instability/mismatch repair-deficient cancer: results from the phase II KEYNOTE-158 study[J]. J Clin Oncol, 2020, 38(1): 1-10. [7] CIBULA D, ABU-RUSTUM N R, BENEDETTI-PANICI P, et al. New classification system of radical hysterectomy: emphasis on a three-dimensional anatomic template for parametrial resection[J]. Gynecol Oncol, 2011, 122(2): 264-268. [8] RAMIREZ P T, FRUMOVITZ M, PAREJA R, et al. Minimally invasive versus abdominal radical hysterectomy for cervical cancer[J]. N Engl J Med, 2018, 379(20): 1895-1904. [9] UPPAL S, GEHRIG P A, PENG K, et al. Recurrence rates in patients with cervical cancer treated with abdominal versus minimally invasive radical hysterectomy: a multi-institutional ? 488 中国抗癌协会妇科肿瘤专业委员会 子宫颈癌诊断与治疗指南(2021年版) ?retrospective review study[J]. J Clin Oncol, 2020, 38(10): 1030-1040. [10] WUYB,LIZM,WUHY,etal.Sentinellymphnodebiopsyin cervical cancer: a meta-analysis[J]. Mol Clin Oncol, 2013, 1(6): 1025-1030. [11] KADKHODAYAN S, HASANZADEH M, TREGLIA G, et al. Sentinel node biopsy for lymph nodal staging of uterine cervix cancer: a systematic review and meta-analysis of the pertinent literature[J]. Eur J Surg Oncol, 2015, 41(1): 1-20. [12] FRUMOVITZ M, PLANTE M, LEE P S, et al. The FILM trial: a randomized phase III multicenter study assessing near infrared fluorescence in the identification of sentinel lymph nodes (SLN) [J]. Gynecol Oncol, 2018, 149: 7. [13] LIM K, SMALL W Jr, PORTELANCE L, et al. Consensus guidelines for delineation of clinical target volume for intensity- modulated pelvic radiotherapy for the definitive treatment of cervix cancer[J]. Int J Radiat Oncol Biol Phys, 2011, 79(2): 348-355. [14] SMALL W Jr, BOSCH W R, HARKENRIDER M M, et al. NRG oncology/RTOG consensus guidelines for delineation of clinical target volume for intensity modulated pelvic radiation therapy in postoperative treatment of endometrial and cervical cancer: an update[J]. Int J Radiat Oncol Biol Phys, 2021, 109(2): 413- 424. [15] KLOPP A H, YEUNG A R, DESHMUKH S, et al. Patient- reported toxicity during pelvic intensity-modulated radiation therapy: NRG oncology-RTOG 1203[J]. J Clin Oncol, 2018, 36(24): 2538-2544. [22] MORRIS M, EIFEL P J, LU J, et al. Pelvic radiation with concurrent chemotherapy compared with pelvic and para-aortic radiation for high-risk cervical cancer[J]. N Engl J Med, 1999, 340(15): 1137-1143. [23] HUANG H, FENG Y L, WAN T, et al. Effectiveness of sequential chemoradiation vs concurrent chemoradiation or radiation alone in adjuvant treatment after hysterectomy for cervical cancer: the STARS phase 3 randomized clinical trial [J]. JAMA Oncol, 2021, 7(3): 361-369. [24] TRIFILETTI D M, SWISHER-MCCLURE S, SHOWALTER T N, et al. Postoperative chemoradiation therapy in high- risk cervical cancer: re-evaluating the findings of gynecologic oncology group study 109 in a large, population-based cohort [J]. Int J Radiat Oncol Biol Phys, 2015, 93(5): 1032-1044. [25] KEYS H M, BUNDY B N, STEHMAN F B, et al. Radiation therapy with and without extrafascial hysterectomy for bulky stage IB cervical carcinoma: a randomized trial of the Gynecologic Oncology Group[J]. Gynecol Oncol, 2003, 89(3): 343-353. [26] KOKKA F, BRYANT A, BROCKBANK E, et al. Hysterectomy with radiotherapy or chemotherapy or both for women with locally advanced cervical cancer[J]. Cochrane Database Syst Rev, 2015(4): CD010260. [27] COLOMBO P E, BERTRAND M M, GUTOWSKI M, et al. Total laparoscopic radical hysterectomy for locally advanced cervical carcinoma (stages IIB, IIA and bulky stages IB) after concurrent chemoradiation therapy: Surgical morbidity and oncological results[J]. Gynecol Oncol, 2009, 114(3): 404- [16] TAYLOR A, ROCKALL A G, REZNEK R H, et al. Mapping 409. pelvic lymph nodes: guidelines for delineation in intensity- modulated radiotherapy[J]. Int J Radiat Oncol Biol Phys, 2005, 63(5): 1604-1612. [17] HIGGINSON D S, MORRIS D E, JONES E L, et al. Stereotactic body radiotherapy (SBRT): technological innovation and application in gynecologic oncology[J]. Gynecol Oncol, 2011, 120(3): 404-412. [18] LANDONI F, MANEO A, COLOMBO A, et al. Randomised study of radical surgery versus radiotherapy for stage Ib-IIa cervical cancer[J]. Lancet, 1997, 350(9077): 535-540. [19] WHITNEY C W, SAUSE W, BUNDY B N, et al. Randomized comparison of fluorouracil plus cisplatin versus hydroxyurea as an adjunct to radiation therapy in stage IIB-IVA carcinoma of the cervix with negative para-aortic lymph nodes: a Gynecologic Oncology Group and Southwest Oncology Group study[J]. J Clin Oncol, 1999, 17(5): 1339-1348. [20] ROSE P G, BUNDY B N, WATKINS E B, et al. Concurrent cisplatin-based radiotherapy and chemotherapy for locally advanced cervical cancer[J]. N Engl J Med, 1999, 340(15): 1144-1153. [21] KEYS H M, BUNDY B N, STEHMAN F B, et al. Cisplatin, radiation, and adjuvant hysterectomy compared with radiation and adjuvant hysterectomy for bulky stage IB cervical carcinoma[J]. N Engl J Med, 1999, 340(15): 1154-1161. [28] TOUBOUL C, UZAN C, MAUGUEN A, et al. Prognostic factors and morbidities after completion surgery in patients undergoing initial chemoradiation therapy for locally advanced cervical cancer[J]. Oncologist, 2010, 15(4): 405-415. [29] HUGUET F, COJOCARIU O M, LEVY P, et al. Preoperative concurrent radiation therapy and chemotherapy for bulky stage IB2, IIA, and IIB carcinoma of the uterine cervix with proximal parametrial invasion[J]. Int J Radiat Oncol Biol Phys, 2008, 72(5): 1508-1515. [30] LEATH C A, STRAUGHN J M. Chemotherapy for advanced and recurrent cervical carcinoma: results from cooperative group trials[J]. Gynecol Oncol, 2013, 129(1): 251-257. [31] MCLACHLAN J, BOUSSIOS S, OKINES A, et al. The impact of systemic therapy beyond first-line treatment for advanced cervical cancer[J]. Clin Oncol (R Coll Radiol), 2017, 29(3): 153-160. [32] MARTH C, LANDONI F, MAHNER S, et al. Cervical cancer: ESMO clinical practice guidelines for diagnosis, treatment and follow-up[J]. Ann Oncol, 2018, 29(Suppl 4): iv262. [33] CIBULA D, P?TTER R, PLANCHAMP F, et al. The European Society of Gynaecological Oncology/European Society for Radiotherapy and Oncology/European Society of Pathology guidelines for the management of patients with cervical cancer [J]. Int J Gynecol Cancer, 2018, 28(4): 641-655. 《中国癌症杂志》2021年第31卷第6期 489 ?[34] SEDLIS A, BUNDY B N, ROTMAN M Z, et al. A randomized trial of pelvic radiation therapy versus no further therapy in selected patients with stage IB carcinoma of the cervix after radical hysterectomy and pelvic lymphadenectomy: a Gynecologic Oncology Group study[J]. Gynecol Oncol, 1999, 73(2): 177-183. [35] NOH J M, PARK W, KIM Y S, et al. Comparison of clinical outcomes of adenocarcinoma and adenosquamous carcinoma in uterine cervical cancer patients receiving surgical resection followed by radiotherapy: a multicenter retrospective study (KROG 13-10)[J]. Gynecol Oncol, 2014, 132(3): 618-623. [36] RYU S Y, KIM M H, NAM B H, et al. Intermediate-risk grouping of cervical cancer patients treated with radical hysterectomy: a Korean Gynecologic Oncology Group study [J]. Br J Cancer, 2014, 110(2): 278-285. [37] DIAZ E S, AOYAMA C, BAQUING M A, et al. Predictors of residual carcinoma or carcinoma-in-situ at hysterectomy following cervical conization with positive margins[J]. Gynecol Oncol, 2014, 132(1): 76-80. (收稿日期:2021-04-28 修回日期:2021-04-30) 子宫颈癌诊断与治疗指南(2021年版) 编写专家 主 编: 玛依努尔 新疆维吾尔自治区人民医院 周 琦 重庆大学附属肿瘤医院 副主编: 盛修贵 中国医学科学院肿瘤医院深圳医院 学术秘书: 邹冬玲 重庆大学附属肿瘤医院 李雨聪 重庆大学附属肿瘤医院 龙行涛 重庆大学附属肿瘤医院 主要编写人员(按姓氏笔画排序): 王 莉 河南省肿瘤医院 王纯雁 中国医科大学肿瘤医院/辽宁省肿瘤 医院 古扎丽努尔 新疆医科大学附属肿瘤医院 ·阿不力孜 龙行涛 重庆大学附属肿瘤医院 田小飞 陕西省肿瘤医院 刘乃富 山东省肿瘤医院 刘开江 上海交通大学医学院附属仁济医院 孙蓬明 福建省妇幼保健院 ·尼牙孜 李雨聪 重庆大学附属肿瘤医院 李隆玉 江西省妇幼保健院 邹冬玲 重庆大学附属肿瘤医院 张国楠 四川省肿瘤医院(电子科技大学医学院 附属肿瘤医院) 陈 刚 华中科技大学同济医学院附属 同济医院 周 琦 重庆大学附属肿瘤医院 柯桂好 复旦大学附属肿瘤医院 夏百荣 中国科学技术大学附属第一医院 郭红燕 北京大学第三医院 黄 奕 湖北省肿瘤医院 黄曼妮 中国医学科学院肿瘤医院 盛修贵 中国医学科学院肿瘤医院深圳医院 康 山 河北医科大学附属第四医院 蔡红兵 武汉大学中南医院
闫丽隽 主任医师 山西省肿瘤医院 妇科969人已读 - 精选 2019ASCCP基本风险的宫颈癌筛查结果异常的管理共识解读
● 446 ● 中国妇产科临床杂志 2020 年 7 月 第 21 卷 第 4 期 Chin J Clin Obstet Gynecol July 2020,Vol.21,No.4 ·共识解读· 2019 ASCCP 基于风险的子宫颈癌筛查结果异常的管理共识解读 李明珠??赵昀??李静然??赵超??魏丽惠 ?2019 美国阴道镜和宫颈病理学会(ASCCP)基于风险 的宫颈癌筛查结果异常和癌前病变管理指南是 ASCCP 发起 的宫颈癌筛查异常后处理的第四次共识指南,第一次共识 会议于 2001 年召开 [1],随后分别于 2006 年 [2] 和 2012 年 [3] 进行了更新。2012 年 ASCCP 共识中已首次提出同等风 险,同等管理的原则,即对 5 年内发生宫颈高级别及以上 病变(CIN3+)的风险进行分层管理,这在概念上是一大 突破,但这一评估依赖于复杂的计算,而且没有充分纳入 既往筛查史。2015 年 ASCCP 发布了一版过渡指南 [4],主 要针对 HPV 初筛提出了管理建议。2019 年 ASCCP 宫颈癌 筛查结果异常和癌前病变的管理共识(以下简称为 2019 版 指南)[5],在既往指南的基础上再次更新,与之前版本的关 键区别在于其基于风险值的量化和细化,加入“阈值”概 念,同等风险,同等管理更加精细化。例如,从 HPV 阳 性的 ASC-US、LSIL 建议进行阴道镜检查,变为 2019 版 “基于风险”的推荐:既往筛查和此次筛查结果,当前发生 CIN3+ 的风险在 4.0% 以上者,建议进行阴道镜检查。提出 这一改变的依据是基于此次筛查结果和既往筛查史 ( 包括 未知史 ) 组合风险评估表 [6]。这个评估表来自于凯撒机构 (KPNC)的一项前瞻性纵向队列研究,该研究对 150 多万 名女性进行了历经 10 年以上的随访,详细描述了各种风险 指标的处理,对此版指南中评估不同风险管理具有决策性 的意义。风险升高的患者,建议进行更频繁的监测、阴道 镜检查和治疗;而对风险较低的患者可以推迟阴道镜检查, 进行更长时间的随访监测,当风险足够低时,再回到常规 筛查。 2019 版指南具体在以下几个方面进行了更新: 一、关于宫颈癌筛查方法 基于 HPV 的检测是风险评估的基础。2019 版指南使 用基于 HPV 的检测,指的是 HPV 初筛或 HPV 检测与宫颈 细胞学的联合筛查。HPV 感染的特征,包括 HPV 类型和 感染持续时间,共同决定了 CIN 3+ 的罹患风险。与 HPV 检测相比,细胞学较低的敏感性和阴性预测值影响其作为 长期风险预测的效果 [7]。单独 HPV 检测或与细胞学的联合 筛查,可延长随访间隔和推迟低风险人群的阴道镜检查。 应采用美国食品和药物管理局(FDA)批准的用于筛查的 方法,需注意的是所有 HPV 检测仅指高危 HPV 类型的检 doi:10.13390/j.issn.1672-1861.2020.04.035 作者单位:100044 北京大学人民医院妇产科 通信作者:魏丽惠 Email:weilhpku@163.com 测。未经 FDA 批准的 HPV mRNA 和 HPV DNA 检测仅可 用于与细胞学联合进行筛查,除非有充分、严格的数据支 持其不同方式的使用 [8]。 只有在无法进行 HPV 检测或无法进行联合筛查的情 况下,才采用单一细胞学检查作为检测手段。如果应用 HPV 检测或联合筛查间隔每年一次,那么单一细胞学检查 则需要每 6 个月一次;如应用 HPV 检测或联合筛查间隔每 3 年一次,单一细胞学筛查则需要每年一次。 二、个性化、基于风险的管理依据当前筛查结果和既 往筛查史结合 2001 版共识首次确定了阴道镜的转诊阈值,即低级别 鳞状上皮内病变(LSIL)和 HPV 阳性的 ASC-US 患者,这 一建议一直延续到 2006 版和 2012 版。2019ASCCP 工作 组回顾多项数据发现,直接转诊阴道镜患者当前发生 CIN 3+ 的风险为 3%~7%[9]。该风险应由当前筛查结果和既往 病史(包括未知病史)以及既往宫颈病变治疗情况综合评 估。即使相同的当前筛查结果,根据既往筛查史评估后会 有不同的管理建议。总体评估原则:根据当前筛查和既往 筛查结果,如当前 CIN3+ 风险 ≥ 4%,应立即进行阴道镜 检查或治疗;如当前 CIN3 风险 < 4%,则评估其 5 年内发 生 CIN3+ 风险,以确定患者是否应在 1 年、3 年或 5 年后 进行随访。 2019 版指南根据不同风险阈值提出以下处理组合分别 为:观察随防、阴道镜检查和治疗,分别代表了不同 CIN3 风险的阈值层面,见图 1。每个风险层的最低阈值,称为 临床操作阈值(clinical action threshold, CAT),决定了下一 步管理建议的级别,具体可通过智能应用程序或通过网址 当前CIN3+风险 25%~59% 推荐快速治疗 ??≥4% 当前CIN3+风险 4%~24% 阴道镜或快速治疗 ?可以接受 ?当前CIN3+ 风险 5年内CIN3+风险 ≥ 0.55% 推荐阴道镜 检查 ??5年内CIN3+风险 0.15%~0.54% 1年复查 ??<4% ?图 1 风险阈值及处理推荐图示 当前CIN3+风险 60%~100% ?5年内CIN3+风险 <0.15% 3年复查 ?5年复查 ? 中国妇产科临床杂志 2020 年 7 月 第 21 卷 第 4 期 Chin J Clin Obstet Gynecol July 2020,Vol.21,No.4 ● 447 ● ?http://cervixca.nlm.nih.gor/Risk Tables/ 查 询 表 格 来 确 定 其 处 于何种风险级别。 三、HPV 阳性的分流问题 所有初筛为 HPV 阳性者,无论 HPV 基因型如何,均 建议用同一次实验室样本进行细胞学的分流检测。这一项 建议对其同等风险,同等管理的指导意义更加明确(如 HPV16 阳性细胞学阳性进行阴道镜检查,但如 HPV16 阳 性细胞学 HSIL 直接快速治疗)。这一推荐与 2015 宫颈癌 筛查异常的临时指南中关于 HPV16/18 可直接转诊阴道镜, 非 HPV16/18 需要细胞学分流的建议不同,2019 版指南指 出 HPV 阳性,无论 HPV 分型如何都要进行细胞学检查。 但 HPV16/18 阳性发生 CIN3 和隐匿性癌的风险较高,因 此即使细胞学检查结果为阴性,也有必要进行阴道镜检查。 另外如 HPV16/18 阳性,但实验室无法提供对同一样本细 胞学的分流检测的条件,患者也可直接转诊阴道镜 [4]。 四、阴道镜检查实践 依据 ASCCP 阴道镜标准 [10]:阴道镜检查中最大限 度地检出 CIN2+ 至关重要,如果没有发现 CIN2+,管理力 度也会降低,仍建议对不同部位醋白区域进行 2~4 块活检。 对于风险较低的人群:细胞学 HSIL 以下、无 HPV16/18 和阴道镜印象完全正常(无任何化生或其他可见异常的醋 白,且有完整可见的鳞柱交界),这种情况发生隐匿 CIN 2+ (1%~7%)和 CIN3( < 1%)的风险较低。不建议进行无 目标性(随机)活检,随访即可。为了确保 CIN2+ 不被遗 漏,ASCCP 阴道镜标准强调了活检的必要性,即阴道镜下 任何程度的化生或其他异常的醋白上皮均应进行活检。 ??五、关于快速治疗的处理推荐 在 2012 版指南中,快速治疗(无需阴道镜活检直接 进行治疗)是宫颈高级别病变患者的一种选择 [3],2019 版再此基础上进行了更明确的定义。KPNC 的数据显示, HPV 阳性,细胞学 HSIL 时,当前 CIN3 和 CIN2 的风险 分 别 为 49% 和 77%[6]; 细 胞 学 HSIL,HPV16 时,CIN3 和 CIN2 的当前风险分别为 60% 和 77%[11]。故对于 25 岁及以 上的非妊娠患者,当 CIN3+ 即刻风险 ≥ 60% 时(如细胞学 HSIL,HPV16+),优先推荐快速治疗。对于 CIN3+ 当前风 险在 25%~60% 之间的患者,可以先进行阴道镜检查或直 接快速治疗。但是在选择快速治疗时,医患应充分沟通共 同决策,特别是对于担心治疗会对今后妊娠结局有潜在影 响的患者。 ??六、高级别鳞状上皮内病变组织病理学报告的推荐 基于 2014 年下生殖道肛门 - 生殖器鳞状上皮内病变术 语(LAST)/ 世界卫生组织(WHO)对宫颈高级别病变进 行二级分类报告结果:即高级别鳞状上皮内病变(HSIL) 和 LSIL,2019 版建议组织病理学报告应包括 CIN2 或 CIN3 限定性词语,因这两种类型的进展风险及治疗方式的选择 有所不同,应采用 HSIL(CIN2)、HSIL(CIN3)的方式报告。 对于一些 CIN 2,保守治疗是可接受的 [12],故 2019 版指南 HSIL 治疗的管理也将 CIN2 和 CIN3 的管理方案根据不同风 险进行推荐,并继续推荐 p16 免疫组织化学在 HSIL(CIN 2 或 CIN 3)组织形态学的应用。但应避免 p16 应用不当, 造成宫颈组织学过度诊断的风险,例如组织形态为 CIN1, 即使 p16 阳性也不应升级为 HSIL(CIN2)。 七、高级别病变的治疗管理和随访 1. 治疗后随访间隔问题 2019 版与 2012 版不同之处在于锥切后首次随访间隔 不再是 12 个月,而是治疗后 6 个月进行基于 HPV 检测的 复查。根据 KPNC 数据,HSIL 治疗后联合检测 /HPV 检 测连续 1、2、3 次阴性后 5 年发生 CIN 3+ 的风险分别为 1.7%/2.0%、0.68%/0.91% 和 0.35%/0.44%[6]。 因 此, 建 议 首次治疗后 6 个月随访如阴性,则每年联合检测或 HPV 检测,直到连续三次阴性。2012 年指南建议 5 年的筛查 间隔,但没有具体说明何时应该停止筛查。KPNC 数据显 示,HSIL 治疗后 5 年 CIN 3+ 的风险仍然高于 0.15% 的阈 值,人群长期研究显示,HSIL 治疗后宫颈癌风险持续增加 2 倍,风险至少持续 25 年,尤其是 50 岁以上人群 [13]。因 此,2019 版指南推荐 3 次阴性随访后,进入每 3 年间隔的 基于 HPV 的检测,至少 25 年。只要患者的预期寿命和接 受筛查的能力没有因健康问题受到严重影响,那么 25 年后 继续间隔 3 年的持续监测也是可以接受的。 2. HSIL(CIN2 和 CIN3)在不同人群的管理 在 2012 年的指南中,21 岁至 24 岁的患者被认为是 一个特殊人群。在目前的指南中,共识是将这一组统称为 “25 岁以下的患者”。以 25 岁为界的原因为 25 岁以下人群 HPV 感染和 CIN2 的自然逆转率很高 [14],肿瘤发病率明显 低于 25 岁以上人群。 系统回顾 CIN2 进行保守治疗后,50% 逆转,32% 持 续,18% 进展为 CIN3,多数消退发生在起初的 12 个月 内,进展率随时间延长而增加,在 30 岁以下消退率较高 (60%)[12]。故 2019 版推荐,对于 <25 岁或≥25 岁有生 育愿望的女性,可采取观察方案,但适用于鳞柱交界完全 可见,宫颈管取样无 CIN2+ 或未定级的 CIN。对于 <25 岁女性,可采用阴道镜和细胞学随访, ≥ 25 岁观察方案 为阴道镜和 HPV 检测为主,首次 6 个月和 12 个月复查。 在观察期间,如果 2 次连续细胞学<ASC-H,病理结果 <CIN2,对于≥25 岁进行基于 HPV 检测为主,<25 岁 细胞学为主,共一年,如果结果仍为阴性,进行基于 HPV 检测每年一次共 3 年,如阴性进入每 3 年一次随访至少 25 年,但如果 CIN2 持续 2 年,建议治疗。CIN3 推荐进行 治疗。另外,如果鳞柱交界不可见,或病变上界不可见或 ECC 为 CIN2 不建议观察,因 CIN2 可能升级,建议进行 宫颈锥切术。 3. 关于 HSIL 的治疗选择问题 HSIL 首选切除性治疗,包括环形电切术(LEEP 或 LLETZ)、冷刀锥化、激光锥活检。消融治疗不建议使用 的情况:1 病变向颈管内延伸;2 当病变覆盖超过 75% 的子宫颈外表面,病变范围超出正在使用的冷冻头治疗范 围时;3 鳞柱交界不完全可见,或病变上边界不完全可 见;4 颈管 CIN2+ 或不能分级的 CIN;5 有 CIN2 的治疗 ? ?● 448 ● 中国妇产科临床杂志 2020 年 7 月 第 21 卷 第 4 期 Chin J Clin Obstet Gynecol July 2020,Vol.21,No.4 ?史;6 活检检查不充分;7 可疑宫颈癌。子宫切除术作为 HSIL(CIN2 或 CIN3)的治疗首要选择是不可取的。除了 特定的临床试验外,对于 HSIL(CIN2 或 CIN3),采用外 用制剂或治疗性疫苗等试剂治疗也是不可取的 [5]。 5. 原位腺癌(AIS)的处理 活检确诊的 AIS 患者,建议进行诊断性切除手术,以 除外浸润性腺癌,即使最终计划进行子宫切除术也应如此。 当 AIS 锥切切缘阴性,可进行单纯子宫切除,当切缘阳 性时,需要二次切除以保证切缘阴性,即使计划切除全子 宫。如果无法保证阴性切缘,保留生育的处理也是不推荐 的。为达到理想的标本长度,在实施 LEEP 后进行“牛仔 帽”式颈管切除使标本破坏是不可取的。切除标本深度至 少 10 mm,对于无未来生育要求者,可将切除标本深度增 加至 18~20 mm。 保留生育功能管理:联合检测及宫颈管取样推荐每 6 个月至少 3 年,之后每年一次,至少 2 年,或直到子宫切 除术。如果连续 5 年都是阴性,可在第 6 年延长至筛查间 隔每三年一次。锥切切缘和宫颈管内取样均可预测子宫切 除标本的残留病变和浸润性癌的风险,HPV 检测阳性是 AIS 复发较有力的预测因素 [13, 15]。 6. 65 岁以上既往筛查异常人群的管理 65 岁以上人群如接受 HPV 检测、联合检测或细胞学 检查,依据 25~65 岁患者方案管理执行。大约 20% 的宫颈 癌发生于 65 岁以上患者 [16]。为了降低 65 岁以上患者的癌 症风险,管理指南建议对结果异常的 65 岁及不符合退出 标准的患者进行持续检测。由于多项指南推荐对于 65 岁 以上接受过充分筛查的患者停止常规筛查,因此关于老年 患者特定筛查试验结果预后价值的数据是有限的。但既往 CIN 3+ 的 65 岁以上患者再发宫颈癌或阴道癌的风险更高, 故对这一类 65 岁以上人群仍需继续监测 [13]。 2019 版指南是基于多项大样本的临床研究结果,在既 往指南基础上进行了更新和完善,也体现出同等风险、同 等管理的精细化,但在学习指南的同时,应了解这是基于 美国筛查策略的变更,没有任何一个指南是放之四海而皆 准的,正如指南中所讲,2019 版指南是推荐在美国本土应 用的宫颈癌筛查和病变管理的指导方针,但是其精细化管 理理念对于我国也有很多学习和借鉴的地方。 参考文献 [1] Wright TJ, Cox JT, Massad LS, et al. 2001 Consensus guide- lines for the management of women with cervical cytological abnormalities[J]. J Low Genit Tract Dis, 2002, 6(2):127-143. DOI: 10.1097/00128360-200204000-00012 [2] Wright TJ, Massad LS, Dunton CJ, et al. 2006 consensus guide- lines for the management of women with abnormal cervical can- cer screening tests[J]. Am J Obstet Gynecol, 2007, 197(4):346- 355. DOI: 10.1016/j.ajog.2007.07.047. [3] Massad LS, Einstein MH, Huh WK, et al. 2012 updated consen- sus guidelines for the management of abnormal cervical cancer screening tests and cancer precursors[J]. Obstet Gynecol, 2013, 121(4):829-846. DOI: 10.1097/AOG.0b013e3182883a34. [4] Huh WK, Ault KA, Chelmow D, et al. Use of primary high- risk human papillomavirus testing for cervical cancer screening: interim clinical guidance[J]. Gynecol Oncol, 2015, 136(2):178- 182. DOI: 10.1016/j.ygyno.2014.12.022. [5] Perkins RB, Guido RS, Castle PE, et al. 2019 ASCCP risk-based management consensus guidelines for abnormal cervical cancer screening tests and cancer precursors[J]. J Low Genit Tract Dis, 2020, 24(2):102-131. DOI: 10.1097/LGT.0000000000000525. [6] Egemen D, Cheung LC, Chen X, et al. Risk estimates sup- porting the 2019 ASCCP risk-based management consensus guidelines[J]. J Low Genit Tract Dis, 2020, 24(2):132-143. DOI 10.1097/LGT.0000000000000529. [7] Schiffman M, Kinney WK, Cheung LC, et al. Relative per- formance of HPV and cytology components of cotesting in cervical screening[J]. J Natl Cancer Inst, 2018, 110(5):501-508. DOI:10.1093/jnci/djx225. [8] Clarke MA, Darragh TM, Nelson E, et al. Reporting and assess- ing the quality of diagnostic accuracy studies for cervical cancer screening and management[J]. J Low Genit Tract Dis, 2020, 24(2):157-166. DOI: 10.1097/LGT.0000000000000527. [9] Wright TC, Stoler MH, Behrens CM, et al. Primary cervical can- cer screening with human papillomavirus: end of study results from the ATHENA study using HPV as the first-line screening test[J]. Gynecol Oncol, 2015, 136(2):189-197. DOI: 10.1016/ j.ygyno.2014.11.076. [10] Wentzensen N, Massad LS, Mayeaux EJ, et al. Evidence-based consensus recommendations for colposcopy practice for cervical cancer prevention in the United States[J]. J Low Genit Tract Dis, 2017, 21(4):216-222. DOI: 10.1097/LGT.0000000000000322. [11] Demarco M, Egemen D, Raine-Bennett TR, et al. A study of partial human papillomavirus genotyping in support of the 2019 ASCCP risk-based management consensus guidelines[J]. J Low Genit Tract Dis, 2020, 24(2):144-147. DOI: 10.1097/ LGT.0000000000000530. [12] Tainio K, Athanasiou A, Tikkinen K, et al. Clinical course of untreated cervical intraepithelial neoplasia grade 2 under ac- tive surveillance: systematic review and meta-analysis[J]. BMJ, 2018, 360:k499. DOI: 10.1136/bmj.k499. [13] Strander B, Andersson-Ellstr?m A, Milsom I, et al. Long term risk of invasive cancer after treatment for cervical intraepithelial neoplasia grade 3: population based cohort study[J]. BMJ, 2007, 335(7629):1077. DOI: 10.1136/bmj.39363.471806. [14] Silver MI, Gage JC, Schiffman M, et al. Clinical outcomes after conservative management of cervical intraepithelial neoplasia grade 2 (CIN2) in women ages 21-39 years[J]. Cancer Prev Res (Phila), 2018, 11(3):165-170. DOI: 10.1158/1940-6207. [15] Costa S, Venturoli S, Origoni M, et al. Performance of HPV DNA testing in the follow-up after treatment of high-grade cervical lesions, adenocarcinoma in situ (AIS) and microinva- sive carcinoma[J]. Ecancermedicalscience, 2015, 9:528. DOI: 10.3332/ecancer.2015.528. [16] Feldman S, Cook E, Davis M, et al. Cervical cancer incidence among elderly women in Massachusetts compared with younger women[J]. J Low Genit Tract Dis, 2018, 22(4):314-317. DOI 10.1097/LGT.0000000000000435. (收稿日期 : 2020-05-12) ??
闫丽隽 主任医师 山西省肿瘤医院 妇科1887人已读 - 精选 学术看点|关铮教授:宫颈锥切术——小手术大学问
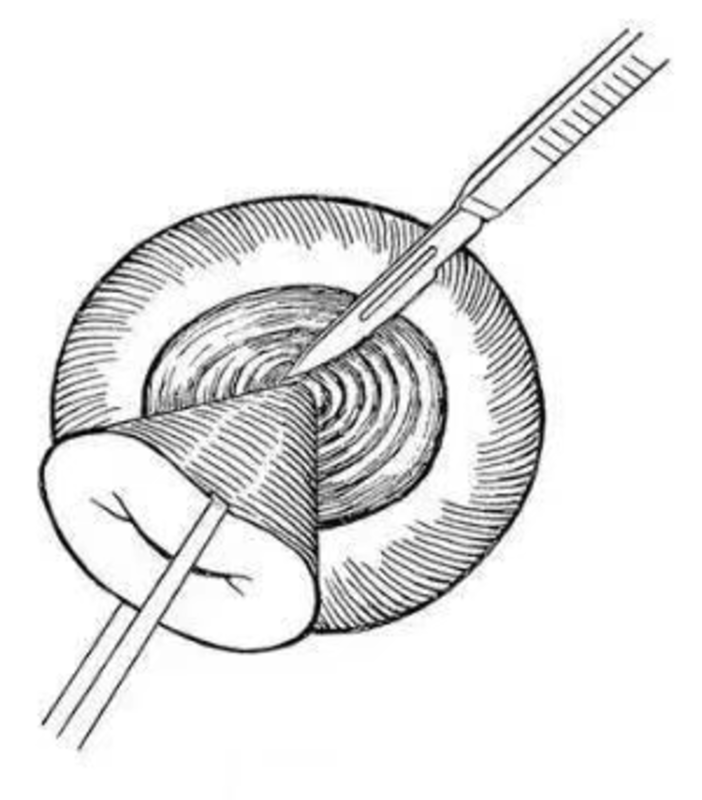
妇产科在线 妇产科在线 2018-06-20 宫颈锥切术是切除部分子宫颈的一种手术,即由外向内呈圆锥的形状切下一部分宫颈组织,包括宫颈环形电切术 一、何时切? 宫颈锥切术的指征为宫颈鳞状上皮内高度瘤样病变(HSIL)或CIN2-3级。禁忌症包括:1.可疑浸润癌或腺上皮不典型增生;2.病变累及宫颈管范围超过1cm,或看不见病变边缘或上限;3.宫颈感染或盆腔炎性疾病;4.妊娠或产后12周内;5.异常出血。 HSIL和LSIL是2014年WHO的新分类,免疫组化P16是HSIL和LSIL划分的重要标志,具体划分如下表: 二、如何切? (一)宫颈锥切术分型 在传统的手术学图谱中,宫颈锥切术的切除范围包括整个鳞柱交界,锥高在2.5cm以上,所以过去手术范围较大。目前,宫颈锥切术分为三型,要求切除完整的转化区和鳞柱交界部以上的部分宫颈管。 因此,可根据宫颈移行区的位置来决定宫颈锥切的发小,且切除范围一定要包括宫颈移行区。 (二)宫颈锥切术分类 根据手术器械类型,宫颈锥切术包括宫颈冷刀锥切(CKC)、宫颈电刀锥切(EKC)、宫颈环形电切(LEEP)、宫颈射频刀锥切、宫颈冷冻治疗等。但射频治疗和冷冻治疗破坏宫颈组织,无法进行病理检查。 1.宫颈冷刀锥切是宫颈锥切术的标准术式。其主要优势为:(1)可一次性切除足够大的、完整的宫颈用于组织病理检查,且锥切标本边缘的切净率较高;(2)切除标本边缘不影响组织病理学诊断;(3)可用于腺上皮异常者的诊断。但该手术方式出血不易控制,易引起并发症。该手术方式主要适用于以下情况 :(1)宫颈细胞学HSIL,阴道镜检查阴性或不满意;(2)阴道镜检未看到病变的边界或未见鳞柱交界的上界;(3)主要病灶位于宫颈管内或HSIL延伸入宫颈管内;(4)TCT诊断较阴道镜下宫颈活检的病理结果重(相差2级);(5)宫颈管搔刮术(ECC)的病理结果为异常或不能确定;(6)TCT示腺上皮异常或可疑宫颈腺癌或原位癌;(7)宫颈活检病理提示可疑微小浸润癌;(8)TCT、阴道镜怀疑宫颈浸润癌,但活检病理未能证实;(9)外宫颈病变范围广,累及宫颈四象限,甚至延伸至阴道穹窿。需要注意的是以上宫颈冷刀锥切术的适应症均不适宜行LEEP治疗。 2.宫颈电刀锥切就是应用电刀取代冷刀,该手术可获取足够大的宫颈椎体用于病理检查,且术中出血少,止血效果好,但电刀可致切缘电凝处组织变性,影响病理医生对靠近切缘处病变的判断。该缺点随着P16染色的出现被弥补,如果P16染色弥漫强阳性,代表切缘阳性,即切缘未切净;如果P16染色阴性,说明是电凝导致了组织变性。 3.宫颈电热圈环切术(LEEP)是通过环形金属丝(圈电极)传到高频交流电,利用高频电流所特有的干燥脱水效应、电弧切割效应来对电极接触的组织进行快速切开。常用的切除模式为移行带环切术和子宫颈环锥切。LEEP用于CIN1和ASC-US诊断时,活检的宫颈深度和颈管的深度约4mm,既可达到诊断和治疗作用,又避免切除过多组织,比宫颈钳活检术优越。 4.锐扶刀的形状与LEEP有相似之处,锐扶刀宫颈锥切是一种射频消融技术,最大的优点是止血效果好,切缘没有热损伤,不影响病理诊断。 (三)术后处理 宫颈锥切术后处理是临床医生需要重点关注的内容之一,包括术后并发症的处理、术后随访和术后妊娠的相关问题。 1.宫颈锥切术后并发症 宫颈锥切术后并发症包括出血、感染、宫颈管口粘连、创面子宫内膜异位症等。出血是最常见的术后并发症,有术后早期和晚期出血。术后早期出血是指宫颈锥切术后即刻出血和术后1-2天内创面出血,多因手术止血不彻底导致,可根据术者经验术中采用“8”字或锁边缝合创面防治出血。然而,术者在止血时一方面要考虑如何妥善止血,另一方面还要考虑如何防止术后宫颈管粘连,可采用宫颈管处放置导尿管、碘伏纱条等措施。此外,强调月经干净以后行宫颈锥切手术,其主要原因包括两方面:①区别阴道出血是月经血还是手术创面出血;②降低宫颈创面子宫内膜异位症发生风险。 2.宫颈锥切术后随访 由于宫颈锥切术后患者比普通人群患宫颈癌风险高2-5倍以上,因此术后要定期随访。术后1-2个月随访主要观察创面愈合进程,术后6个月行TCT及HPV检测,随访阳性者则需要阴道镜再次评估。 三、切缘阳性怎么办? 1.切缘未净的定义 鳞状上皮内病变:紧邻切缘指病变距离切缘3mm。 腺上皮病变:因其具有病变的跳跃性,要求病变距离切缘>7mm才安全。 宫颈管内切缘阳性:出现残留复发的风险高。 2.切缘阳性的处理原则 符合以下条件者,可进行随访:①无腺上皮异常证据;②无宫颈管切缘阳性;③无浸润性病变的证据;④患者年龄小于50岁。 当出现内切缘阳性,腺体受累或多象限受累,患者年龄≥50岁,阴道镜检查困难,随访条件差等情况时,需要行再次宫颈锥切术或子宫切除术。其中,单纯全子宫切除的指征主要包括:无生育要求;充分的宫颈切除后切缘仍为阳性;锥切治疗后存在高级别细胞学异常;患者不愿意接受保守治疗;因某些原因无法进行充分的TCT,如宫颈管狭窄;患者存在其他切除子宫的指征;已排除浸润性疾病。 3.宫颈锥切术后复发 关于宫颈锥切术后复发的问题有个概念需要理解,即病变残留和病变复发。病变残留指术后6个月内发现宫颈病变,病变复发指术后6个月以上发现宫颈病变(第一次TCT复查阴性后又出现CIN者)。 宫颈锥切术后复发与手术方式、手术切缘状况、腺体受累、HPV持续感染等因素相关。①研究显示,CKC与LEEP相比,术后1年宫颈病变复发率低,HPV清除率高。②宫颈锥切术后切缘阳性复发率高,宫颈管搔刮术(ECC)可预测病灶残留,对判断宫颈管内病变和复发有很重要的意义。③研究发现,腺体受累者复发率是无受累的4.51倍,此时宫颈锥切的深度可影响病灶残留和复发率。④锥切术后HPV逐渐被清除,多数在6个月内转阴(术后6个月复查较为合理),但仍有20%的术后患者HPV持续感染。根据相关资料,LEEP术后3个月、6个月、9个月和12个月的HPV持续阳性率分别为44.6%、10.6%、2.1%和2.1%。数据调查发现HPV阳性者复发率明显高于阴性者(9.2%:1.9%)。 四、宫颈锥切术与妊娠 1.宫颈锥切术对妊娠的影响 宫颈锥切术后由于宫颈长度缩短、宫颈壁变薄,约20%术后妊娠患者存在不良结局,晚期流产的比例是非锥切者的7倍,而锥切类型、锥切大小、宫颈长度是宫颈锥切术后早产的三个高危因素。 一组关于宫颈切除深度对妊娠结局的影响数据资料如下: 宫颈切除深度>10mm时,将增加早产的风险; 宫颈切除深度>12mm时,早产风险增加3倍; 宫颈切除深度10-14mm时,早产绝对风险为8%; 宫颈切除深度>20mm时,早产风险将上升至18%。 由上可知,宫颈锥切的锥高越高,早产风险将越大。 2.宫颈机能不全 (1)定义:早孕期无宫缩时出现宫颈扩张,而无法维持继续妊娠 (2)诊断:①病史:多次孕中期妊娠自然流产史或早产史;②查体:8号宫颈扩张棒无阻力通过;孕期无痛性宫颈扩张,羊膜囊突出;③子宫输卵管造影:子宫峡部漏斗区呈管状扩张;④超声:非孕期宫颈管宽径>6mm,宫颈管长度
 闫丽隽 主任医师 山西省肿瘤医院 妇科4372人已读
闫丽隽 主任医师 山西省肿瘤医院 妇科4372人已读
问诊记录 查看全部
- 宫腔内高回声结节 发现宫腔内高回声结节10个月,宫腔内高回声结节缓慢增大,月经... 高回声结节有可能是什么病变?是否需要宫腔镜检查?需要住院吗?总交流次数2已给处置建议
- 县医院检出子宫肌瘤20mm,未用药 大半年继继续续有恶露,咋天县医院彩超检查子宫肌瘤20--15... 预约挂号,门诊就诊总交流次数1已给处置建议
- 小细胞肺癌,化疗两次,月经淋漓不尽 肿瘤医院确诊小细胞肺癌,化疗两次,月经淋漓不尽,第一次去省妇... 肿瘤期间月经的问题,止血总交流次数4已给处置建议
- 患者:女 49岁 子宫内膜癌 最后交流时间 2022.06.18子宫内膜癌 子宫内膜癌,伴有出血,上个月月底查出来的,想来太原总交流次数2已给处置建议
- 宫颈癌术后 我妈妈宫颈癌术后五年了,今天复查做b超,别的都正常总交流次数2已给处置建议



