科室医生 查看全部
按疾病推荐专家 查看全部
科普·直播义诊专区 查看全部
- 骨科快速康复的领域
一、加速康复在关节骨科中的应用 随着世界人口老龄化的进程,关节置换术在全世界呈逐年上升趋势,据研究报道,至2030年,美国地区每年选抨行初次全髋关节置换术病人将比2005年增加174%达57万人, 选择行初次全膝关节置换术将增加673%达348万人。传统髋、膝关节置换术后病人的平均住院日为5 ~7天,Meyers的研究曾指出随着平均住院日的缩短,将导致术后并发症发生率的增高。出于对此种情况的顾虑,医疗花费的控制主要集中于减少植入假体的费用,然而,医疗改革提出的医疗质量控制强调在减少医疗费用的同时,提高病人的就医满意度。因此,如何优化疾病诊治过程中的各个环节,在提高病人满意度、减少住院时间的同时,不增加术后并发症的发生率成为一个亟须考虑和解决的问题。 加速康复外科在髋、膝关节置换术中的成功应用,使得这一问题得以解决。各种微创理念与优化手术操作技术的兴起,关节外科医师更加注重在手术过程中尽量减少剥离,避免软组织损伤;各种新型手术入路及器械的发明,使得真正的肌肉间隙人路成为可能。同时,选择行关节置换手术病人多为老年甚至卨龄病人,术前多并存一种或多种内科疾病;而术前正确的评估与处埋,可提高病人对手术打击的耐受力,同时也是保证手术安全的前提。另一方面,髋、膝关节置换手术出血量较大,术前术后疼痛反应明显,睡眠质量较差,完善的围术期血液管理、疼痛管理、睡眠管理,可降低手术应激,加快术后关节功能恢复,缩短住院时间,提高病人满意度,术后静脉血栓栓塞症、感染、脱位是髋膝关节置换术后的主要并发症,有效的围术期预防可显著降低术后再入院率。 因此,加速康复在关节置换术中的实施涉及到术前、术中、术后的方方面而,同时在实施过程中需要关节外科医师、内科医师、麻醉医师、护十、物理治疗师、心理治疗师等多个学科 的联合与配合。关于加速康复在关节置换术围术期的具体实施措施及方法,后续章节将逐一详细介绍,在此不再赘述。 在骨科的各个亚专业中,加速康复在关节骨科中的应用较早且较成熟。其临床应用效果也获得了较多的循证医学证据支持。Auyong等学者通过对比实施ERAS路径前后的病人数据,结果发现实施ERAS路径后,平均住院从76.6小时降低至56.1小时,术后30天再入院率从5.6%降低至2.4%,术后疼痛反应更轻,阿片类药物使用更少,术后功能恢复更好。加速康复关节外科在减少平均住院日的同时,另一重要目的在于改善病人围术期的主 观体验(free of risk),提高病人满意度。Jones通过对8项临床研究进行系统评价后指出, ERAS髋、膝关节置换术后病人的生活质量(QOL)及病人满意度均较传统关节置换术后病人 高。但尚缺乏统一的定量评价标准,且国内尚缺乏相关研究。华西匡院骨科自2016年以来有101例全髋关节置换术病人严格执行ERAS措施,平均术后住院时间从以往的4. 7天缩短到3.2 天,且52例病人(51. 5% )术后住院时间≤48小时,具休的加速康复流程管理可参见以下内容。 二、加速康复在脊柱骨科及创伤骨科中的说用 与关节置换术相比,ERAS在脊柱骨科及创伤骨科中的探索仅限于特定的疾病种类及于手术方式中;其原因在于脊柱手术方式多变,手术时间较长,术后疼痛重且卧床时问长,创伤手术有其急诊性质也限制了 ERAS的应用。Wainwright等学者通过严谨、广泛的文献检索后发现,目前仅有四篇文献简单报道了 ERAS在脊柱手术病人屮的应用经验,其中三篇仅报道了单一的微创手术方式、多模式镇痛及恶心、呕吐管理、血液管理在促进术后病人康复中的作用,仅有一篇文献报道了联合应用术前宣教、早期下床活动、术后自我评判式康复锻炼及早期出院标准的REAS方案在退变性脊柱滑脱病人中的应用效果,研究结果也发现实施ERAS方案后,平均住院日降低了4.7天,基于有限的循证医学证据,笔者也认为ERAS在脊柱手术中的应用仍有待进一步深入研究,同时也应针对不同的疾病种类及手术方式制定更加细化的ERAS方案,但是,ERAS在脊柱手术屮是有效的,至少目前的证据支持在适当的病人中联合应用术前宣教、多模式疼痛管理、血液管理、早期活动及制定出院标准与康复方案将有助于加速病人术后功能康复。 据2014年一项《近十年我国各地区骨质疏松症流行病学状况》报告,目前我国60岁以上的老年人已达3亿,全国40岁以上的骨质疏松病人已达到1.12亿。骨质疏松病人易发生跌倒,导致骨折,其中以髋部骨折多见。国际骨质疏松基金会(IOF)报告也指出,在2010 年,中国50岁及以上的人口中发生了大约230万例骨折,这数字预计将在2050年上升到600万例。英国国家髋部骨折数据库显示,髋部骨折手术病人的平均住院日为( 19.5 ± 4.9) 天。因此,有效的实施ERAS以减少住院日将有重大意义。目前关于ERAS、在髋部骨折病人的临床应用研究较少,暂无统一的ERAS方案,有待进一步研究。但髋部骨折病人与关节置换术病人类似,多为老龄人,并存疾病较多;且髋部骨折病人术前即存在明显隐性失血,术前需卧床,发生贫血、营养不良、肺部感染、尿路感染、静脉血栓栓塞症等并发症的风险较高。 因此,笔者认为除了关节置换术ERAS方案外,髋部骨折病人ERAS的成功实施需更多关注 营养支持、血液管理、早期活动及并发症预防。
姚保平 副主任医师 甘肃成县人民医院 骨科2581人已读 - 中暑的治疗
中暑了,怎么办?可以这样治疗: 1.停止活动并在凉爽、通风的环境中休息。脱去多余的或者紧身的衣服。 2.如果患者有反应并且没有恶心呕吐,给患者喝水或者运动饮料。也可服用藿香正气水等中药。 3.让患者躺下,抬高下肢15~30cm。 4.用湿的凉毛巾放置于患者的头部和躯干部以降温,或将冰袋置于患者的腋下、颈侧和腹股沟处。 5.如果30分钟内患者情况没有改善,寻求医学救助。如果患者没有反应,开放气道,检查呼吸并给予适当处置。 6.对于重症高热患者,降温速度决定预后。体温越高,持续时间越长,组织损害越严重,预后也越差。体外降温无效者,用4℃冰盐水进行胃或直肠灌洗,也可用4℃的5%葡萄糖盐水或生理盐水1000~2000ml静脉滴注,既有降温作用,也适当扩充容量,但开始速度宜慢,以免引起心律失常等不良反应。 7.严重的中暑,就叫热射病,必要时,需行床旁血液净化治疗。 8.加强监测和对症治疗。
刘斌 主治医师 甘肃成县人民医院 骨科1223人已读 - 骨质疏松性骨折诊疗指南(2017年)
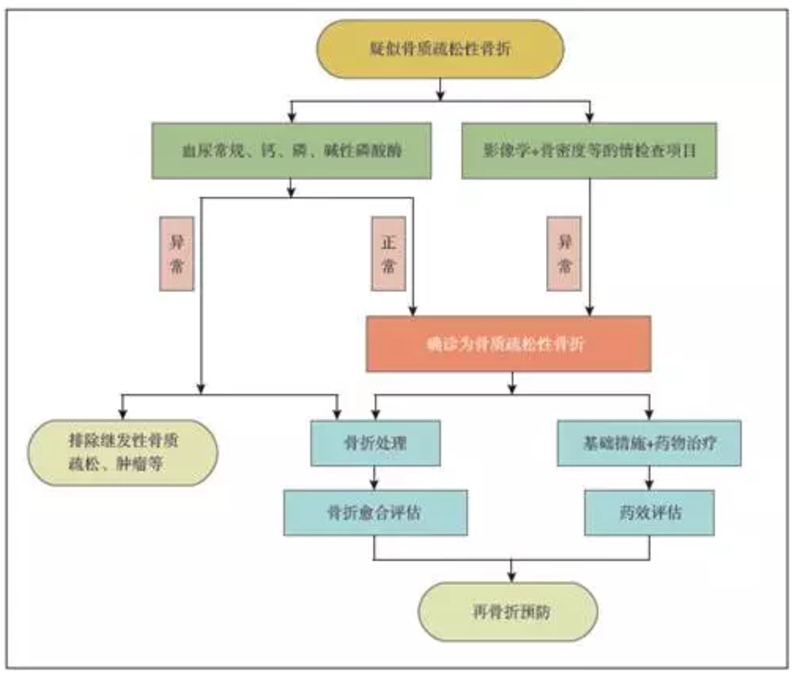
骨质疏松性骨折是中老年最常见的骨骼疾病,也是骨质疏松症的严重阶段,具有发病率高、致残致死率高、医疗花费高的特点。而我国骨质疏松性骨折的诊疗现状是诊断率低、治疗率低、治疗依从性和规范性低。2008年,中华医学会骨科学分会发布了《骨质疏松骨折诊疗指南》,对我国骨质疏松性骨折的诊断及治疗起到了巨大的指导和规范作用。 为了及时反映当今骨质疏松性骨折手术和药物治疗的新理念和循证医学进展,优化骨质疏松性骨折诊疗策略,规范骨科医生诊疗行为,自2015年5月开始,中华医学会骨科学分会骨质疏松学组及《中华骨科杂志》编辑部组织国内本领域的专家,针对原指南的不足,参考近年来国内外对骨质疏松性骨折防治的指南,遵循科学性、实用性和先进性的原则,对原指南进行更新。 一、定义 (一)骨质疏松性骨折 为低能量或非暴力骨折,指在日常生活中未受到明显外力或受到"通常不会引起骨折外力"而发生的骨折,亦称脆性骨折(fragility fracture)。"通常不会引起骨折外力"指人体从站立高度或低于站立高度跌倒产生的作用力。骨质疏松性骨折与创伤性骨折不同,是基于全身骨质疏松存在的一个局部骨组织病变,是骨强度下降的明确体现,也是骨质疏松症的最终结果。 (二)骨质疏松症(osteoporosis, OP) 以骨强度下降、骨折风险增加为特征的骨骼系统疾病。骨强度反映骨骼的两个主要方面,即骨密度和骨质量。 骨质疏松症分为原发性和继发性两大类。本指南仅针对原发性骨质疏松症导致的骨质疏松性骨折而制定。 二、流行病学及其特点 2013年国际骨质疏松基金会(International Os?teoporosis Foundation,IOF)报告:全球每3 秒钟有1例骨质疏松性骨折发生,约50%的女性和20%的男性在50岁之后会遭遇初次骨质疏松性骨折,50%初次骨质疏松性骨折患者可能会发生再次骨质疏松性骨折;女性骨质疏松性椎体骨折再骨折风险是未发生椎体骨折的4倍。骨质疏松性骨折可造成疼痛和重度伤残,髋部和椎体发生骨质疏松性骨折可降低患者预期寿命,长期卧床者的致死率可达20%、永久性致残率可达50%。 骨质疏松性骨折具有以下特点:①骨折患者卧床制动后,将发生快速骨丢失,会加重骨质疏松症;②骨重建异常、骨折愈合过程缓慢,恢复时间长,易发生骨折延迟愈合甚至不愈合;③同一部位及其他部位发生再骨折的风险明显增大;④骨折部位骨量低,骨质量差,且多为粉碎性骨折,复位困难,不易达到满意效果;⑤内固定治疗稳定性差,内固定物及植入物易松动、脱出,植骨易被吸收;⑥多见于老年人群,常合并其他器官或系统疾病,全身状况差,治疗时易发生并发症,增加治疗的复杂性。 骨质疏松性骨折多见于老年人群,尤其是绝经后女性。发生的常见部位有:胸腰段椎体、髋部(股骨近端)、腕部(桡骨远端)、肱骨近端等;发生了脆性骨折临床上即可诊断骨质疏松症。 三、骨质疏松性骨折的诊断 (一)临床表现 可有疼痛、肿胀和功能障碍,可出现畸形、骨擦感(音)、反常活动;但也有患者缺乏上述典型表现。具有骨质疏松症的一般表现。 (二)影像学检查 1.X线:可确定骨折的部位、类型、移位方向和程度,对骨折诊断和治疗具有重要价值。X线片除具有骨折的表现外,还有骨质疏松的表现。 2.CT:常用于判断骨折的程度和粉碎情况、椎体压缩程度、椎体周壁是否完整、椎管内的压迫情况。 3.MRI:常用于判断椎体压缩骨折是否愈合、疼痛责任椎及发现隐匿性骨折,并进行鉴别诊断等。 4.全身骨扫描(ECT):适用于无法行MR检查或排除肿瘤骨转移等。 (三)骨密度检查 拟诊为骨质疏松性骨折的患者建议行骨密度检查。双能X线吸收法(dualenergy X-ray absorpti?ometry, DXA)测量值是世界卫生组织(World Health Organization,WHO)推荐的骨质疏松症评估方法,是公认的骨质疏松诊断的金标准。 参照WHO推荐的诊断标准,DXA测定骨密度值低于同性别、同种族健康成人的骨峰值不足1个标准差为正常(T值≥-1.0 SD);降低1~2.5个标准差为骨量低下或骨量减少(-2.5 SD< T值40%)。引起疼痛的骨折椎体即为疼痛责任椎体,可根据骨折节段局部的压痛、叩击痛,结合MRI或ECT结果综合判断。 2. 治疗 (1)非手术治疗 适用于症状和体征较轻,影像学检查显示为轻度椎体压缩骨折,或不能耐受手术者。治疗可采用卧床、支具及药物等方法,但需要定期进行X线片检查,以了解椎体压缩是否进行性加重。 (2)手术治疗 椎体强化手术,包括椎体成形术(PVP)和椎体后凸成形术(PKP),是目前最常用的微创手术治疗方法,适用于非手术治疗无效,疼痛剧烈;不稳定的椎体压缩性骨折;椎体骨折不愈合或椎体内部囊性变、椎体坏死;不宜长时间卧床;能耐受手术者。高龄患者宜考虑早期手术,可有效缩短卧床时间,减少骨折并发症的发生。绝对禁忌证:不能耐受手术者;无痛、陈旧的骨质疏松性椎体压缩性骨折;凝血功能障碍者;对椎体成形器械或材料过敏者。相对禁忌证:椎体严重压缩性骨折,椎管内有骨块;有出血倾向者;身体其他部位存在活动性感染者;与椎体压缩骨折无关的神经压迫引起的根性痛。 术中应避免发生骨水泥渗漏,必要时可选用网袋技术或遥控骨水泥注射技术加以预防。另外,术中还可以同时取活检,以便与肿瘤引起的脊柱压缩性骨折进行鉴别。 对有神经压迫症状和体征、严重后凸畸形、需行截骨矫形以及不适合行微创手术的不稳定椎体骨折患者,可考虑行开放手术治疗。术中可采用在椎弓根螺钉周围局部注射骨水泥、骨水泥螺钉、加长和加粗椎弓根钉或适当延长固定节段来增强内固定的稳定性。 (二)髋部骨折 1.诊断 骨质疏松性髋部骨折主要包括股骨颈骨折和转子间骨折,是骨质疏松症最严重并发症,具有致畸率、致残率高、病死率高、恢复缓慢的特点,骨折后第1年内的死亡率高达20%~25%,存活者中超过50%的患者会留有不同程度的残疾。根据临床表现和影像学可明确诊断。治疗骨质疏松性髋部骨折的目的是尽快采取有效的措施,恢复患者的负重功能,减少卧床时间。 2.治疗 (1)股骨颈骨折:常采用Garden分型评估骨折的稳定性和移位程度。老年骨质疏松性股骨颈骨折推荐尽早手术治疗,包括闭合或切开复位内固定术、人工关节置换术等。对于骨折移位不明显的稳定型骨折或合并内科疾病无法耐受手术者,可以酌情采用外固定架或非手术治疗。 选择人工股骨头置换还是人工全髋关节置换,主要根据患者的年龄、全身状况、预期寿命等因素来决定。对高龄、全身情况较差、预期寿命不长者,可考虑行人工股骨头置换,以缩短手术时间,减少术中出血,满足基本的日常生活要求;否则行人工全髋关节置换术。 (2)股骨转子间骨折:常采用Evans分型和AO分型。目前,主要治疗手段是闭合或切开复位内固定,包括髓内和髓外固定。从生物力学角度,髓内固定更具优势。人工髋关节置换不作为转子间骨折的常规治疗方法,仅当作一种补充手段。 (三)桡骨远端骨折 1.诊断 根据病史、体检及X线检查基本可作出诊断。桡骨远端骨质疏松性骨折多为粉碎性骨折,易累及关节面,骨折愈合后常残留畸形和疼痛,造成腕关节和手部功能障碍,屈伸和旋转受限。 2.治疗 对于可恢复关节面平整及正常掌倾角和尺偏角、能够恢复桡骨茎突高度者,可采用手法复位、石膏或小夹板外固定等非手术治疗。 对累及关节面的桡骨远端粉碎性骨折、不稳定的桡骨远端骨折、手法复位后桡骨短缩超过3 mm、侧位X线片示背侧成角超过10°、关节面台阶超过2 mm、手法复位不满意者可采用手术治疗,目的是恢复关节面的平整及相邻关节面的吻合关系,重建关节的稳定性以及恢复无痛且功能良好的腕关节。手术方法可根据骨折的具体情况选择,包括经皮撬拨复位克氏针内固定、外固定支架固定、切开复位钢板内固定、桡骨远端髓内钉固定等。 (四)肱骨近端骨折 1.诊断 肱骨近端骨质疏松性骨折,因骨质条件欠佳而常导致复位和固定困难,尤其是粉碎性骨折,可出现肱骨头坏死、肩关节脱位或半脱位,严重影响关节功能。临床可根据X线检查判断骨折类型,通过CT扫描明确主要骨块移位及压缩程度,而MRI则有助于判断肩袖损伤。 2.治疗 无移位的肱骨近端骨折可采用非手术治疗,方法为颈腕吊带悬吊、贴胸位绷带固定或肩部支具固定等。有明显移位的肱骨近端骨折建议手术治疗,可根据患者具体情况采用闭合或切开复位内固定。内固定可选择肱骨近端解剖型钢板、锁定钢板、肱骨近端髓内钉等。克氏针、螺钉、张力带固定操作简便,对组织损伤小。对肱骨近端Neer分型三或四部分的严重粉碎性高龄骨折患者,可考虑行人工肱骨头置换术。 六、骨质疏松性骨折药物干预 (一)干预目的 骨质疏松性骨折的病理基础是骨质疏松,骨折后应积极采用规范的抗骨质疏松药物治疗,其目的是缓解疼痛,抑制急性骨丢失,提高骨量,改善骨质量,降低再骨折发生率。 (二)干预药物 1.基础药物 (1)钙剂,可改善骨矿化、减缓骨量丢失。 (2)维生素D,可促进钙吸收,有利于骨骼健康、增加肌力、降低再骨折风险。 钙剂和维生素D可与抗骨质疏松药物联合使用,并贯穿整个治疗过程。 2.抗骨质疏松药物 (1)抑制骨吸收类药物 ①双膦酸盐类:可提高腰椎和髋部骨密度,降低椎体及髋部等部位再骨折发生率;主要包括阿仑膦酸钠、利塞膦酸钠、唑来膦酸(5mg;注意4mg剂量唑来膦酸无临床适应证,仅用于治疗转移性肿瘤)、伊班膦酸钠。 ②选择性雌激素受体调节剂(SERMs):可选择性地作用于雌激素的靶器官,与不同形式的雌激素受体结合,发生不同的生物效应,降低骨转换至女性绝经前水平,阻止骨丢失,增加骨密度。 ③降钙素类:可抑制破骨细胞生物活性、减少破骨细胞数量,对骨质疏松性骨折后的急性骨丢失和疼痛有较好的治疗作用;主要包括鲑鱼降钙素、鳗鱼降钙素等。 ④雌激素:能抑制骨转换、阻止骨量丢失,可提高椎体和髋部骨密度。绝经后骨质疏松性骨折患者建议在专科医生指导下个体化运用。 (2)促进骨形成类药物 重组人甲状旁腺激素片段1?34(rhPTH1?34),具有增加成骨细胞分泌胶原、促进骨基质形成及其矿化、促进骨形成、改善骨重建的作用,可有效增加骨密度,显著降低绝经后妇女椎体和非椎体骨折风险。 (3)活性维生素D类 主要包括骨化三醇及其类似物——阿法骨化醇,适用于绝经后骨质疏松症,但不推荐作为日常补充。老年人、肾功能不健全及1α羟化酶缺乏患者建议补充活性维生素D。 (4)维生素K类 四烯甲萘醌可促进骨形成、抑制骨吸收、提高骨量,可降低骨质疏松性骨折再骨折发生率。 (5)中成药 人工虎骨粉、异黄酮类及淫羊藿类复合物等中成药对骨质疏松性骨折患者有减轻疼痛、提高骨密度的疗效。 需要强调的是,不推荐同时联合应用同一作用机制的抗骨质疏松药物。 (三)干预原则 骨质疏松性骨折抗骨质疏松药物干预需要根据骨质疏松严重程度,注重个体化原则,考虑药物的适应证和禁忌证、临床疗效、安全性、经济性和依从性等诸多因素,合理应用。 1.骨质疏松性骨折后,早期钙和维生素D用药剂量可酌情增加;钙剂应注重元素钙含量,推荐补充元素钙1000 mg/d;普通维生素D补充剂量推荐为800IU/d。 2.骨质疏松性骨折发生前,已使用抗骨质疏松药物者,应重新评估骨质疏松状况,不建议盲目停药。 3.骨质疏松性骨折发生前,未使用抗骨质疏松药物者,应在骨折处理后,患者全身情况稳定时,尽早使用抗骨质疏松药物治疗。 4.骨质疏松性骨折后,规范的双膦酸盐使用对骨折愈合无不利影响。双膦酸盐使用应参考下列情况。 (1)双膦酸盐类药物联合钙和维生素D应用,可提高抗骨质疏松疗效。 (2)口服双膦酸盐类药物,禁用于导致食管排空延迟的食管异常(狭窄或迟缓不能)、不能站立或坐直至少30min者、对产品任何成分有过敏者、低钙血症。 (3)静脉注射双膦酸盐类药物时,少数患者可能会出现一过性发热反应,建议在静脉使用双膦酸盐类药物的同时,选用非甾类抗炎药物5~7d。 (4)当患者肌酐清除率低于35ml/min时,静脉双膦酸盐禁用,口服双膦酸盐不推荐使用。 5.骨质疏松性骨折属于骨质疏松严重阶段,下列情况是使用促骨形成类药物的参考条件。 (1)对已使用抗骨吸收药物治疗多年而发生骨质疏松性骨折患者,建议停用抗骨吸收类药物,选用促骨形成类药物。 (2)65岁以上女性骨质疏松性椎体骨折且骨密度低于-2.5 SD、绝经后女性多次发生骨质疏松性椎体骨折或髋部骨折、运用双膦酸盐后仍发生骨质疏松性骨折的患者,推荐使用促骨形成药物。 (3)多发性骨质疏松性骨折患者,可以使用促骨形成药物。 6.降钙素对缓解骨质疏松性骨折骨痛有益,可减少骨折后急性骨丢失,建议在骨质疏松性骨折的制动患者中短时间(3个月)使用。 7.对围绝经期骨质疏松性骨折患者,更年期症状(血管舒缩症状)明显,可选用雌激素;无明显更年期症状,可选用选择性雌激素受体调节剂(SERMs);需在专科医生指导下使用。 8.骨质疏松性骨折后抗骨质疏松治疗,应注重长期干预,通常在骨折愈合后还需坚持定期随访,提高药物干预的依从性。 (四)干预对骨折愈合和内植物影响 骨质疏松性骨折后,应用钙剂和活性维生素D可提高患者成骨活性指标,增加骨痂面积。应用双膦酸盐会出现骨痂增大、矿化增加,未见骨折延迟愈合;使用rhPTH1?34,可促进骨折区骨痂形成。 骨质疏松性骨折内固定手术后,应用双膦酸盐类药物可抑制骨量的进一步丢失,提高内固定物的稳定性,降低内固定移位的发生率。 骨质疏松性髋部骨折人工关节置换术后,应用双膦酸盐类药物可提高髋部骨量,减少假体周围骨丢失,降低假体松动发生率。 骨质疏松性椎体骨折内固定术后,应用rhPTH1?34可提高椎体骨量,降低椎弓根螺钉松动的发生率。 (五)干预注意事项 1.干预疗程 双膦酸盐类药物疗程一般为3~5年,而后再根据治疗后骨代谢指标改变、再骨折风险程度改变决定"继续用药"或"停药观察(药物假期)"。rhPTH1?34使用不超过2年。 激素类和生物制剂类药物一旦停用,其疗效即消退,需序贯其他治疗。雌激素和选择性雌激素受体调节剂尚无明确疗程限定,使用时间可根据治疗效果确定。 2.随访和评估 (1)使用抗骨质疏松药物干预后,应保持定期随访,了解并处理不良反应、骨折愈合情况、临床症状改善情况、再骨折预防实施情况等。 (2)抗骨质疏松治疗效果,早期可观察骨转换指标,如P1NP和S?CTX的改变,并帮助提高干预依从性。抗骨质疏松治疗1年后,可比较双能X线骨密度是否超过最小有意义变化值,以评估疗效。 3.药物转换 对于确定治疗无效患者,IOF专家组提出的药物转换原则可供参考:转换为更强效的同一类型抗骨吸收的药物;口服剂型药物转换为注射剂型药物;抗骨吸收类药物转换为促骨形成类药物。 七、术后再骨折风险评估及处理 (一)骨质疏松性骨折术后再骨折风险评估 骨质疏松性骨折术中及术后仍然存在发生骨折风险,甚至更高,因此骨折风险评估对骨质疏松性骨折的治疗和预防有重要的意义。 骨密度是经典的骨质疏松性骨折风险预测因素,其代表70%的骨强度,骨密度每下降1个标准差,被检测的骨骼区域骨折风险增加1.5~3.0倍。骨小梁结构和骨转换对骨强度也有重要意义。此外,高龄、女性等因素与再骨折风险相关。肌少症在骨质疏松和骨质疏松性骨折发病中的作用逐渐受到重视,肌力和平衡能力评定有助于评估跌倒风险。 抗骨质疏松治疗,包括药物治疗及功能锻炼,有助于降低再骨折风险。 (二)骨质疏松性骨折术后再骨折处理 骨质疏松性骨折后再骨折既可以发生于原有骨折部位,也可以发生于其他部位。对于骨质疏松性骨折术后再骨折,尤其应该重视局部和全身的抗骨质疏松治疗。骨质疏松性骨折术后原位再骨折则常与骨折不愈合或延迟愈合有关,需要根据具体原因选择保守治疗、增加或更换内固定、植骨甚至关节置换手术。 八、康复与并发症预防 骨质疏松性骨折,尤其是脊柱和髋部骨折,常见的并发症包括静脉血栓形成、肺部感染、褥疮、泌尿系感染、心脑血管意外等,严重者甚至可导致死亡,远期还可能残留疼痛和肢体功能障碍。除与相关专业医生协作开展并发症防治外,骨折后及手术后尽早指导患者进行适当的康复锻炼,对于并发症的预防和骨折远期疗效的提高有重要帮助。 骨质疏松性骨折患者的康复治疗既要遵循一般骨折的康复规律,又要考虑到患者骨质量差和骨折愈合缓慢的特点,可根据具体情况采用多种康复措施,例如:疼痛管理、饮食及生活习惯指导、运动康复、康复辅具的使用、骨质疏松健康知识教育、中医药康复等,可在康复科医生协助下完成。 (一)围手术期康复与并发症预防 对于脊柱和髋部骨折,在内固定或关节置换术基础上,应鼓励患者在医护人员的指导下尽早坐起和站起,以缩短卧床时间,减少卧床相关并发症的发生。髋部骨折术后宜循序渐进地进行关节功能的主动活动和被动运动,尤其是患肢主动活动。采用髓内固定或关节置换的患者,术后可尽早尝试患肢部分负重;采用锁定钢板等髓外固定技术的患者,患肢下地负重时间需适当推迟;关节置换术后早期,应根据采用的手术入路,适当限制关节活动范围;椎体成形术后12h,患者可尝试坐起,24h后可尝试站立,腰背部肌肉力量训练和平衡训练有助于加速患者恢复。 桡骨远端骨折内固定术后或拆除外固定后,应重视关节活动度、肌肉力量等康复训练。肩关节骨折后的康复训练通常由被动运动开始,可在上肢吊带或外展架上行前屈、外旋运动,待疼痛缓解后,逐步开始行主动肌力锻炼和关节活动度训练等。 (二)围手术期后的康复 围手术期后的康复措施主要包括运动康复、物理疗法和个性化的康复辅具,这些康复措施有助于改善骨折后残留的肢体疼痛、肿胀及功能障碍,增加骨强度,改善肢体协调性以避免跌倒,提高患者生活质量。 本指南仅为学术性指导意见,随着医学的发展,其中的某些内容需不断完善,临床实施方案必须依据临床具体情况制定,采取各种预防及治疗措施前,请参阅相关产品说明。
 姚保平 副主任医师 甘肃成县人民医院 骨科1184人已读
姚保平 副主任医师 甘肃成县人民医院 骨科1184人已读
总访问量 180,960次
在线服务患者 77位
科普文章 9篇






