科室介绍 查看全部
科室医生 查看全部
科普·直播义诊专区 查看全部
- 精选 晚期胆管癌的介入治疗新模式
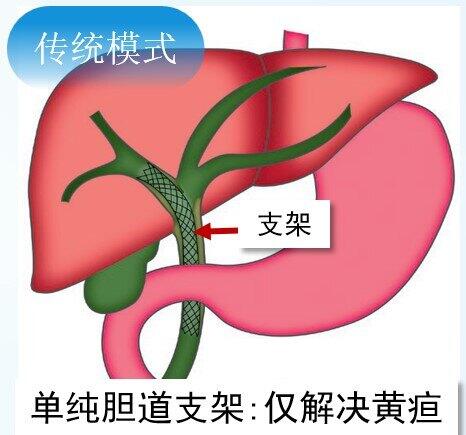
多数胆管癌患者在确诊时处于中晚期,只有约10%的病人有手术机会。而对于不可切除的胆管癌患者,传统的一线治疗为全身静脉化疗,但治疗缓解率低,生存获益不佳,且有些患者不能耐受。介入治疗,作为一种微创治疗手
 周卫忠 副主任医师 江苏省人民医院 介入放射科1528人已读
周卫忠 副主任医师 江苏省人民医院 介入放射科1528人已读 - 精选 肝癌治疗新技术分享
肝癌治疗新技术分享TAHA结合免疫治疗晚期HCC病例CASE Report/ 病例分享晚期HCC病例:第一次治疗前左右肝脏广泛性病变 如图1患者,男,因腹胀、腹痛检查发现肝占位入院治疗。如上图为DSA实质期照片,可以非常直观地看到左右几乎占据全部肝脏的肝癌多发性病灶。采用肝脏化学消融治疗,以最大限度保护残余肝脏的结构和功能。术后配合免疫等综合治疗处理。第一次治疗1月后CT 随访所有病灶均有一定程度退缩。如上腹部CT所示(图2)图2 上腹部CT 平扫肝内左右泛发性病变以明显缩小,病人临床症状大幅改善。经过3次治疗,4月后随访观察,病人病灶缩小、灭活85%以上,临床恢复很好,症状明显改善、精神好转,且体重增加。客观影像资料显示,治疗效果介于CR和PR之间,收到既往类似患者少见的临床疗效。4月随访DSA如图3 照片 所示:DSA表现为供血动脉变细,左右肝脏内的肿瘤明显缩小,并且是肿瘤组织坏死,在DSA的影像上可以看见没有肿瘤染色,提示病理上肿瘤组织液化坏死,失去活力。这种肿瘤组织液化坏死,失去活力除了病理检查可以直观看见以外,上面的DSA血管造影可以提示,无创的MRI即磁共振同样可以证明肿瘤组织的生存情况。图4 是患者4月后的磁共振随访照片。上述病例显示新的消融免疫治疗方法,除了在早期、中期肝癌能够取得和外科手术切除同样的效果、来减少患者痛苦外,对于中期和晚期,特别在此强调的甚至部分像上面外科和其他手段都无法实施的病人,也能够取得临床很好的疗效。因此,在此特别报道,借助好大夫在线这一好的平台,具体介绍上述典型患者,以造福相关病员!
王杰 主任医师 江苏省人民医院 介入放射科1489人已读 - 精选 肝动脉化疗栓塞联合微波消融与外科根治性切除治疗小肝癌的对照研究
【摘要】 目的 比较肝动脉化疗栓塞联合微波消融(TACE-MWA)与外科根治性切除(SR)治疗小肝癌的临床疗效。材料和方法 回顾性分析2010年1月至2017年12月期间在我院行TACE-MWA或SR治疗的199例小肝癌患者的临床资料。TACE-MWA与SR治疗的患者按1:2行倾向性匹配,分析两组术后的无疾病生存率(DFS)和总体生存率(OS)。结果 匹配后共纳入患者72例(TACE-MWA组24例,SR组48例)。所有患者平均随访时间29.2个月(TACE-MWA:26.1个月;SR:30.8个月)。TACE-MWA组和SR组的1年、2年和3年的DFS分别为78.8%、78.8%、56.2%和91.7%、71.9%、62.5%。TACE-MWA组和SR组的1年、2年和3年的OS分别为100%、95.5%、95.5%和100%、97.5%、97.5%。两组间的DFS和OS均无明显统计学差异(P=0.730和P=0.648)。结论 与SR相比,TACE-MWA治疗小肝癌的DFS与OS均无明显统计学差异。TACE-MWA可以成为治疗小肝癌的一种有效模式。【关键词】小肝癌;肝动脉化疗栓塞;微波消融;外科切除Comparison Study of Transarterial Chemoembolization Combined with Microwave Ablation versus Surgical Resection for the Treatment of Small Hepatocellular CarcinomaGUO Weiping, WANG Jie, GUAN Yiwei, ZHANG Jinxing, ZU Qingquan, SHI Haibin. Department of Interventional Radiology, The First Affiliated Hospital with Nanjing Medical University, Nanjing 210029, ChinaCorresponding author: WANG Jie, E-mail: wangjie_jsph@189.cn【Abstract】 Objective: To compare the effectiveness of transarterial chemoembolization combined with microwave ablation (TACE-MWA) with surgical resection (SR) for the treatment of small hepatocellular carcinoma (HCC). Materials and Methods: From January 2010 to December 2017, the clinical data of 199 patients with small HCC, who were treated by TACE-MWA or SR in our hospital, were studied retrospectively. Patients who were treated by TACE-MWA and SR were propensity score matched (1:2 ratio). Disease-free survival (DFS) rates and overall survival (OS) rates were recorded and analyzed after treatment. Results: After progression matching, 72 patients were included (TACE-MWA group: 24 patients; SR group: 48 patients). Mean follow-up period was 29.2 months (TACE-MWA group: 26.1 months; SR group: 30.8 months). The 1-, 2-, and 3-year DFS rates were 78.8%, 78.8%, and 56.2% for TACE-MWA group and 91.7%, 71.9%, and 62.5% for SR group, respectively. The 1-, 2-, and 3-year OS rates were 100%, 95.5%, and 95.5% for TACE-MWA group and 100%, 97.5%, and 97.5% for SR group, respectively. There was no statistically significant difference in DFS rates and OS rates between groups (P=0.730 and P=0.648). Conclusions: Compared with SR, there was no statistically significant difference in DFS rates and OS rates of TACE-MWA in the treatment of small HCC. It seemed that TACE-MWA was an effective treatment model for small HCC.【Key words】Small hepatocellular carcinoma; Transarterial chemoembolization; Microwave ablation; Surgical resection随着影像学和血清学检查的进步,已经能够对一大部分小肝癌做出早期诊断[1]。这些肝癌患者可以选择肝移植、肝切除、消融等治疗方式[2]。肝移植可以获得更好的生存时间,但肝源的长期等待时间却限制了其成为早期肝癌的一种常规治疗选择[3]。相比之下,外科切除(SR)则被认为是早期肝癌患者的一线治疗方案[4]。但是近年来微波消融(MWA)由于具有肿瘤坏死率高、创伤小、费用低等优势,在小肝癌的治疗上取得了较好的进展,尤其适用于肝功能代偿差或一般情况不佳而不能耐受手术切除的患者[5]。理论上,MWA可以使肿瘤细胞达到完全性坏死,但形成的坏死区域相对较小[6]。另外,在肝硬化基础上衍生的小肝癌,尚有一些伴发的微病灶未能被显示。肝动脉化疗栓塞联合微波消融(TACE-MWA)首先通过向肿瘤供血动脉注射化疗栓塞物质,达到诊断和治疗的双重目的,也可以减少微波加热过程中血液流动所带来的冷却效应,从而加强消融肿瘤的凝固效应[7-8]。因此,本研究回顾性分析了我院TACE-MWA与SR治疗小肝癌的临床数据,通过倾向性匹配从而减少非随机化设计所带来的潜在偏倚,比较两者术后无疾病生存率(DFS)和总体生存率(OS)之间的差异。1 材料与方法1.1 患者纳入此次回顾性研究的数据是来自2010年1月至2017年12月期间,在我院以TACE-MWA或SR作为初始治疗的HCC患者。我们仍然推荐SR作为患者的一线治疗方案。对于那些由于高龄、严重肝硬化及主观因素不适合或拒绝手术切除的患者,TACE-MWA的联合治疗作为二线方案。患者纳入的标准为:(a)单病灶直径或双病灶直径之和≤3cm;(b)Child-Pugh(CP)Class A / B。排除标准包括:(a)有血管侵入或远处转移;(b)伴有其他恶性肿瘤病史;(c)TACE-MWA或SR初始治疗前,又行其他抗肿瘤治疗;(d)失访或数据不全。由于TACE-MWA组的病例数明显少于SR组,为了减少非随机研究设计所带来的潜在偏移,按照1:2对TACE-MWA组和SR组的病例进行倾向性匹配(图1)。所有患者随访至死亡或至2018年12月。此次研究经我院伦理审查委员会批准。1.2 TACE-MWA与SRTACE-MWA:采用Seldinger技术穿刺右侧股动脉,将5F鞘引入股动脉后,将5F导管插至腹腔动脉、肝固有动脉及肠系膜动脉行血管造影,评估肿瘤的位置、大小、数量、血供等。后将2.7F微导管超选至肿瘤供血动脉。根据患者肝功能和肿瘤直径,通过微导管注入超液化碘油(3-6mL)与表柔比星(10mg)制成的混合乳剂,达到门静脉亚段分支显影后,再以适当的明胶海绵颗粒栓塞病灶供血动脉至血流停止。TACE治疗后的2-4周患者复查腹部CT评估病灶,并行MWA治疗。使用南京亿高(ECO)公司生产的多功能微波治疗仪,输出频率2450±50MHz,输出功率0-100W,逐级可调,连续输出。根据术前CT选定穿刺点及穿刺路径,麻醉监护下,透视或CT引导下穿入微波针,穿过病灶中心并突破病灶对侧缘。将微波针通过电缆线与输出主机连接,打开冷水循环系统。根据病灶直径设定输出功率及消融时间,要求凝固范围超出病灶边缘5-10mm[9],开始行消融治疗。消融结束后退出微波针,并灼烧穿刺道。术后予以心电监护、保肝等对症治疗。SR:常规术前准备,全身麻醉后,行病灶肝段或亚段切除。切除前常规行超声检查再次确定病灶位置、切除范围及肝内血管结构。1.3 随访术后每隔1-3个月行CT或MRI检查以此评估治疗后是否存在残留或复发肿瘤。通过影像学检查、门诊或电话随访等确定复发时间、生存期。无疾病生存期定义为术后至发现肝内或肝外肿瘤复发、末次随访的时间。生存期定义为术后至死亡或末次随访的时间。对于残留或复发的肿瘤,根据多学科讨论意见行下一步治疗方案。1.4 数据分析采用SPSS 23.0软件分析。计数、计量资料描述和比较分别用n(%)、(`x±s)和c2检验、t检验。使用Kaplan-Meier方法和log-rank检验评估两组的无疾病生存率(DFS)和总体生存期(OS)。P<0.05提示有统计学差异。为了减少潜在偏倚所带来的影响,对两组病例进行倾向性匹配。根据之前的研究[10-11]确定倾向模型中所需要的相关独立变量,包括性别、年龄、病灶个数、病灶大小、乙肝病毒(HBV)、谷丙转氨酶(ALT)、谷草转氨酶(AST)、甲胎蛋白(AFP)、Child-Pugh(CP)评分。最终根据上述变量按照1:2对TACE-MWA组和SR组进行匹配。表1患者匹配前后的基线资料2 结果2.1 患者基线特征匹配后共纳入患者72例(TACE-MWA组24例,SR组48例)。两组患者的性别、年龄、病灶个数、病灶大小、HBV感染率、ALT、AST、AFP、CP评分均无统计学差异(表1)。2.2 安全性评估TACE-MWA组和SR组术后并发症(发热、腹痛、恶心、呕吐)的发生率分别为33.3%(8/24)和60.4%(29/48),且两组并发症的发生率具有统计学差异(P=0.030)。所有这些反应通过对症处理后,均得到有效缓解。两组均未发现与治疗相关的严重并发症(脏器损伤、胆瘘、出血、腹水、肝衰竭)或死亡。2.3 DFS和OS所有患者的平均随访时间29.2±14.7个月(TACE-MWA:26.1±7.3个月;SR:30.8±17.1个月)。随访期间,TACE-MWA组和SR组各有1人死亡。TACE-MWA组和SR组分别有7人和16人出现肿瘤复发。TACE-MWA组出现肿瘤复发的7人中有5人再次行TACE,1人行MWA,1人因一般情况较差而行保守治疗。SR组出现肿瘤复发的16人中有6人再次行外科切除,5人行TACE,3人行MWA,2人分别因一般情况较差和患者拒绝而行保守治疗。TACE-MWA组和SR组的1年、2年和3年的DFS分别为78.8%、78.8%、56.2%和91.7%、71.9%、62.5%(图2 A),两组间DFS无明显统计学差异(P=0.730)。TACE-MWA组和SR组的1年、2年和3年的OS分别为100%、95.5%、95.5%和100%、97.5%、97.5%(图2 B),组间也无明显统计学差异(P=0.648)。图两组患者的无疾病生存率和总体生存率3 讨论本研究比较了TACE-MWA和SR治疗小肝癌的安全性及临床疗效。我们的结果显示与SR相比,TACE-MWA的联合治疗是一种可行的、安全的和有效的治疗模式。在临床上,小肝癌的理想治疗目标为根治。肝癌血供十分丰富,且部分存在动静脉短路,血流速度快[12],而丰富的血流极易带走消融产生的大量热能,即所谓的热沉效应[13]。回顾性的研究显示单纯MWA的完全消融率可以达到87-98%,直径≤3cm的病灶消融过后的局部肿瘤进展率达10-24%,5年生存率为24-78%[14-16]。然而,术前的影像学检查所确定的消融边界有时与实际肿瘤边界不符,容易导致消融范围不够,致使肿瘤残余[17]。TACE同时具有诊断和治疗的目的,也可以降低丰富的血流所造成的热沉效应[18-19],加速肿瘤组织的坏死以及加强微波的凝固作用[20]。TACE术后碘油沉积于病灶及其边缘,从而可以更为准确的评估病灶的大小以及计划消融范围。再者,TACE还能发现术前影像学检查未能发现的微小卫星灶。Seki等人[21]使用TACE-MWA治疗的18例直径>2cm且≤3cm的小肝癌患者中有17例获得了完全坏死。Yang等人[22]同样使用TACE-MWA治疗了35例直径≤3cm的小肝癌患者,结果显示所有的41个病灶均完全坏死。而本研究TACE-MWA组的所有患者第一次影像学复查提示所有病灶均完全坏死,与文献报道一致。我们的研究结果也显示TACE-MWA组的DFS略低于SR组,但无明显统计学差异(P=0.730)。通过病例回顾,我们发现TACE-MWA组复发的7例均为肝内新生病灶,而非原位复发。因此,可以认为TACE联合MWA可以为小肝癌提供类似根治性的治疗[23]。Chen[24]等人对直径≤3cm病灶的亚组分析中得出TACE-MWA术后1年、2年OS分别为100%和95%,而本研究也得出了与其相似的1年、2年OS(100%和95.5%)。Shi等人[25]对MWA与SR进行了比较,其中他们对直径≤3cm的单病灶又进行了亚组分析,结果显示两个亚组的1年、3年和5年OS(MWA组:98%、78%、65%;SR组:97%、82%、74%)和DFS(MWA组:85%、54%、33%;SR组:89%、66%、52%)均无明显统计学差异(OS:P=0.577;DFS:P=0.140)。在本研究中,TACE-MWA组中大多数为肝硬化较重不宜行手术切除的患者,研究结果表明TACE-MWA组和SR组的OS无明显统计学差异(P=0.648)。因此,我们认为在不宜行外科切除时,TACE-MWA可以作为治疗小肝癌的首选方案。两组术后我们均未观察到出血、肝衰竭等严重并发症的发生,但发热、疼痛、恶心、呕吐等并发症的发生率SR组(60.4%)明显高于TACE-MWA组(33.3%),且具有统计学差异(P=0.030)。提示TACE-MWA的微创治疗相较于外科切除更为安全,病人的术后反应也更为轻微。同样我们的研究也存在着几个缺陷:(1)由于所有患者的平均随访时间只有29.2个月,因此我们只比较了3年内的DFS与OS,而无法对5年及更长时间的DFS和OS进行比较,后续我们会对此类患者进行更长期的随访。(2)尽管使用了倾向性匹配进行统计分析以尽可能减少潜在偏倚,但仍无法完全消除回顾性研究的局限性。(3)此次研究为单中心研究,入组的患者数量相对较少,得出的结果尚需前瞻性对照研究进一步证实。总而言之,此次研究结果显示TACE-MWA取得了与SR相当的DFS和OS。TACE-MWA可以成为治疗小肝癌的一种有效的治疗模式。参考文献[1] Berretta M, Cavaliere C, Alessandrini L, et al. Serum and tissue marks in hepatocellular carcinoma and cholangiocarcinoma: clinical and prognostic implications [J]. Oncotarget, 2017, 8: 14192-14220.[2]Forner A, Reig ME, de Lope CR, et al. Current strategy for staging and treatment: the BCLC update and future prospects [J]. Semin Liver Dis, 2010, 30: 61-74.[3] Salvalaggio PR, Felga G, Axelrod DA, et al. List and liver transplant survival according to waiting time in patients with hepatocellular carcinoma [J]. Am J Transplant, 2015, 15: 668-677.[4] Ye SL, Takayama T, Geschwind J, et al. Current approaches to the treatment of early hepatocellular carcinoma [J]. Oncologist, 2010, 15: 34-41.[5] Aramaki M, Kawano K, Ohno T, et al. Microwave coagulation therapy for unresectable hepatocellular carcinoma [J]. Hepatogastroenterology, 2004, 51: 1784-1787.[6] 彭齐荣,张罗生,谢苏民,等. 冷循环微波技术治疗肝癌的临床研究[J]. 现代消化及介入诊疗, 2005,10:200-202.[7] 肖震宇,陈孝平,黄志勇. 阻断肿瘤血供后微波凝固治疗肝癌的临床研究(附120例临床分析)[J]. 中华肝胆外科杂志, 2005,11:806-808.[8] 李征,米登海,杨克虎,等. 经动脉化疗栓塞联合微波消融治疗肝癌有效性和安全性的系统评价[J]. 介入放射学杂志,2015,24:957-963.[9] Wong SN, Lin CJ, Lin CC, et al. Combined percutaneous radiofrequency ablation and ethanol injection for hepatocellular carcinoma in high risk locations [J]. AJR Am J Roentgenol, 2008, 190: 187-195.[10] Terzi E, Piscaglia F, Forlani L, et al. TACE performed in patients with s single nodule of hepatocellular carcinoma [J]. BMC Cancer, 2014, 14: 601.[11] Song MJ, Bae SH, Lee JS, et al. Combination transarterial chemoembolization and radiofrequency ablation therapy for early hepatocellular carcinoma [J]. Korean J Intern Med, 2016, 31: 242-252.[12] 杨业发,程红岩,徐爱民,等.肝癌肝外动脉供血的形成机制与介入治疗的研究[J].中华普通外科杂志,2004,19:411-413.[13] Feng K, Yan J, Li X, et al. A randomized controlled trial of radiofrequency ablation and surgical resection in the treatment of small hepatocellular carcinoma [J]. J Hepatol, 2012, 57: 794-802.[14] Donadon M, Solbiati L, Dawson L, et al. Hepatocellular carcinoma: the role of interventional oncology [J]. Liver Cancer, 2016, 6: 34-43.[15] Chinnaratha MA, Chuang MY, Fraser RJ, et al. Percutaneous thermal ablation for primary hepatocellular carcinoma: a systematic review and meta-analysis [J]. J Gastroenterol Hepatol, 2016, 31: 294-301.[16] Shibata T, Iimuro Y, Yamamoto Y, et al. Small hepatocellular carcinoma: comparison of radio-frequency ablation and percutaneous microwave coagulation therapy [J]. Radiology, 2002, 223: 331-337.[17] Petrowsky H, Busuttil RW. Resection or ablation of small hepatocellular carcinoma: what is the better treatment? [J]. J Hepatol, 2008, 49: 502-504.[18] Patterson EJ, Scudamore CH, Owen DA, et al. Radiofrequency ablation of porcine liver in vivo: effects of blood flow and treatment time on lesion size [J]. Ann Surg, 1998, 227: 559-565.[19] 宗迎迎,徐浩,许伟,等. 经肝动脉化疗栓塞联合经皮微波消融序贯治疗早期肝癌的疗效及预后影响因素[J]. 介入放射学杂志,2015,24:210-214.[20]何文,梁晓宁,张晓蓉,等. 超声引导微波联合肝动脉化疗栓塞术治疗大肝癌的疗效评价[J]. 中国微创外科杂志, 2005,5:31-33.[21] Seki T, Tamai T, Nakagawa T, et al. Combination therapy with transcatheter arterial chemoembolization and percutaneous microwave coagulation therapy for hepatocellular carcinoma [J]. Cancer, 2000, 89: 1245-1251.[22]杨维竹,江娜,黄宁,等. 经导管肝动脉化疗栓塞联合经皮微波凝固治疗小肝癌[J]. 中国医学影像技术, 2008, 24: 1647-1649.[23] Wang WD, Hou SN, Zhong ZL, et al. Radiofrequency ablation combined with transcatheter arterial chemoembolization therapy versus surgical resection for Barcelona-Clinic Liver Cancer (BCLC) A hepatocellular carcinoma: a meta-analysis[J]. J Intervent Med, 2018, 1: 49-57. [24] Chen QF, Jia ZY, Yang ZQ, et al.Transarterial chemoembolization monotherapy versus combined transarterial chemoembolization-microwave ablation therapy for hepatocellular carcinoma tumors ≤5cm: a propensity analysis at a single center [J]. Cardiovasc Intervent Radiol, 2017, 40: 1748-1755.[25] Shi J, Sun Q, Wang Y, et al. Comparison of microwave ablation and surgical resection for treatment of hepatocellular carcinomas conforming to Milan criteria [J]. J Gastroenterol Hepatol, 2014, 29: 1500-1507.
王杰 主任医师 江苏省人民医院 介入放射科1968人已读
问诊记录 查看全部
- 颅内动脉瘤 我母亲本周在江宁医院做了核磁共振,发现可能是动脉瘤,接着做了... 是否需要去当面就诊,是否需要手术,如何控制病情,谢谢总交流次数8已给处置建议
- 右侧肢体、右脸麻,轻微脑梗,颈动脉瘤 患者入院后完善双下肢静脉:双侧下肢静脉未见明显异常。头颈CT... 是否需要手术,哪种方式?手术会有并发症,后遗症吗?如果保守治疗,多长时间复查总交流次数8已给处置建议
- 颈内动脉瘤 有高血压,经常头晕头疼,近段时间做血管成像查出来颈内动脉瘤1... 这个需要手术治疗吗?到你们医院做脑动脉造影当天能做到吗?需不需要住院呢?总交流次数11已给处置建议
- 脑动脉瘤 刘主任您好!我二次复查报告,请刘主任帮我看看有没有问题?我要... 要不要治疗?总交流次数11已给处置建议
- 右颈内动脉c1段闭塞 10月10日突发右臂酸疼,右脸咀嚼困难,右眼视力模糊,右侧头... 栓塞的右颈内动脉能手术开通吗?什么时候或什么情况下可以考虑手术?哪种手术?谢谢主任!总交流次数11已给处置建议
总访问量 2,493,807次
在线服务患者 3,015位
科普文章 57篇
领导风采








