内分泌指南
发表者:杨建 人已读
指南 |中国绝经管理与绝经激素治疗指南(2018)
2019-01-03休斯敦馆阅3744转53中华医学会妇产科学分会绝经学组
【摘要】《中国绝经管理与绝经激素治疗指南(2018)》由中华医学会妇产科学分会绝经学组的全体专家在2012版指南基础上修订,并采纳了国内相关学术领域专家的修改意见,旨在指导医疗保健专业人士优化绝经过渡期及绝经后妇女的健康管理。本指南综合了本领域近年来的研究进展,也借鉴了近几年全球各大绝经学会相应指南中的重要信息,并纳入了证据水平和建议等级;保留了2012版指南中的规范绝经激素治疗(menopause hormone therapy, MHT)诊疗流程,并有所改进;增加了绝经的分期系统——生殖衰老研讨会分期+10,便于理解生殖衰老过程的临床、生物学、内分泌变化;肯定了MHT的最佳适应证是治疗血管舒缩症状(vasomotor symptoms,VMS)、生殖泌尿道萎缩相关问题和预防绝经相关的低骨量及骨质疏松症。MHT的风险取决于药物类型、剂量、使用时间、管理方式、启动时间以及是否使用孕激素。MHT应依据现有最好的证据个体化进行,定期重新评估是否继续或停止MHT,以获得最大收益及最小风险。对年龄小于60岁或绝经10年内无MHT禁忌证的妇女,针对VMS、骨量丢失和骨折,启动MHT治疗的收益风险比最高。只要无禁忌证,早发性卵巢功能不全患者应给予激素补充治疗至普通女性自然绝经的平均年龄,之后按照绝经后MHT原则进行。
【关键词】指南;绝经;绝经激素治疗;激素补充治疗;血管舒缩症状;乳腺癌;心血管疾病;认知;绝经生殖泌尿综合征
绝经的本质是卵巢功能衰竭。伴随卵巢功能的衰退,女性会出现多种绝经相关症状、组织萎缩退化和代谢功能紊乱,导致一系列身心健康问题。随着人类寿命的延长,绝经过渡期和绝经后期已成为女性生命周期中最长的一个阶段,需要对该阶段女性进行全面生活方式指导和健康管理,包括饮食、运动、控烟、限酒等,并指导适宜人群开展绝经激素治疗(menopause hormone therapy, MHT),或对非适宜人群采用非激素治疗,以缓解更年期相关症状,提高和改善其生命质量。
MHT是针对卵巢功能衰竭而采取的一种治疗措施。经过多年实践证实,科学应用MHT可有效缓解绝经相关症状,绝经早期使用还可在一定程度上预防老年慢性疾病的发生[1- 2]。
为使国内各级医师更好地开展绝经管理并指导治疗,中华医学会妇产科学分会绝经学组基于国内外最新循证医学结果和最佳证据,参考国际最新相关指南,结合我国具体情况,在2012年修订的《绝经期管理与激素补充治疗临床应用指南》[3]基础上,经多次讨论修改,制定本指南。本指南中应用的证据水平和建议等级来自英国皇家学院UK Green TOP指南[4]。
1绝经的诊断和分期
1.1诊断
绝经是指月经永久性停止,属回顾性临床诊断。40岁以上女性末次月经后12个月仍未出现月经,排除妊娠后则可临床诊断为绝经(注:这个概念有误导之嫌,应该加上:并且激素水平符合绝经的表现。因为我遇到好几个50岁以后1-2年不来月经的,主管医生直接诊断“绝经”,次日查房,建议查激素水平来确定诊断,结果,激素水平显示患者没有绝经,只是闭经而已。如果不查激素,也不干预的话,子宫内膜长期受雌激素刺激,癌变的可能性明显增加)。绝经的真正含义并非指月经的有无,而是指卵巢功能的衰竭。单纯子宫切除的妇女,虽然不再有月经来潮,如卵巢功能正常,则不属于绝经范畴。
1.2分期
随着临床和科研的深入,需对生殖衰老过程进一步细分。2011年发表的“生殖衰老研讨会分期+10”(Stages of Reproductive Aging Workshop+10, STRAW+10)是目前公认的生殖衰老分期金标准[B][5]。该分期系统将女性生殖衰老分为3个阶段:生育期、绝经过渡期和绝经后期,每个阶段又进一步划分为早期和晚期;生育期增加了峰期,用阿拉伯数字-5~+2表示;生育期晚期和绝经后期早期进一步细分为2~3个亚阶段,采用阿拉伯数字后加英文字母a、b、c表示,故整个生殖衰老分期由10个特定阶段构成(图1)。
生殖衰老分期系统的主要标准是月经周期长度改变。进入绝经过渡期早期(-2)的标志是月经周期长短不一(即月经紊乱),10次月经周期中有2次或以上发生邻近月经周期改变≥7 d;进入绝经过渡期晚期(-1)的标志是月经周期≥60 d,且卵泡刺激素(follicle-stimulating hormone,FSH)≥25 U/L。绝经后期早期的+1a阶段为最终月经(final menstrual period,FMP)后的1年,+1a结束方能明确绝经;+1b为+1a后1年;在+1a和+1b阶段,激素水平仍然波动较大;进入+1c阶段,FSH稳定升高,雌二醇持续维持在低水平。+2期为绝经后期晚期,此阶段女性健康问题更多体现在各种组织器官退行性改变导致的各种疾病,包括骨质疏松症、心脑血管疾病、认知功能障碍等。
需注意的是,STRAW+10分期标准适用于大多数女性,但不适用于多囊卵巢综合征、早发性卵巢功能不全(premature ovarian insufficiency, POI)、子宫内膜切除和子宫切除、慢性疾病及化疗影响了卵巢功能的女性,这些情况下应采用内分泌指标和窦卵泡计数等支持标准确定其生殖衰老分期。
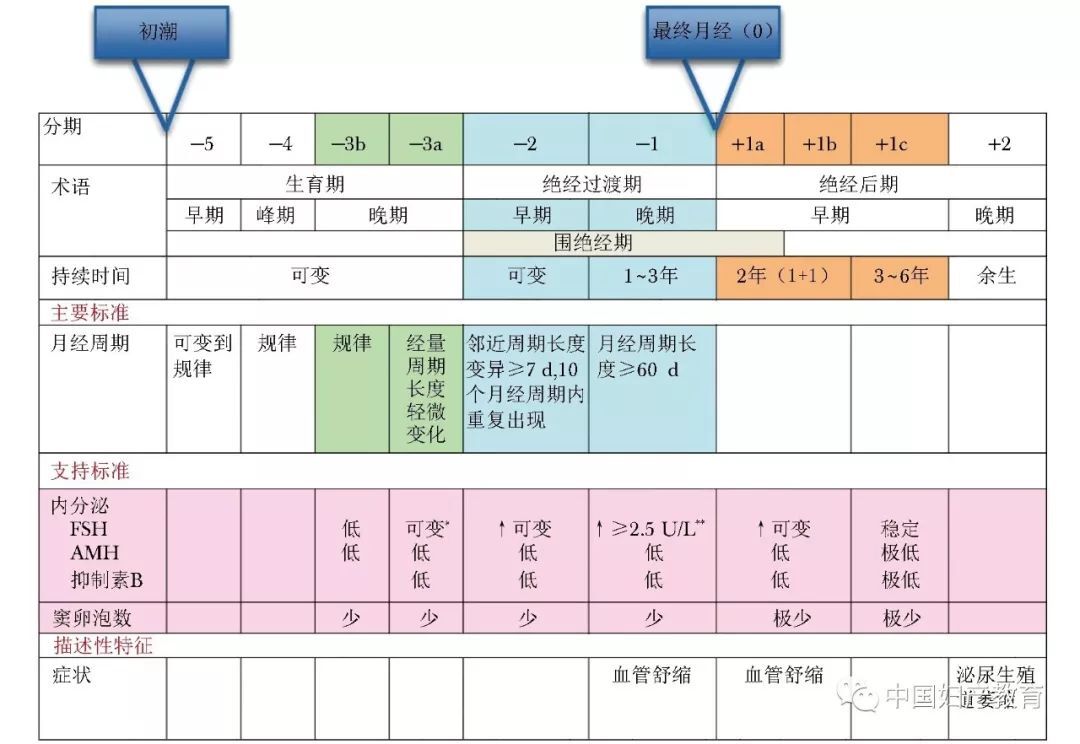
图1生殖衰老研讨会分期+10系统
FSH:卵泡刺激素; AMH:抗缪勒氏管激素;*在周期第2~5天取血;**依据目前采用的国际垂体激素标准的大致预期水平
2绝经健康管理策略和绝经激素治疗的指导原则
2.1绝经健康管理策略
卵巢功能衰退是女性衰老的突出表现,女性将经历月经改变直至绝经,并伴随多种绝经相关症状。绝经对心血管、骨骼、认知会产生持续不良影响,需对绝经女性开展全面健康管理,包括每年健康体检、推荐合理饮食、增加社交脑力活动和健康锻炼。中国幅员辽阔,地域差别大,结合各地的饮食习惯,建议全谷物纤维、足量蔬菜和水果、每周2次鱼类食品、控糖(≤50 g/d)、少油(25~30 g/d)、限盐(≤6 g/d)、限酒(酒精量≤15 g/d)、戒烟,足量饮水(1500~1700 ml/d)[6]。每日规律有氧运动,每周累计150 min,另加2~3次抗阻运动,以增加肌肉量和肌力[B]。
2.2绝经激素治疗指导原则[1-3,7-9]
2.2.1 MHT属医疗措施,启动MHT应在有适应证、无禁忌证、女性本人有通过MHT改善生活质量的主观意愿前提下尽早开始[A]。
2.2.2绝经过渡期女性与老年女性使用MHT的风险和获益不同。对年龄<60岁或绝经10年内、无禁忌证的女性,mht用于缓解血管舒缩症状(vasomotor>
2.2.3不推荐仅为预防心血管疾病和阿尔兹海默病目的而采用MHT。雌激素缺乏后尽早开始MHT可使女性获得雌激素对心血管和认知的保护[A]。
2.2.4有子宫的女性在补充雌激素时,应加用足量足疗程孕激素以保护子宫内膜;已切除子宫的妇女,通常不必加用孕激素[A]。
2.2.5 MHT必须个体化。根据治疗症状的需求、获益/风险评估、相关检查结果、个人偏好和治疗期望等因素,选择性激素的种类、剂量、配伍、用药途径、使用时间[A]。
2.2.6接受MHT的女性每年至少接受一次全面获益/风险评估,包括绝经症状评分、新发疾病筛查、全面体检、必要的检查检验,讨论生活方式和防控慢病策略,根据评估结果个体化调整MHT方案。目前尚无证据支持限制MHT应用的时间,只要获益/风险评估结果提示获益大于风险则可继续使用MHT[A]。
2.2.7不推荐乳腺癌术后患者使用MHT[B]。
2.2.8仅为改善绝经生殖泌尿综合征(genitourinary syndrome of menopause,GSM)时建议首选阴道局部雌激素治疗;当口服或经皮MHT不能完全改善生殖泌尿道局部症状时,可同时加用局部雌激素治疗[A]。
2.2.9绝经后腹部脂肪增加与雌激素水平降低有关[B]。雌激素治疗可减少绝经后腹部脂肪堆积,减少总体脂肪量,改善胰岛素敏感度,降低2型糖尿病的发病率[A]。
3绝经激素治疗的适应证和禁忌证
3.1适应证
不同年龄女性启动MHT获益不同,推荐在卵巢功能衰退后尽早启动。对于POI患者,只要无禁忌证,建议行MHT。
3.1.1绝经相关症状
月经紊乱、潮热、多汗、睡眠障碍、疲倦、情绪障碍(如易激动、烦躁、焦虑、紧张、低落)等[A]。
3.1.2生殖泌尿道萎缩相关问题(GSM)
阴道干涩,外阴阴道疼痛、瘙痒,性交痛,反复发作的萎缩性阴道炎,反复下尿路感染,夜尿、尿频、尿急等[A]。
3.1.3低骨量及骨质疏松症
存在骨质疏松症的危险因素及绝经后骨质疏松症。MHT可作为预防60岁以下及绝经10年以内女性骨质疏松性骨折的一线选择[A]。
3.2禁忌证
(1)已知或怀疑妊娠;
(2)原因不明的阴道出血;
(3)已知或可疑患乳腺癌;
(4)已知或可疑患性激素依赖性恶性肿瘤;
(5)最近6个月内患活动性静脉或动脉血栓栓塞性疾病;
(6)严重肝肾功能不全;
(7)血卟啉症、耳硬化症;
(8)现患脑膜瘤(禁用孕激素)。
4绝经激素治疗的慎用情况
慎用并非禁用,在应用前和应用过程中应咨询相应专业医生,共同确定应用MHT的时机和方式,同时采取比常规随诊更为严密的措施,监测病情进展。
4.1子宫肌瘤
子宫切除术后或肌瘤剔除术后的女性可行MHT。保留子宫行MHT者,肌瘤<3>5 cm风险可能会增大,肌瘤3~5 cm者应根据患者情况综合判断。对肌瘤而言,雌激素口服比经皮更安全,替勃龙比雌孕激素连续联合疗法(estrogen progestogen therapy, EPT)更安全[3,7,10]。
4.2子宫内膜异位症
子宫内膜异位症患者自然绝经后需MHT者,建议使用EPT(E+P)或替勃龙治疗,不建议使用序贯疗法,雌激素应使用最低有效剂量。严重子宫内膜异位症行子宫及双侧附件切除后的患者,如需MHT,建议使用雌孕连续联合激素方案或替勃龙治疗至少2年后再改为单用雌激素[11]。
4.3子宫内膜增生症
子宫内膜不典型增生的治疗原则是子宫切除。无不典型子宫内膜增生症须在治疗完全逆转后,才可考虑MHT。EPT对保留子宫的女性具有更高的安全性;全子宫切除术后是否需联合使用孕激素尚无明确证据。所有患者均应密切随访,有子宫者定期行子宫内膜活检术[12]。
4.4血栓形成倾向
所有绝经后女性开始MHT前均需对血栓形成的危险因素、血栓栓塞病史及家族史进行详细了解和评价,具有阳性病史者建议专科就诊咨询,必要时行易栓症相关筛查。经皮雌激素的血栓风险显著低于口服雌激素[13- 14]。
4.5胆囊疾病
MHT可能促进胆囊结石的形成,增加胆囊手术风险。经皮雌激素可能具有较高的安全性[15]。
4.6系统性红斑狼疮
雌激素在系统性红斑狼疮(systemic lupus erythematosus,SLE)的病理过程中可能起重要作用。SLE患者更容易出现卵巢早衰和骨质疏松。已有证据提示SLE活动期患者不适合MHT,病情稳定或处于静止期者可在严密观察下行MHT。此外,SLE患者有更高的血栓形成风险,应用经皮雌激素可减少血栓形成[16]。
4.7乳腺良性疾病及乳腺癌家族史
影像检查提示的乳腺增生并非病理性改变,不是MHT的禁忌证。组织学诊断的乳腺增生,尤其非典型增生,需咨询专科医生是否可行MHT。其他乳腺良性疾病包括脂肪坏死、乳腺纤维瘤、乳管乳头状瘤的乳腺癌风险尚不确定[17]。
大多数乳腺癌是散发的,并无家族聚集性。MHT不会进一步增加有乳腺癌家族史女性乳腺癌的风险,也不会增加卵巢切除术后BRCA1或BRCA2基因突变女性的乳腺癌风险[18]。
4.8癫痫、偏头痛、哮喘
MHT中雌激素剂量的增加与癫痫发作频率增加相关[4]。先兆偏头痛是卒中高危因素,雌激素对偏头痛的作用与其血清浓度波动密切相关。血清雌二醇水平波动可能影响女性患者哮喘发作的严重程度,使用经皮雌激素或EPT可能具有更高的安全性。
5绝经激素治疗常用药物和方案
5.1常用口服药物
5.1.1雌激素
天然雌激素:17β-雌二醇、戊酸雌二醇、结合雌激素。
注:结合雌激素片主要成份为:含有从孕马尿液中提取的雌激素混合物,为水溶性雌激素硫酸钠盐混合物。它是雌酮硫酸钠与马烯雌酮硫酸钠的混合物。同时还含有硫酸钠结合物、17α-氢马烯雌酮、17α-雌二醇和17β-_氢马烯雌酮。
戊酸雌二醇是人体天然雌激素17β-雌二醇的前体。
5.1.2孕激素
5.1.2.1天然孕激素:微粒化黄体酮。
5.1.2.2合成孕激素:地屈孕酮、17ɑ-羟孕酮衍生物[如醋酸甲羟孕酮(medroxyprogesterone acetate,MPA)]、19-去甲睾酮衍生物(如炔诺酮、醋酸炔诺酮、左炔诺孕酮、地诺孕素)、19-去甲孕酮衍生物(如诺美孕酮)、螺内酯衍生物(如屈螺酮)等。
地屈孕酮是最接近天然的孕激素,对乳腺刺激较小。屈螺酮具有较强的抗盐皮质激素作用和一定的抗雄激素作用。
推荐应用天然雌激素、天然或最接近天然的孕激素[A]。
注:地屈孕酮,我最不喜欢用的孕激素,现在全国的妇产科医生多数都在用,我认为被吹得太神了,厂家的广告果然厉害,所以从心里抵触。注意,天然孕激素是微粒黄体酮和黄体酮针剂。地屈孕酮是合成的,只是接近天然。
5.1.3雌、孕激素复方制剂
5.1.3.1雌、孕激素序贯制剂
雌二醇/雌二醇地屈孕酮片(注:芬吗通):每盒28片,前14片仅含雌二醇,后14片每片含雌二醇及10 mg地屈孕酮。因雌二醇含量不同分为两种剂型1/10和2/10,1/10中每片含1 mg雌二醇,2/10中每片含2 mg雌二醇。
戊酸雌二醇/戊酸雌二醇醋酸环丙孕酮片(注:克龄蒙):每盒21片,前11片每片含2 mg戊酸雌二醇;后10片每片含2 mg戊酸雌二醇及1 mg醋酸环丙孕酮。
5.1.3.2雌、孕激素连续联合制剂
雌二醇/屈螺酮片(注:安今益):每盒28片,每片含雌二醇1 mg和屈螺酮2 mg。
5.1.4替勃龙
替勃龙有效成分为7-甲基-异炔诺酮,属于组织选择性雌激素活性调节剂,2.5 mg/片。口服后在体内代谢后产生较弱的雌激素、孕激素和雄激素活性,对情绪低落和性欲低下有较好的效果,不增加乳腺密度[19][A]。
5.2常用非口服药物
5.2.1经皮雌激素
雌二醇凝胶,每2.5 g含雌二醇1.5 mg,每日经皮涂抹;半水合雌二醇皮贴,每贴每日释放17β-雌二醇50 μg,每周更换1次。
雌激素经皮给药避免了口服的肝脏首过效应,减少了对肝脏合成蛋白质及凝血因子生成的影响。相对于口服,经皮雌激素的静脉血栓、心血管事件、胆囊疾病的风险显著降低,改善性欲的作用更优[14][A]。
5.2.2经阴道雌激素
雌三醇乳膏:每克乳膏含雌三醇1 mg;普罗雌烯阴道胶丸:每粒含普罗雌烯10 mg;氯喹那多-普罗雌烯阴道片:每片含普罗雌烯10 mg和氯喹那多200 mg;结合雌激素软膏:每克软膏含结合雌激素0.625 mg。
雌三醇对子宫内膜刺激小,对血浆雌二醇水平基本无影响;普罗雌烯属于严格局部作用的雌激素,不吸收入血,不刺激子宫内膜增生;结合雌激素可轻度升高血浆雌二醇水平,对子宫内膜作用亦为轻度。
5.2.3左炔诺孕酮宫内系统(levonorgestrel intrauter-ine system,LNG-IUS)
含LNG 52 mg,每日向宫腔释放LNG 20 μg,维持5年。LNG使子宫内膜腺体萎缩、间质蜕膜化、内膜变薄,可预防和治疗子宫内膜增生[12][A],亦可用于MHT的子宫内膜保护[20][C]。
5.3具体方案
5.3.1单孕激素补充方案:适用于绝经过渡期早期,调整卵巢功能衰退过程中的月经问题。
5.3.1.1口服:地屈孕酮10~20 mg/d或微粒化黄体酮200~300 mg/d或醋酸甲羟孕酮4~6 mg/d,于月经或撤退性出血的第14天起,使用10~14 d。
5.3.1.2宫腔内放置:LNG-IUS,尤其适合于有子宫内膜增生的患者。
5.3.2单雌激素补充方案:适用于子宫已切除的妇女,通常连续应用。
5.3.2.1口服:戊酸雌二醇0.5~2 mg/d、或17β-雌二醇1~2 mg/d、或结合雌激素0.3~0.625 mg/d。
5.3.2.2经皮:半水合雌二醇贴0.5~1帖/7 d;或雌二醇凝胶0.5~1计量尺/d,涂抹于手臂、大腿、臀部等皮肤(避开乳房和会阴)。
5.3.3雌孕激素序贯方案:适用于有完整子宫、围绝经期或绝经后仍希望有月经样出血的妇女。
5.3.3.1连续序贯:在治疗过程中每天均用药。可采用连续序贯复方制剂:雌二醇/雌二醇地屈孕酮片(注:芬吗通)(1/10或2/10) 1片/d,共28 d;也可连续用口服或经皮雌激素28 d,后10~14 d加用孕激素。
5.3.3.2周期序贯:在治疗过程中每周期有3~7 d不用任何药物。可采用周期序贯复方制剂戊酸雌二醇片/雌二醇环丙孕酮片(注:克龄蒙),1片/d,共21 d;也可采用连续用口服或经皮雌激素21~25 d,后10~14 d加用孕激素,然后停药3~7 d,再开始下一周期。
5.3.4雌、孕激素连续联合方案:适用于有完整子宫、绝经后不希望有月经样出血的妇女。可每天采用雌激素(口服或经皮)加孕激素,连续给药;也可采用复方制剂如雌二醇/屈螺酮片1片/d(注:安今益),连续给药。
5.3.5替勃龙:1.25~2.5 mg/d,连续应用。
5.3.6阴道局部雌激素的应用:可使用雌三醇乳膏、普罗雌烯阴道胶丸或霜、结合雌激素软膏,1次/d,连续使用2周,症状缓解后改为2次/周。短期(3~6个月)局部应用雌激素阴道制剂,无需加用孕激素<1+>,但缺乏超过1年使用的安全性数据,长期使用者应监测子宫内膜。
6规范绝经激素治疗诊疗流程[21]
6.1总体诊疗流程
首先评估拟采用MHT患者的适应证、禁忌证和慎用情况。有适应证、无禁忌证、慎用情况控制良好者可予以MHT;存在禁忌证,或慎用情况尚未控制但急需治疗绝经相关症状者,给予非激素治疗。所有接受MHT的女性应同时进行健康指导。原则上不推荐女性60岁以后或绝经10年以上开始启用MHT。MHT应用中应定期随访,并评估风险和利弊,个体化调整MHT方案(图2)。
6.2更年期门诊初次接诊流程
接诊流程包括病史采集,经查体和必要的辅助检查以判断就诊对象的绝经状态,并进行医学处理前的基本临床检查(图3)。初次接诊的重要目的是判断是否有MHT的适应证,是否存在禁忌证和/或慎用情况。
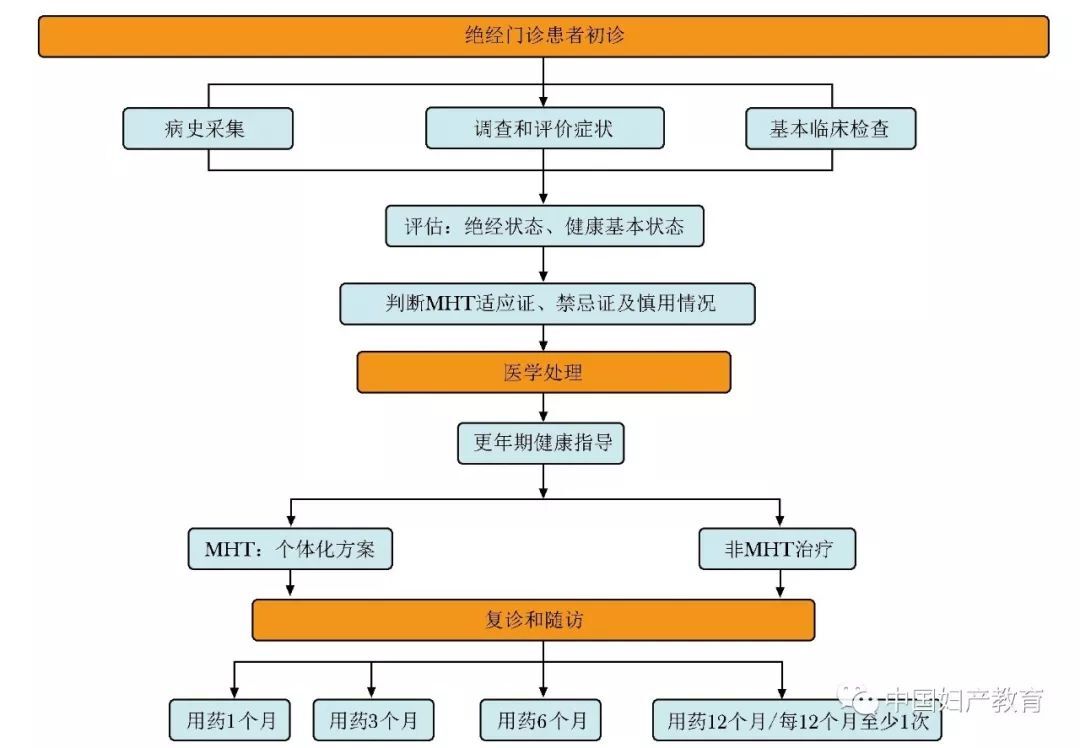
图2MHT临床规范诊疗流程
MHT:绝经激素治疗
6.3方案选择
对所有患者进行更年期健康指导。拟接受MHT的患者,根据患者本人的意愿和病情特点,如子宫、全身或局部症状的个体化差异,风险和利弊评估结果,选择恰当的个体化MHT方案;不可或不愿接受MHT的患者,推荐非MHT疗法(图4)。
6.4复诊和随访
MHT的定期随诊非常重要。复诊的主要目的在于了解治疗效果,解释可能发生的乳房胀痛和非预期出血等副反应,关注MHT获益和风险,个体化调整方案,鼓励适宜对象坚持治疗。MHT的使用期无特殊限定,可按个体情况和本人意愿调整MHT方案或改变治疗策略,年长女性应更谨慎评估MHT风险和关注不良事件。只要获益大于风险,鼓励坚持规范用药,定期随访(图5)。
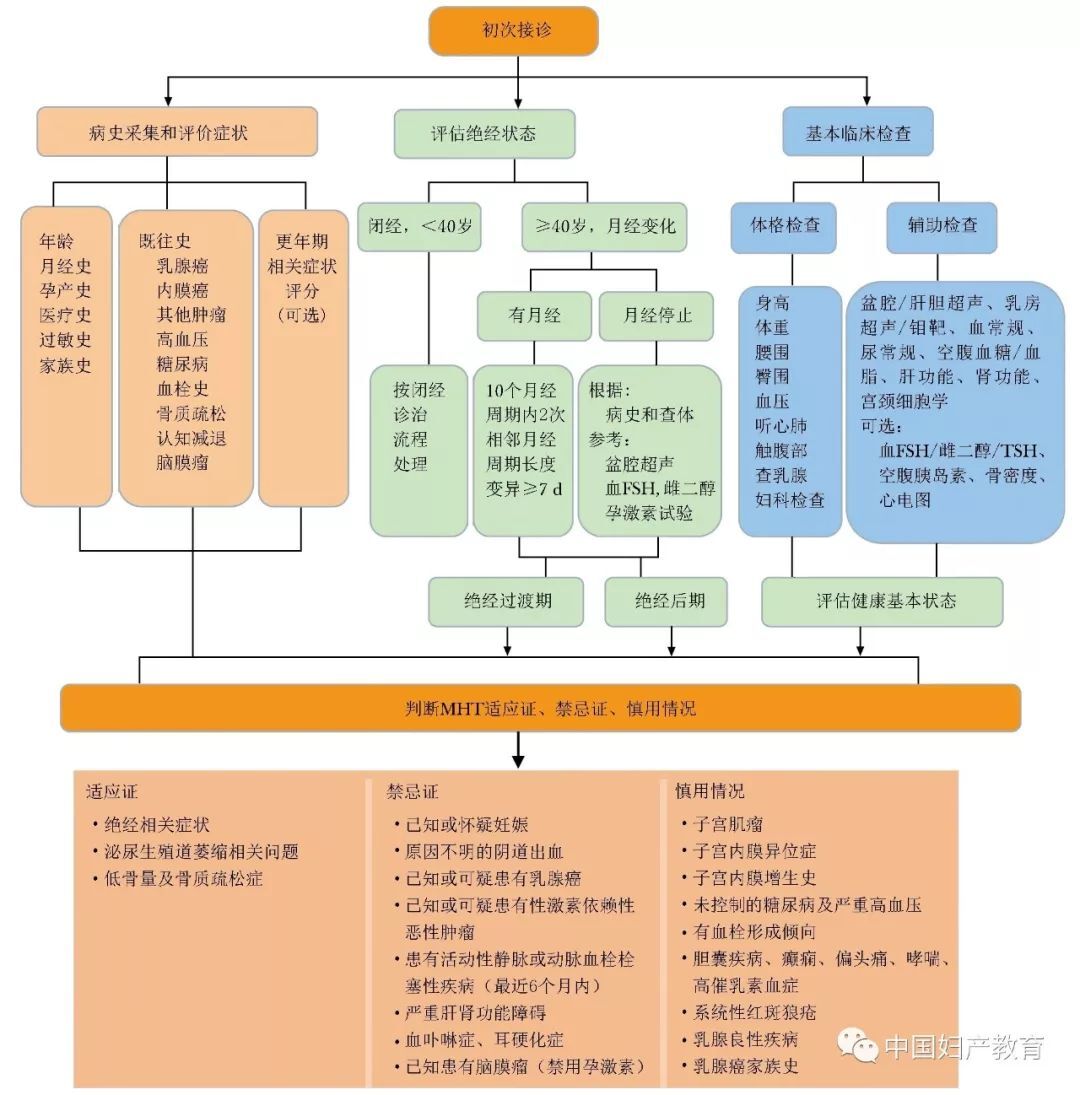
图3更年期门诊初次接诊流程
FSH:同图1; MHT:同图2;TSH:促甲状腺激素
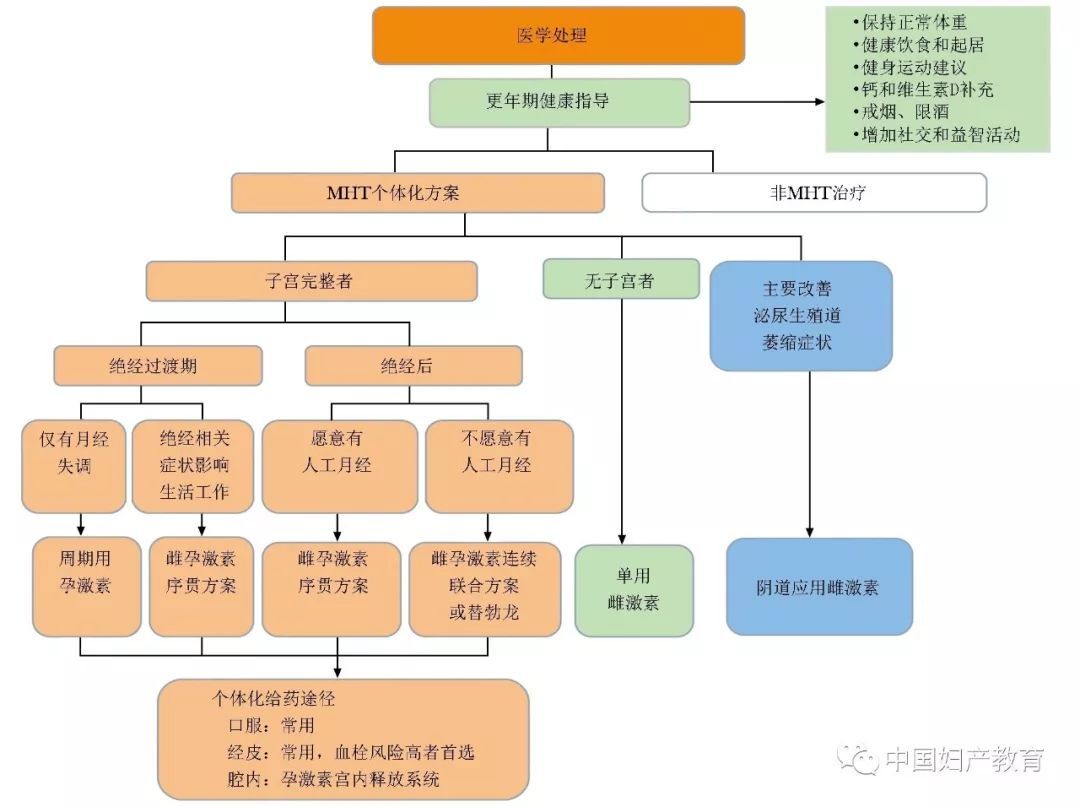
图4绝经激素治疗方案选择策略
MHT:同图2
7绝经激素治疗的长期获益与风险
7.1绝经后骨质疏松症
绝经后由于雌激素缺乏,骨转换增加,骨吸收大于骨形成致骨量丢失加速,导致骨质疏松症发生风险明显增加。MHT通过抑制破骨细胞活动和降低骨转化以减缓绝经后女性骨量丢失,对于绝经前后启动MHT的女性,可获得骨质疏松性骨折一级预防的好处[2,22][A]。
7.2心脑血管疾病
对于年龄<>[23][A]。低剂量经皮雌激素(<50>[24][B]。不建议单纯为预防冠心病启动MHT[A]。近几年的随机临床试验,如DOPS[25]、KEEPS[26]、ELITE[27],证实了绝经早期启用MHT是可降低心血管损害并可能获益的“机会窗” <1+>。
MHT相关静脉血栓栓塞症(venous thromboembolism,VTE)的风险随年龄增长而增加,且与肥胖程度呈正相关。口服MHT增加VTE事件风险,有VTE个人史的女性禁用口服雌激素治疗[A]。经皮雌激素不增加VTE的风险<2++>,有VTE高风险(包括体质量指数>30 kg/m2、吸烟、易栓症家族史)的女性,经皮雌激素可能更安全[24][B]。某些孕激素,如MPA,导致VTE风险增大[C]。
7.3中枢神经系统
MHT可改善与绝经相关的轻中度抑郁症状<1++>。及早开始MHT对降低阿尔茨海默病和痴呆风险有益,特别是手术绝经的女性[28][B]。>60岁或绝经10年以上才启用MHT会对认知功能产生不利影响,增加痴呆风险<1+>。MHT可能会增加癫痫患者的发作频率<1-~2->,与帕金森病风险无关[B],对偏头痛、多发性硬化症的影响尚不确定[B]。
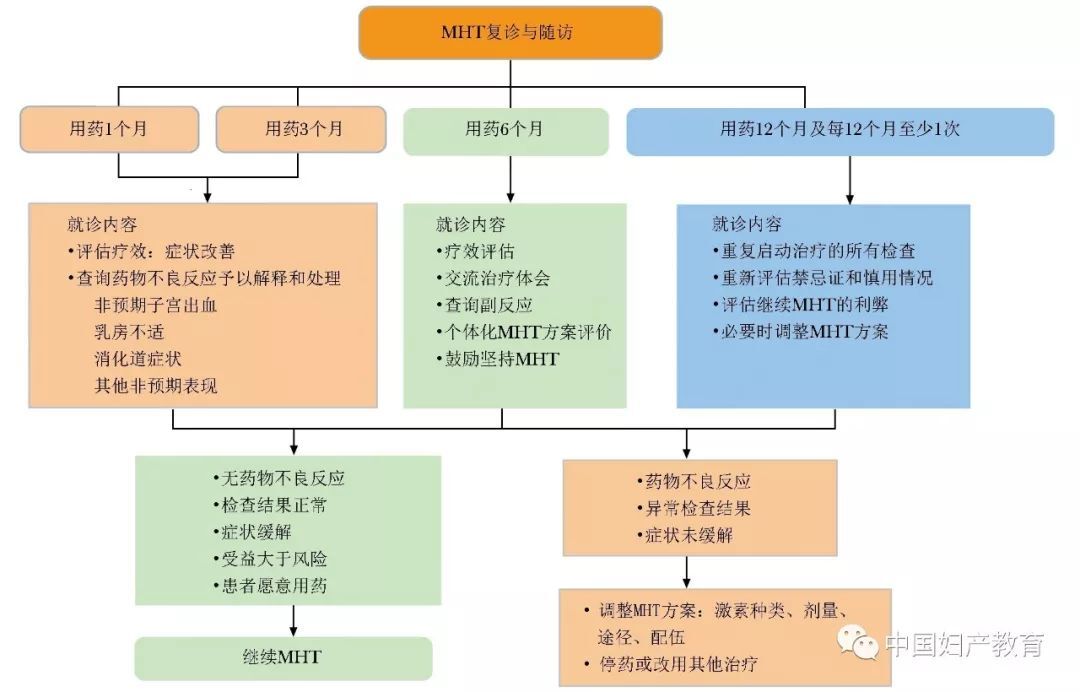
图5绝经激素治疗复诊与随访
MHT:同图2
7.4 2型糖尿病
雌激素可增加胰岛素敏感度[29],提高碳水化合物的代谢,有助于血糖控制,可减少或延缓发展为2型糖尿病。雌激素口服与经皮给药相比,能更大程度减少糖尿病的发展,尤其在绝经10年内受益更明显,但不提倡MHT用于预防2型糖尿病[30][A]。糖尿病患者冠心病风险发生率高,应用MHT时需加强监护,血糖控制不佳者,应慎重权衡MHT的利弊[B]。
7.5绝经后肌肉骨关节症状
绝经后肌肉骨关节症状是常见躯体症状,表现为肩、颈腰背部肌肉和肌腱疼痛;关节症状主要表现为肩、膝,腰骶关节和手指关节等部位的疼痛,常伴有骨关节炎。雌激素缺乏与骨关节炎发生有一定关系,MHT能够减少软骨的降解和关节替代手术<1+>。
7.6肌肉减少
肌肉减少症(下文简称肌少症)是一种以进行性骨骼肌质量减少和力量降低、功能下降为特征,进而引起相关衰弱、跌倒、残疾等不良事件的综合征。研究表明,体内性激素水平降低可能是肌少症发生的关键机制之一[31]。睾酮和雌激素水平下降加速肌肉减少及骨骼肌质量下降。对绝经后女性应用MHT可预防女性肌少症的发生[32][B]。
7.7乳腺癌
MHT引起的乳腺癌风险很小,治疗结束后风险逐渐降低[33][B]。乳腺癌风险增加主要与MHT方案中添加的合成孕激素有关,并与孕激素应用的持续时间有关[34]。天然孕激素和选择性雌激素受体调节剂优化了对代谢和乳腺的影响。与合成孕激素相比,微粒化黄体酮或地屈孕酮导致乳腺癌的风险可能更低[35]。现有数据显示,口服和经皮雌激素给药途径之间的乳腺癌风险并无差异[36]<2+>。
7.8子宫内膜癌
有子宫的女性,MHT方案中应加用足量及足疗程的孕激素以保护子宫内膜[A]。连续联合方案对防止子宫内膜增生和子宫内膜癌最有效,MHT序贯方案中孕激素的使用时间不应短于10~14 d[37][A]。
7.9宫颈癌
随机对照研究(WHI和HERS)显示,使用MHT不增加宫颈癌的风险[A]。长期队列研究结果类似[38][B]。
7.10卵巢癌
根据现有数据,MHT与卵巢癌的风险关系仍不明确[39- 40][B]。
7.11肺癌
WHI和观察性研究提示:单用雌激素或EPT均不增加肺癌的发病率[A];EPT≤5年,对所有类型肺癌有保护性作用;任何方案MHT治疗5~10年,对非小细胞肺癌有保护性作用;EPT≥10年的吸烟者肺癌风险增加[B];EPT肺癌的死亡风险较高,但不增加50~59岁妇女的肺癌死亡率[41- 42]。
7.12结直肠癌
MHT可降低结直肠癌发生风险[43- 44]<2++>。3项荟萃分析结果显示,MHT停止4年后仍然对结直肠癌风险降低具有有益的作用[45- 46][A]。
7.13上消化道癌
MHT与肝细胞癌之间无明确相关性[47]。MHT可能降低胃癌发生的风险[48]。MHT是否增加胆囊癌、食管癌发生风险目前仍有争议[49][C]。
8绝经相关症状的治疗策略
8.1血管舒缩症状
8.1.1 MHT:对于无禁忌证的女性,雌激素是治疗VMS最有效的措施,同时可改善睡眠障碍、情绪不稳定等绝经症状,提高绝经女性健康相关的生活质量[50- 51][A]。
8.1.2非MHT:主要用于有MHT禁忌证和对MHT有顾虑不愿意使用者。
8.1.2.1选择性5-羟色胺再摄取抑制剂、选择性5-羟色胺和去甲肾上腺素双重再摄取抑制剂、可乐定对缓解VMS有一定效果,但不能作为MHT替代方案,可用于有MHT禁忌证的女性[52][A]。加巴喷丁对VMS有效,但副作用较前述药物多[53][B]。
8.1.2.2经随机对照试验研究证实,某些中成药(如香芍颗粒[54]和坤泰胶囊[55])对缓解VMS及其他绝经期症状有效。某些植物药(如黑升麻[56])对缓解VMS及其他绝经症状可能有效。这些药物的长期安全性仍需更多的循证医学研究数据支持[C]。
8.1.2.3生物同质激素:指具有与内源性激素相同分子结构的合成的外源性激素。尚无有力的证据支持该类激素制剂的安全性及有效性,不推荐使用[7,57][B]。
8.1.2.4植物雌激素:常见的有大豆异黄酮。该类激素疗效尚存在争议,且缺乏长期的安全性研究数据,不推荐使用[58]。
8.1.2.5其他:正念减压疗法、星状神经节阻滞、针灸、催眠等可能起到辅助治疗作用[59- 60][B]。
8.2泌尿生殖系统症状
GSM包括与绝经雌激素缺乏相关的外阴、阴道、尿道和膀胱症状与体征。生殖道症状包括生殖道干燥、烧灼、刺激,阴道润滑缺乏导致的性问题和疼痛。泌尿道症状包括尿急,尿痛和反复泌尿系感染。雌激素对GSM治疗最有效。
8.2.1对于以GSM为主的绝经后女性:若无系统MHT禁忌证,首选阴道局部雌激素治疗[61];若有系统MHT禁忌证或生殖泌尿道萎缩症状,首选润滑剂和湿润剂治疗,若无效,可在严密观察下短期选择阴道局部雌激素治疗[62][A]。
8.2.2全身症状明显同时合并GSM者,系统应用MHT可使GSM得到缓解;若缓解不明显,可在系统应用MHT的同时阴道局部应用低剂量雌激素[63]。
8.2.3阴道局部雌激素治疗可减少复发性尿路感染的次数[64]<1+>。
8.2.4不推荐使用系统MHT治疗压力性尿失禁[65][A]。
8.2.5膀胱过度活动症(overactive bladder,OAB)是一种以尿急症状为特征的症候群,常伴有尿频和夜尿症状,伴或不伴急迫性尿失禁。阴道使用雌激素对改善尿急、尿频症状有优势<2+>,推荐抗胆碱能药物与局部雌激素联合使用作为治疗绝经后女性OAB的一线药物[66],同时结合生活方式改变及膀胱训练[A]。
补充雌激素常与盆底锻炼、子宫托、盆底手术联合使用,改善胶原合成和阴道上皮萎缩症状,但在子宫脱垂治疗有效性方面缺乏证据。
8.3绝经女性的性健康和避孕
8.3.1绝经女性的性健康
绝经症状与绝经期妇女生活质量密切相关。增龄和性激素水平的下降导致了绝经期妇女性功能障碍(female sexual dysfunction, FSD)发生率增高,心理和社会因素也有影响[67][B]。绝经期FSD的最常见表现是性欲减退,其次是与生殖道萎缩相关的性交困难和疼痛[68][C]。
8.3.1.1 MHT可改善轻度至中度FSD(尤其在疼痛方面)[69][A],替勃龙也对FSD具有治疗价值[70][A]。睾酮治疗可能对性欲和/或性兴奋缺乏的妇女有用[71][A]。
8.3.1.2阴道保湿和润滑剂能够有效治疗轻度至中度阴道干燥以缓解性交时的不适和疼痛[2][B]。
8.3.2围绝经期避孕
没有具体针对年龄的避孕方法禁忌证。复方口服避孕药可在避孕同时缓解绝经相关症状,缓解阴道干涩,但高龄女性使用复方口服避孕药的潜在血栓风险高于年轻女性[C],选择屏障法避孕更安全。孕激素宫内缓释系统(LNG-IUS)长效、可逆,可提供围绝经期的高效避孕(失败率<>[72][A]。不推荐绝经后女性使用复方口服避孕药代替MHT,复方口服避孕药更高的雌激素活性可能导致心血管不良事件风险增加[D],且对骨骼的保护作用不及MHT[72]。
9早发性卵巢功能不全
POI指女性在40岁前卵巢功能衰退的临床综合征,以停经或月经稀发4个月、间隔>4周,连续2次FSH>25 U/L为主要特征[73,74]。40岁以下和30岁以下女性POI的发病率分别为1%和0.1%[75]。由于雌激素水平下降更早出现,POI患者低雌激素相关问题如骨质疏松、心血管、泌尿生殖道健康问题及认知功能减退问题风险更大。POI女性MHT获益更多,风险更小。只要POI患者无禁忌证,应给予性激素补充治疗(hormone replacement therapy, HRT)至普通女性自然绝经的平均年龄,之后按照MHT原则进行[B]。POI患者年轻时需要相对较大剂量的雌激素[76],推荐剂量为17β-雌二醇2 mg/d、结合雌激素1.25 mg/d或经皮雌二醇75~100 μg/d。由于患者诊断POI后仍有5%的怀孕几率[77],在POI早期有避孕需求者可考虑短期应用复方口服避孕药(compound oral contraceptives,COCs),但不宜长期应用。HRT与COCs相比,对骨骼及代谢更有利[78]<1->。
10小结
卵巢功能衰退将给女性带来长期健康危害,严重影响其生活质量。因此,绝经管理理应成为妇产科专业工作者的必然使命。应针对不同需求和不同基础健康状态,采用最适宜于患者的措施改善相关症状,减轻由于雌激素缺乏带来的长期不良影响,让绝经过渡期和绝经后期妇女更具尊严地生活。
参与制定本指南的专家组名单(按姓氏汉语拼音排序)
曹媛(郑州大学第一附属医院)
陈蓉(北京协和医院)
陈子江(山东省立医院)
丁岩(新疆医科大学第一附属医院)
符书馨(中南大学湘雅二医院)
郭雪桃(山西医科大学第一医院)
惠英(北京医院)
金敏娟(浙江省湖州市妇幼保健院)
马颖(中国医科大学附属盛京医院)
雷小敏(三峡大学附属仁和医院)
李佩玲(哈尔滨医科大学附属第二医院)
林元(福建省妇幼保健院)
吕淑兰(西安交通大学医学院第一附属医院)
罗敏(北京协和医院)
穆玉兰(山东省立医院)
任慕兰(东南大学附属中大医院)
阮祥燕(首都医科大学附属北京妇产医院)
史惠蓉(郑州大学第一附属医院)
舒宽勇(江西省妇幼保健院)
唐良萏(重庆医科大学附属第一医院)
王世宣(华中科技大学同济医学院附属同济医院)
吴洁(南京医科大学第一附属医院)
谢梅青(中山大学孙逸仙纪念医院)
徐春琳(河北医科大学第二医院)
徐克惠(四川大学华西第二医院)
徐苓(北京协和医院)
杨欣(北京大学人民医院)
阴春霞(长春市妇产医院)
郁琦(北京协和医院)
张绍芬(复旦大学附属妇产科医院)
张淑兰(中国医科大学附属盛京医院)
张学红(兰州大学第一医院)
张雪玉(宁夏医科大学总医院)
张治芬(杭州市妇产科医院)
周红林(昆明医科大学第二附属医院)
朱瑾(复旦大学附属妇产科医院)
主要执笔人
谢梅青(中山大学孙逸仙纪念医院)
陈蓉(北京协和医院)
任慕兰(东南大学附属中大医院)
参考文献
[1]de Villiers TJ, Hall JE, Pinkerton JV, et al. Revised Global Consensus Statement on Menopausal Hormone Therapy[J]. Climacteric,2016,19:313- 315.
[2]Baber RJ, Panay N, Fenton A. 2016 IMS Recommendations on women’s midlife health and menopause hormone therapy[J]. Climacteric,2016,19:109- 150.
[3]中华医学会妇产科学分会绝经学组.绝经期管理与激素补充治疗临床应用指南(2012版)[J]. 中华妇产科杂志,2013,48:795- 799.
[4]Royal College of Obstetricians and Gynaecologists.Development of RCOG Greentop Guidelines (Clinical Governance Advice No. 1)[EB/OL]. https://www.rcog.org.uk/green-top-development.
[5]Harlow SD, Gass M, Hall JE, et al. Executive summary of the Stages of Reproductive Aging Workshop +10: addressing the unfinished agenda of staging reproductive aging[J]. Climacteric,2012,15:105- 114.
[6]中国营养学会.中国居民膳食指南(2016)[M].北京:人民卫生出版社,2016:10- 11.
[7]The NAMS 2017 Hormone Therapy Position Statement Advisory Panel. The 2017 hormone therapy position statement of The North American Menopause Society[J]. Menopause,2017,24:728- 753.
[8]Committee on Gynecologic Practice. Committee Opinion No. 698: Hormone Therapy in Pri-mary Ovarian Insufficiency[J]. Obstet Gynecol,2017,129:e134-e141.
[9]Sarri G, Davies M, Lumsden MA, et al.Diagnosis and management of menopause: summary of NICE guidance[J].BMJ,2015,351:h5746.
[10]Rossouw JE, Anderson GL, Prentice RL, et al. Risks and benefits of estrogen plus progestin in healthy postmenopausal women: principal results From the Women’s Health Initiative random-ized controlled trial[J]. JAMA,2002,288:321- 333.
[11]Moen MH, Rees M, Brincat M, et al. EMAS position statement: managing the menopause in women with a past history of endometriosis[J]. Maturitas,2010,67:94- 97.
[12]Gallos ID, Shehmar M, Thangaratinam S, et al. Oral progestogens vs levonorgestrel-releasing intrauterine system for endometrial hyperplasia: a systematic review and metaanalysis[J]. Am J Obstet Gynecol,2010,203:541- 547.
[13]American College of Obstetricians and Gynecologists. ACOG committee opinion no. 556: Postmenopausal estrogen therapy: route of administration and risk of venous thromboembolism[J]. Obstet Gynecol,2013,121:887- 890.
[14]Bergendal A, Kieler H, Sundstrom A, et al. Risk of venous thromboembolism associated with local and systemic use of hormone therapy in peri- and postmenopausal women and in relation to type and route of administration[J]. Menopause,2016,23:593- 599.
[15]Liu B, Beral V, Balkwill A, et al. Gallbladder disease and use of transdermal versus oral hormone replacement therapy in postmenopausal women: prospective cohort study[J]. BMJ,2008,337:a386.
[16]Canonico M. Hormone therapy and hemostasis among postmenopausal women: a review[J]. Menopause,2014,21:753- 762.
[17]马薇,金泉秀,吴云飞,等.乳腺增生症诊治专家共识[J].中国实用外科杂志,2016,36:759- 762.
[18]Rebbeck TR, Friebel T, Wagner T, et al. Effect of short-term hormone replacement therapy on breast cancer risk reduction after bilateral prophylactic oophorectomy in BRCA1 and BRCA2 mutation carriers: the PROSE Study Group[J]. J Clin Oncol,2005,23:7804- 7810.
[19]Cummings SR, Ettinger B, Delmas PD, et al. The effects of tibolone in older postmenopausal women[J]. N Engl J Med,2008,359:697- 708.
[20]Somboonporn W, Panna S, Temtanakitpaisan T, et al. Effects of the levonorgestrel-releasing intrauterine system plus estrogen therapy in perimenopausal and postmenopausal women: systematic review and meta-analysis[J]. Menopause,2011,18:1060- 1066.
[21]中华医学会妇产科学分会绝经学组.绝经相关激素补充治疗的规范诊疗流程[J].中华妇产科杂志,2013,48:155- 158.
[22]de Villiers TJ, Stevenson JC. The WHI: the effect of hormone replacement therapy on fracture prevention[J]. Climacteric,2012,15:263- 266.
[23]Hawkes N. HRT increases risk of blood clots and stroke, finds new analysis[J]. BMJ,2015,350:h1336.
[24]L’Hermite M. HRT optimization, using transdermal estradiol plus micronized progesterone, a safer HRT[J]. Climacteric,2013,16:44- 53.
[25]Schierbeck LL, Rejnmark L, Tofteng CL, et al. Effect of hormone replacement therapy on cardiovascular events in recently postmenopausal women: randomised trial[J]. BMJ,2012,345:e6409.
[26]Harman SM, Black DM, Naftolin F, et al. Arterial imaging outcomes and cardiovascular risk factors in recently meno-pausal women: a randomized trial[J]. Ann Intern Med,2014,161:249- 260.
[27]Hodis HN, Mack WJ, Henderson VW, et al. Vascular Effects of Early versus Late Postmeno-pausal Treatment with Estradiol[J]. N Engl J Med,2016,374:1221- 1231.
[28]Gleason CE, Dowling NM, Wharton W, et al. Effects of Hormone Therapy on Cognition and Mood in Recently Postmenopausal Women: Findings from the Randomized, Controlled KEEPS-Cognitive and Affective Study[J]. PLoS Med,2015,12:e1001833, e1001833.
[29]Bitoska I, Krstevska B, Milenkovic T, et al. Effects of Hormone Replacement Therapy on Insulin Resistance in Postmenopausal Diabetic Women[J]. Open Access Maced J Med Sci,2016,4:83- 88.
[30]Stuenkel CA. Menopause, hormone therapy and diabetes[J]. Climacteric,2017,20:11- 21.
[31]Maggiolini M, Picard D. The unfolding stories of GPR30, a new membrane-bound estrogen receptor[J]. J Endocrinol,2010,204:105- 114.
[32]Greising SM, Baltgalvis KA, Lowe DA, et al. Hormone therapy and skeletal muscle strength: a meta-analysis[J]. J Gerontol A Biol Sci Med Sci,2009,64:1071- 1081.
[33]Davey DA. Menopausal hormone therapy: a better and safer future[J]. Climacteric,2018:1- 8. doi: 10.1080/13697137.2018.1439915. [Epub ahead of print].
[34]Kotsopoulos J, Gronwald J, Karlan BY, et al. Hormone Replacement Therapy After Oopho-rectomy and Breast Cancer Risk Among BRCA1 Mutation Carriers[J]. JAMA Oncol,2018. doi: 10.1001/jamaoncol.2018.0211. [Epub ahead of print].
[35]Stute P, Wildt L, Neulen J. The impact of micronized progesterone on breast cancer risk: a systematic review[J]. Climacteric,2018,21:111- 122.
[36]Crandall CJ, Hovey KM, Andrews C, et al. Comparison of clinical outcomes among users of oral and transdermal estrogen therapy in the Women’s Health Initiative Observational Study[J]. Menopause,2017,24:1145- 1153.
[37]Sjogren LL, Morch LS, Lokkegaard E. Hormone replacement therapy and the risk of endome-trial cancer: A systematic review[J]. Maturitas,2016,91:25- 35.
[38]Jaakkola S, Pukkala E, K Lyytinen H, et al. Postmenopausal estradiol-progestagen therapy and risk for uterine cervical cancer[J]. Int J Cancer,2012,131:E537-E543.
[39]Bassuk SS, Manson JE. Oral contraceptives and menopausal hormone therapy: relative and attributable risks of cardiovascular disease, cancer, and other health outcomes[J]. Ann Epidemiol,2015,25:193- 200.
[40]Beral V, Gaitskell K, Hermon C, et al. Menopausal hormone use and ovarian cancer risk: individual participant meta-ana-lysis of 52 epidemiological studies[J]. Lancet,2015,385:1835- 1842.
[41]Manson JE, Chlebowski RT, Stefanick ML, et al. Menopausal hormone therapy and health outcomes during the intervention and extended poststopping phases of the Women’s Health Initiative randomized trials[J]. JAMA,2013,310:1353- 1368.
[42]Schwartz AG, Ray RM, Cote ML, et al. Hormone Use, Reproductive History, and Risk of Lung Cancer: The Women’s Health Initiative Studies[J]. J Thorac Oncol,2015,10:1004- 1013.
[43]Grodstein F, Martinez ME, Platz EA, et al. Postmenopausal hormone use and risk for colorec-tal cancer and adenoma[J]. Ann Intern Med,1998,128:705- 712.
[44]Grodstein F, Newcomb PA, Stampfer MJ. Postmenopausal hormone therapy and the risk of colorectal cancer: a review and meta-analysis[J]. Am J Med,1999,106:574- 582.
[45]Prentice RL, Pettinger M, Beresford SA, et al. Colorectal cancer in relation to postmenopau-sal estrogen and estrogen plus progestin in the Women’s Health Initiative clinical trial and obser-vational study[J]. Cancer Epidemiol Biomarkers Prev,2009,18:1531- 1537.
[46]Manson JE, Chlebowski RT, Stefanick ML, et al. Meno-pausal hormone therapy and health outcomes during the intervention and extended poststopping phases of the Women’s Health Initiative randomized trials[J]. JAMA,2013,310:1353- 1368.
[47]Mcglynn KA, Sahasrabuddhe VV, Campbell PT, et al. Reproductive factors, exogenous hor-mone use and risk of hepatocellular carcinoma among US women: results from the Liver Cancer Pooling Project[J]. Br J Cancer,2015,112:1266- 1272.
[48]Camargo MC, Goto Y, Zabaleta J, et al. Sex hormones, hormonal interventions, and gastric cancer risk: a meta-analysis[J]. Cancer Epidemiol Biomarkers Prev,2012,21:20- 38.
[49]Brusselaers N, Maret-Ouda J, Konings P, et al. Menopausal hormone therapy and the risk of esophageal and gastric cancer[J]. Int J Cancer,2017,140:1693- 1699.
[50]Maclennan AH, Broadbent JL, Lester S, et al. Oral oestrogen and combined oestrogen/progestogen therapy versus placebo for hot flushes[J]. Cochrane Database Syst Rev,2004:D2978.
[51]Cintron D, Lahr BD, Bailey KR, et al. Effects of oral versus transdermal menopausal hormone treatments on self-reported sleep domains and their association with vasomotor symptoms in recently menopausal women enrolled in the Kronos Early Estrogen Prevention Study (KEEPS)[J]. Menopause,2018,25:145- 153.
[52]Loprinzi CL, Sloan J, Stearns V, et al. Newer antidepressants and gabapentin for hot flashes: an individual patient pooled analysis[J]. J Clin Oncol,2009,27:2831- 2837.
[53]Toulis KA, Tzellos T, Kouvelas D, et al. Gabapentin for the treatment of hot flashes in women with natural or tamoxifen-induced menopause: a systematic review and meta-analysis[J]. Clin Ther,2009,31:221- 235.
[54]陈蓉,郁琦.香芍颗粒临床应用指导建议[J].中国实用妇科与产科杂志,2015,31:419- 420.
[55]李存存,王晶晶,陈潮,等.坤泰胶囊与激素替代疗法治疗更年期综合征有效性和安全性比较的Meta分析[J]. 中国中西医结合杂志,2013,33:1183- 1190.
[56]中华医学会妇产科学分会绝经学组.莉芙敏临床应用指导建议[J].中国实用妇科与产科杂志,2012,28:556- 557.
[57]Gaudard AM, Silva DSS, Puga ME, et al. Bioidentical hormones for women with vasomotor symptoms[J]. Cochrane Database Syst Rev,2016,(8):D10407.
[58]Lethaby A, Marjoribanks J, Kronenberg F, et al. Phytoestrogens for menopausal vasomotor symptoms[J]. Cochrane Database Syst Rev,2013,(12):D1395.
[59]Carmody J, Crawford S, Churchill L. A pilot study of mindfulness-based stress reduction for hot flashes[J]. Menopause,2006,13:760- 769.
[60]Carmody JF, Crawford S, Salmoirago-Blotcher E, et al. Mindfulness training for coping with hot flashes: results of a randomized trial[J]. Menopause,2011,18:611- 620.
[61]Stuenkel CA, Davis SR, Gompel A, et al. Treatment of Symptoms of the Menopause: An Endocrine Society Clinical Practice Guideline[J]. J Clin Endocrinol Metab,2015,100:3975- 4011.
[62]Faubion SS, Larkin LC, Stuenkel CA, et al. Management of genitourinary syndrome of menopause in women with or at high risk for breast cancer: consensus recommendations from The North American Menopause Society and The International Society for the Study of Women’s Sexual Health[J]. Menopause,2018,25:596- 608.
[63]Gandhi J, Chen A, Dagur G, et al. Genitourinary syndrome of menopause: an overview of clinical manifestations, pathophysiology, etiology, evaluation, and management[J]. Am J Obstet Gynecol,2016,215:704- 711.
[64]Caretto M, Giannini A, Russo E, et al. Preventing urinary tract infections after menopause without antibiotics[J]. Maturitas,2017,99:43- 46.
[65]Castro RA, Arruda RM, Bortolini MA. Female urinary incontinence: effective treatment strategies[J]. Climacteric,2015,18:135- 141.
[66]Chughtai B, Forde JC, Buck J, et al. The concomitant use of fesoterodine and topical vaginal estrogen in the management of overactive bladder and sexual dysfunction in postmenopausal women[J]. Post Reprod Health,2016,22:34- 40.
[67]Appa AA, Creasman J, Brown JS, et al. The impact of multimorbidity on sexual function in middle-aged and older women: beyond the single disease perspective[J]. J Sex Med,2014,11:2744- 2755.
[68]Iglesia CB. What’s new in the world of postmenopausal sex?[J]. Curr Opin Obstet Gynecol,2016,28:449- 454.
[69]Pines A, Sturdee DW, Maclennan AH. Quality of life and the role of menopausal hormone therapy[J]. Climacteric,2012,15:213- 216.
[70]Biglia N, Maffei S, Lello S, et al. Tibolone in post-menopausal women: a review based on recent randomised controlled clinical trials[J]. Gynecol Endocrinol,2010,26:804- 814.
[71]Wierman ME, Arlt W, Basson R, et al. Androgen therapy in women: a reappraisal: an Endocrine Society clinical practice guideline[J]. J Clin Endocrinol Metab,2014,99:3489- 3510.
[72]Linton A, Golobof A, Shulman LP. Contraception for the perimenopausal woman[J]. Climacteric,2016,19:526- 534.
[73]Webber L, Davies M, Anderson R, et al. ESHRE Guideline: management of women with premature ovarian insufficiency[J]. Hum Reprod,2016,31:926- 937.
[74]中华医学会妇产科学分会绝经学组.早发性卵巢功能不全的激素补充治疗专家共识[J].中华妇产科杂志,2016,51:881- 886.
[75]Sternfeld B, Wang H, Quesenberry CJ, et al. Physical activity and changes in weight and waist circumference in midlife women: findings from the Study of Women’s Health Across the Nation[J]. Am J Epidemiol,2004,160:912- 922.
[76]Sullivan SD, Sarrel PM, Nelson LM. Hormone replacement therapy in young women with primary ovarian insufficiency and early menopause[J]. Fertil Steril,2016,106:1588- 1599.
[77]Bidet M, Bachelot A, Bissauge E, et al. Resumption of ovarian function and pregnancies in 358 patients with premature ovarian failure[J]. J Clin Endocrinol Metab,2011,96:3864- 3872.
[78]Cartwright B, Robinson J, Seed PT, et al. Hormone Replacement Therapy Versus the Combined Oral Contraceptive Pill in Premature Ovarian Failure: A Randomized Controlled Trial of the Effects on Bone Mineral Density[J]. J Clin Endocrinol Metab,2016,101:3497- 3505.
2018 Chinese Guidelineon Menopause Managementand Menopause Hormone Therapy
Menopause Group, Obstertrics and Gynecology Branch, Chinese Medical Association
Department of Obstetrics and Gynecology, Peking Union Medical College Hospital, Chinese Academy of Medical Sciences &Peking Union Medical College, Beijing 100730, China
Corresponding author:YU Qi Tel: 010- 69155012,E-mail:yuqimd@163.com
【Abstract】This guideline has been announced by experts of Menopause Group, Obstetrics and Gynecology Branch, Chinese Medical Association on menopause management and menopause hormone therapy (MHT) to help healthcare professionals in optimizing their management of transitionally menopausal and postmenopausal women. New results on MHT and menopause management after 2012 as well as all of the important information from main international guidelines were reviewed. Levels of evidence and grades of recommendations were also included. The standardized MHT flowcharts of diagnosis and treatment were retained and improved from the last version. The menopause staging system, Stages of Reproductive Aging Workshop +10 (STRAW+10), was added to facilitate the understanding on clinical, biological, and endocrine changes in the reproductive aging process for doctors in this field. Vasomotor symptoms (VMS), genitourinary syndrome of menopause, and prevention of menopause-related low bone mass and osteoporosis were reconfirmed as the indications for MHT. The risks of MHT depend on types, dosages, time of use, management, start-up time, and whether progesterone is used. To maximize the benefits and minimize the risks, MHT should be individualized based on the updated evidence, and the benefit-risk ratio should be reassessed annually. For women within 10 years after menopause, or younger than 60 years old with no contraindications, MHT for the treatment of VMS and prevention of bone loss and fractures has the most favorable benefit-risk ratio. Premature ovarian insufficiency patients should be treated with hormone replacement therapy till the average age of natural menopause and followed by the postmenopausal MHT.
【Keywords】guideline; menopause; menopause hormone therapy; hormone replacement therapy; vasomotor symptoms;breast cancer; cardiovascular disease; cognition; genitourinary syndrome of menopause
MedJPUMCH,2018,9(6):512-525
本指南同期发布于《中华妇产科杂志》2018年第11期
基金项目:中国医学科学院医学与健康科技创新工程(2017- 12M- 1- 002);国家重点研究发展计划(973计划) (2018YFC1002105)
DOI:10.3969/j.issn.1674-9081.2018.06.007
【文章编号】1674-9081(2018)06-0512-14
【文献标志码】A
【中图分类号】R711
通信作者:郁琦电话:010- 69155012,E-mail:yuqimd@163.com中国医学科学院北京协和医学院北京协和医院妇产科,北京100730
本文为转载文章,如有侵权请联系作者删除。本文仅供健康科普使用,不能做为诊断、治疗的依据,请谨慎参阅
发表于:2020-10-16