科室医生 查看全部
科普·直播义诊专区 查看全部
- 精选 有时,仅仅治愈是不够的!
最近经历了两例病例,有些触动,在对患儿生殖保存的方面,我们是不是应当多考虑一些,再往前走一步或许会更好,与患儿,与家属。Case 1:男孩,12岁,前T淋巴母细胞淋巴瘤,经过大剂量化疗,临床治愈,19岁结婚,配偶孕3个月,胎心消失流产,后一直不孕,精子检测提示数量低下;Case 2:女孩,2岁,盆腔原始神经外胚叶瘤,经过两次手术和15个疗程化疗,第二次手术时,切除了右侧受累的卵巢,临床治愈,12岁时,左侧附件区再次出现巨大囊性占位,术前一直担心囊肿来源于左侧卵巢,如何尽可能保留部分卵巢组织成为优先考虑,幸运的是囊肿为输卵管旁囊肿,卵巢得以保留,但输卵管被切除,失去自然受孕的机会,假如肿物来源于左侧卵巢,又是恶性,我们又该如何抉择和面对?实际上,在生殖保存方面,还是有些办法现实可行:1 睾丸或卵巢解剖上“移位”:对于会阴部及阴囊内恶性占位,术后需要瘤床放疗,睾丸会在放疗视野内,我们可以先行手术,将睾丸移位至腹壁皮下,放疗结束后,再回移至阴囊;女孩盆腔恶性肿瘤,术后需要放疗,卵巢不可避免会受影响,术中我们可以将卵巢上移或外移至瘤床外,并在其周围缝扎2到4枚鈦夹作为标记,这样在描绘靶区时可以把它画在靶区外。2 精子或卵巢组织冻存:对于青春期的男孩,借助于Sperm Banking是完全可行的;对于女孩,冻存卵母细胞或卵巢组织有一定困难,但不乏成功案例,目前国内北京妇产科医院建有卵巢组织冻存库,术中我们可以切取卵巢1/4组织予以冻存,将来需要时可以回植于患儿体内。
王景福 主任医师 山东第一医科大学附属肿瘤医院 儿童肿瘤科6134人已读 - 精选 肿瘤患儿可以要下一代吗?
肿瘤患儿父母或到了孕龄期的“患儿”总是要问而且又无法回避的问题:患儿的下一代会不会生出一个病孩,或者说比别人风险更大?2012在特牛CA: A Cancer Journal for Clinicians上有一篇综述总结了两项研究结果,其结论是:接受过放化疗治疗的患儿,成年后其下一代患有遗传病或先天畸形的风险没有增加,希望能够部分回答患儿、父母及临床医生对生殖方面的关切。但我们还是要持谨慎态度,因为放疗和化疗一定会给患儿带来某些基因突变,尤其生殖系统接受过放疗治疗,存在遗传给下一代的风险,我们还需对下一代进行更长时间的跟踪观察,包括寿命、成年癌等。此外,患儿父母还经常问:我再生一个孩子,还会得肿瘤?是不是机会更大?我的观点是:如果脱离致癌环境,做好孕期保健,再生一个同样肿瘤患儿的几率不会比正常人群高。原因是:儿童肿瘤多为散发病例,突变多发生在肿瘤细胞,极少伴有体细胞或生殖细胞突变,所以遗传倾向和家族集聚性极弱。除了个别肿瘤,比如存在体细胞RB1基因突变的视网膜母细胞瘤或PHOX2B突变的神经母细胞瘤,第二胎发生同类肿瘤的风险明显增加,但我们可以借助遗传咨询提前预知。参考:CA: A Cancer Journal for Clinicians Volume 62, Issue 3, pages 145-146, 12 MAR 2012.
 王景福 主任医师 山东第一医科大学附属肿瘤医院 儿童肿瘤科4161人已读
王景福 主任医师 山东第一医科大学附属肿瘤医院 儿童肿瘤科4161人已读 - 精选 Wilms Tumor:手术“能切”和“切对了”是两码事
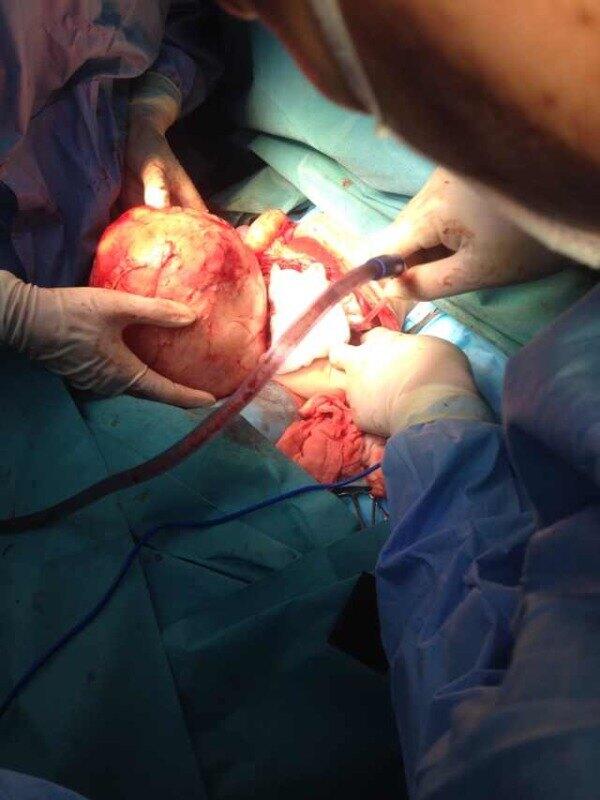
肾母细胞瘤发生局部淋巴结广泛转移比例相对较低,所以手术切除难度不大,一般医院都可完成。但是门诊我们经常会遇到这样术后的病人:区域性淋巴结没有活检,肿瘤是否侵出包膜或腹腔有无种植转移没有记录,这些直接影响肿瘤分期,进而影响方案选择;术中肿瘤破裂,保护不当,发生肿瘤细胞播散,人为提升肿瘤分期。是能切了,但是没切对,存在诸多不妥。那我们该如何做,下面是我们应当遵循的一些原则: 1、手术的目的:完整切除肿瘤,术中避免出现肿瘤细胞外溢;评估肿瘤累及范围,精确分期。 2、手术切口:经腹部或胸腹联合切口,经腰背部切口应避免,因其:暴露有限,操作困难;无法完成肿瘤累及范围评估。 3、能够切除的肿瘤:术前穿刺活检或术中切开活检应避免,因为存在提升肿瘤分期的风险。 4、术中探查:对侧肾脏常规探查是没有必要的,除非术前影像学检查提示对侧可能受累。 5、输尿管受累:术前尿液中存在血凝块、出现梗阻性肾盂积水或无功能肾,应行膀胱镜检查,术中应采取肿物连同受累输尿管整块切除(En bloc resection)。 6、不建议行部分肾切除,除非下列情况:存在发展成双侧肾母细胞瘤潜在风险( Wilms Tumor 相关综合征),肿瘤体积较小;孤立肾;马蹄肾; 新生儿伴有Denys-Drash或Frasier综合征,目的是延期透析。 7、双侧肾母细胞瘤:尽可能保留正常肾组织;肾移植推迟到肿瘤切除术后1-2年,确定无肿瘤复发和转移。 8、淋巴结活检:应行肾门或腹主动脉旁的淋巴结活检,即使外观提示可能正常。 9、术中标记:瘤床范围及转移的淋巴结应用钛夹或银夹进行标记,指导术后放疗计划制定。 本文系王景福医生授权好大夫在线(www.haodf.com)发布,未经授权请勿转载。
 王景福 主任医师 山东第一医科大学附属肿瘤医院 儿童肿瘤科4089人已读
王景福 主任医师 山东第一医科大学附属肿瘤医院 儿童肿瘤科4089人已读
问诊记录 查看全部
- 松果体非生殖细胞瘤性生殖细胞肿瘤 2022年9月底间断性呕吐,10月初到医院误判为消化疾病,以... 第一次手术切除含生殖成份、卵黄囊成份的成熟畸胎瘤后,经过康复治疗,化疗、放疗,放疗3月后卵黄囊肿瘤复...总交流次数7已给处置建议
- 室管膜瘤 室管膜瘤三级后颅窝型,已经手术切除,正在进去化疗和靶向治疗,... 室管膜瘤三级后颅窝型,已经手术切除,正在进去化疗和靶向治疗,想咨询一下质子放疗。总交流次数19已给处置建议
- 肾母细胞瘤二期,手术做了,左肾肿瘤摘除 肾母细胞瘤二期,想过去化疗,手术已经做了,左肾和肿瘤已经全部... 什么时候可以去就诊,可以去做化疗。总交流次数4已给处置建议
- 患者:男 6岁10个月 最近增强检查右肾有不明物 最后交流时间 2023.10.10最近增强检查右肾有不明物 19号做了第二次切除手术、29号开始上化疗 做了派特没有转移、这种的话还有机会吗总交流次数11已给处置建议
- 神经母细胞瘤 神经母细胞瘤腹膜后恶性肿物化疗三次肿瘤明显缩小, 想问一下别的地方采干细胞,山东肿瘤医院给移植吗总交流次数9已给处置建议
总访问量 725,461次
在线服务患者 455位
科普文章 25篇







