科室介绍 查看全部
科普·直播义诊专区 查看全部
- 精选 【典型病例】骶骨巨大神经鞘瘤外科手术1例
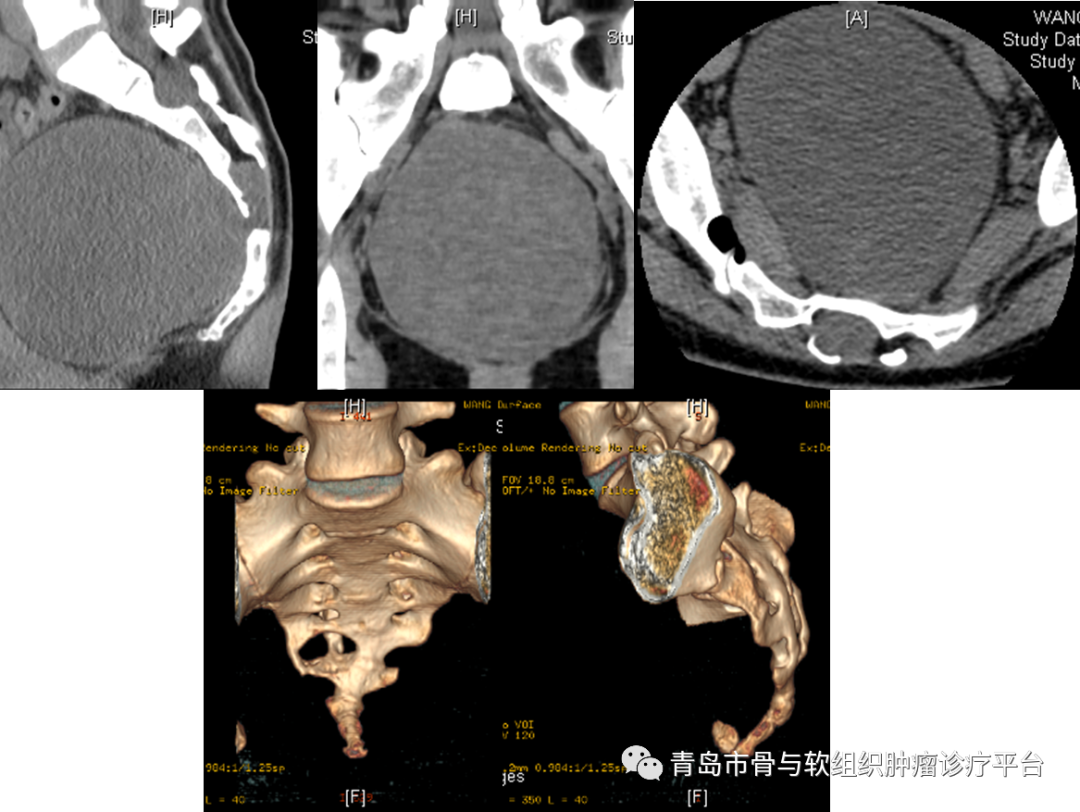
病例简介患者王某某,女性,27岁。主诉:发现骶尾部肿物4月余。现病史:发现骶尾部肿物4月余,无疼痛不适,大小便功能正常,会阴区无明显麻木不适。外院行骶尾部MR示:骶管内及骶椎前占位,脊索瘤?神经源性肿瘤?为求进一步治疗就诊于我院,门诊以“骶尾部肿物”收治入院,患者自患病以来,精神可,饮食睡眠可,大小便未见明显异常,体重未见明显变化。查体:双下肢活动及感觉可,双侧伸髋、屈髋、伸膝、屈膝活动可。骶尾部无明显压痛、叩击痛,会阴区无明显麻木不适。目前诊断:骶尾部占位性病变术前检查术前骶尾部T2相MRI平扫术前骶尾部MRI增强平扫术前骶尾部CT三维成像术前讨论1. 骶前巨大肿瘤,考虑为脊索瘤或神经鞘瘤可能大。切除过程中使用超声骨刀行骶骨截骨,有效降低术中出血风险。2. 术中需要充分保护双侧S3神经根,降低术后患者出现大小便功能异常的风险。术后关注患者大小便功能,早期康复锻炼。3. 骶前区有一层松散的组织,尽量使用钝性分离直肠,避免出现不必要的损伤。4.手术切除后存在较大空腔,感染风险较大。术前需要进行预防性使用抗生素,术前12h行清洁灌肠。术后关注引流情况。手术过程术后病理肉眼所见:灰白结节样物一枚,带部分骨组织,结节大小1110.79.5cm,距骨断端1.5cm,骨组织大小107.22cm,切面灰白灰黄质稍韧,部分呈胶冻样,包膜完整。病理诊断:(骶骨肿瘤)神经鞘瘤(大小1110.79.5cm),部分区域水肿、退变,局灶区域边界欠清,侵及骨组织,建议密切随访复查。免疫组化结果:S-100(+),SOX10(+),CK(-),Brachyury(-),H3K27Me3(+,表达未缺失),Ki-67(+,2%),Desmin(-),INI-1(+,表达未缺失),CD34(部分+),EMA(-)。病例总结涉及骶骨的肿瘤主要包括原发性和转移性肿瘤。转移性肿瘤较原发性肿瘤更常见。最常见的良性骶骨肿瘤是巨细胞瘤。最常见的原发性骶骨恶性肿瘤是脊索瘤,其次是软骨肉瘤。神经鞘瘤起源于神经,但其临床上与其他骶骨肿瘤类似,治疗方法也相同,被归类为骶骨肿瘤。骶骨是神经源性肿瘤的好发部位之一,绝大多数为良性周围神经鞘瘤。术前完善的影像学检查和实验室检查十分必要。被忽视的周围神经鞘瘤后期可能发展到非常巨大,导致盆腔器官功能障碍。大多数良性周围神经鞘瘤可以接受保留功能的保守手术切除治疗。需要密切关注肿瘤复发情况,必要时进行大剂量放疗控制肿瘤生长。对于恶性周围神经鞘瘤,多由神经纤维瘤病恶化而来。治疗方法包括放疗和整块手术切除。慢性神经压迫引起的慢性、钝性、下背部或尾部疼痛是骶骨肿瘤最常见的症状之一。肿瘤压迫可能导致肠道或泌尿系统习惯改变。骶骨下段肿瘤体积足够大时,直肠指诊可以触及其前部。对于较大的骶骨肿瘤,如脊索瘤和软骨肉瘤,臀部可能出现巨大肿块。高度恶性肿瘤的患者剧烈疼痛可能持续数周,行走困难,出现强迫体位等。骶骨肿瘤外科手术前需要完善影像学检查:包括平片、CT、MRI、血管造影。必要时PET-CT检查。术前需要明确切除范围,精准切除,尽可能多保留骶神经,以降低术后出现大小便功能异常的风险。Todd等研究证实,双侧S3神经保留的患者中,正常的肠和膀胱功能分别保持在100%和69%。骶骨手术术后出现的并发症包括:术中失血、感染、伤口问题(包括切口感染、皮肤或肌肉坏死、伤口愈合不良等)、直肠损伤、神经损伤(肿瘤较大时需关注坐骨神经)、脑脊液漏等。因此术前需要进行根据肿瘤范围大小,考虑术前12-24h行动脉栓塞或球囊植入,降低出血风险。术中可行控制性降压和控制性低温,以减少术中出血。术前24h预防性使用抗生素,术前12h行清洁灌肠,降低术后感染风险。近年来,青大附院骨肿瘤团队目前已常规开展各类骶骨肿瘤切除手术,大多数患者围手术期出血少,术后预后良好,目前也已经成为我科特色诊疗技术之一。
 郑炳鑫 主治医师 青岛大学附属医院 骨肿瘤科229人已读
郑炳鑫 主治医师 青岛大学附属医院 骨肿瘤科229人已读 - 精选 【团队合作】累及第1-3肋的胸壁肿瘤整块切除+胸壁重建
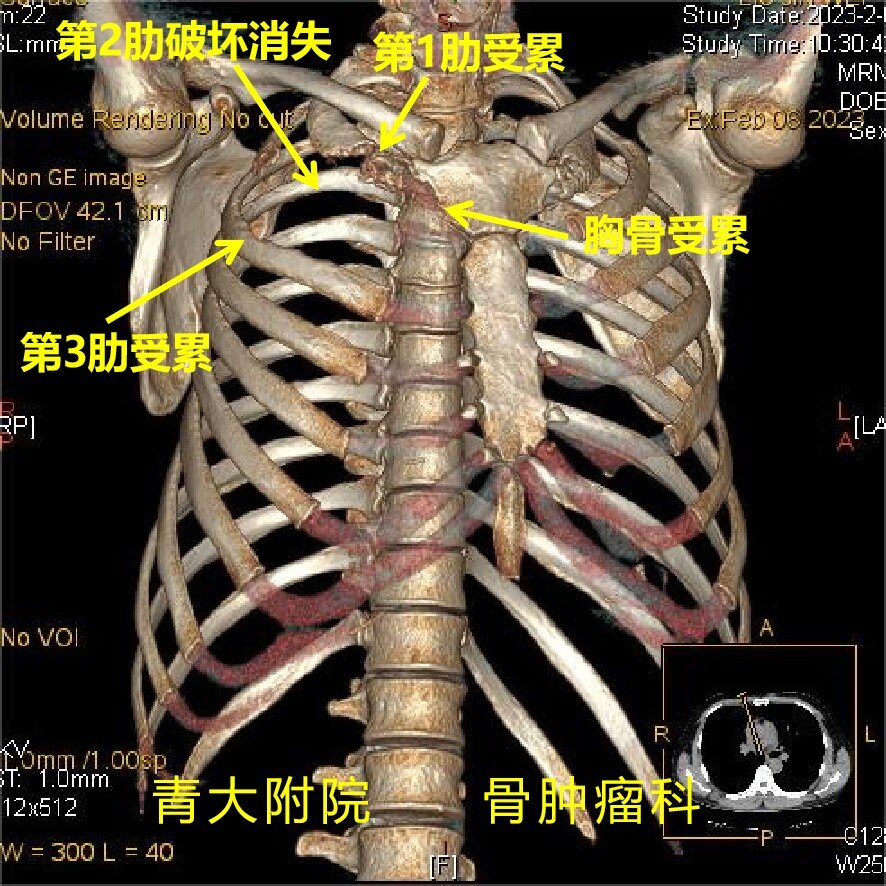
病例简介患者:刘某,男,45岁。主诉:右侧肩部不适6月,加重伴胸痛2月。现病史:患者6月前无明显诱因出现右侧肩部不适,伴疼痛,不伴肩关节活动受限,不伴上肢麻木,2月前上述症状加重,伴右侧胸前疼痛,不伴憋气及呼吸困难,后于我院就诊,行影像学检查发现右侧胸壁肿瘤,后行穿刺,病理结果示“梭形细胞恶性肿瘤,形态倾向肉瘤”。后于肿瘤科行术前辅助放疗和安罗替尼治疗,现为进一步诊治收入我科。目前诊断:右侧胸壁肿瘤术前讨论:患者右侧胸壁恶性肿瘤,累及第1-3肋,一方面:由于第1肋位置隐匿,前上方锁骨覆盖,显露困难,周围毗邻锁骨下血管及臂丛神经,肿瘤的切除难度风险较高,且肿瘤累及部分胸骨,术中需一并切除;另一方面:肿瘤突入胸腔,势必与胸膜及肺组织黏连难以分离,术中可能切除部分肺,需与胸外科共同完成手术,同时肿瘤切除后胸壁缺损巨大,需要牢靠的重建胸壁。拟行胸壁肿瘤整块切除+LARS韧带胸壁重建。术前检查胸部增强CT:右上前胸壁见团块状软组织密度影,密度较均匀,不均匀强化,边界较清,大小约89mm×58mm×60mm,边界较清,累及右侧第1-3前肋,可见骨质破坏,第二肋前段消失。体积较前部分减小。胸部MR:右侧前胸壁可见团块状混杂T1混杂T2信号影,大小约85mm×56mm×65mm,右侧第2前肋骨质明显破坏,第3前肋局部骨质破坏。术前设计肿瘤切除手术在胸外科、麻醉科、手术室等兄弟科室的保驾护航下顺利完成。术中由骨肿瘤科岳斌主任、胸外科徐林浩主任完成右侧胸壁(第1-3肋+部分胸骨)及部分累及的肺组织一期完整切除,同时利用LARS人工韧带重建胸壁缺损,未出现并发症!术后病理:(右胸壁)恶性肿瘤,意见为恶性间皮瘤(局限性,肉瘤样,大小874cm),肿瘤侵犯肋骨,部分区域与肺膜粘连,但未侵至肺实质未累及骨断端及肺断端。免疫组化结果:CK(-),WT-1(灶+),Calretinin(+),D2-40(+),Brg1(+,未缺失),CD34(-),STAT6(-),MUC-4(-),SATB2(弱+),S-100(-),Desmin(-),GATA3(-)。病例总结胸壁肿瘤可为良性或恶性,可原发于胸壁,也可源于原发性肺肿瘤或转移病灶的直接扩张,原发性胸膜恶性肿瘤也可侵犯胸壁。胸壁肿瘤切除术是对外科医生具有挑战的手术,尤其颈胸交界处的胸壁肿瘤,周围重要的血管神经众多,深面毗邻胸腔内重要脏器,可能导致严重的术后肺功能不全、血管神经损伤等。约55%的胸壁肿瘤为恶性,包括软骨肉瘤、恶性纤维瘤、恶性间皮瘤等。胸壁原发恶性肿瘤通常需行局部扩大切除术,肿瘤的整块切除可提高患者无进展生存率和总生存率。本例患者中肿瘤位于胸前壁,肿瘤体积较大,侵犯三根肋骨及部分胸骨。我们选择使用LARS人工韧带重建胸壁缺损。LARS(LigamentAdvancedReinforcementSystem)是一种人工合成的韧带增强及重建材料,其设计依据“仿生学原理”,内部结构与人体正常的韧带纤维结构相似,关节内的纵形纤维有弹性但不会被拉长,有强大的抗疲劳能力并允许人体细胞长入,从而达到修复重建的目的。本例手术中,我们将LARS韧带分别缝合固定到第1-3肋和胸骨残端,同时将胸壁肌肉缝合固定到Lars韧带,实现了良好的软组织覆盖,弹性并牢固的重建患者胸壁。近年来,青大附院骨肿瘤科骨肿瘤MDT模式不断推广与成熟,除了与影像科、病理科、肿瘤内科、放疗科、介入科等专业定期开展疑难病例讨论,也与胸外科、血管外科、胃肠外科、泌尿外科等兄弟科室建立联合手术模式,为胶东半岛骨与软组织肿瘤疑难疾病的诊疗提供新的平台和希望。改善了患者的生存质量,延长了患者的生存期,目前已成为我科的特色医疗技术之一。
 郑炳鑫 主治医师 青岛大学附属医院 骨肿瘤科99人已读
郑炳鑫 主治医师 青岛大学附属医院 骨肿瘤科99人已读 - 精选 【典型病例】胸壁巨大软骨肉瘤切除+人工韧带重建胸壁术1例
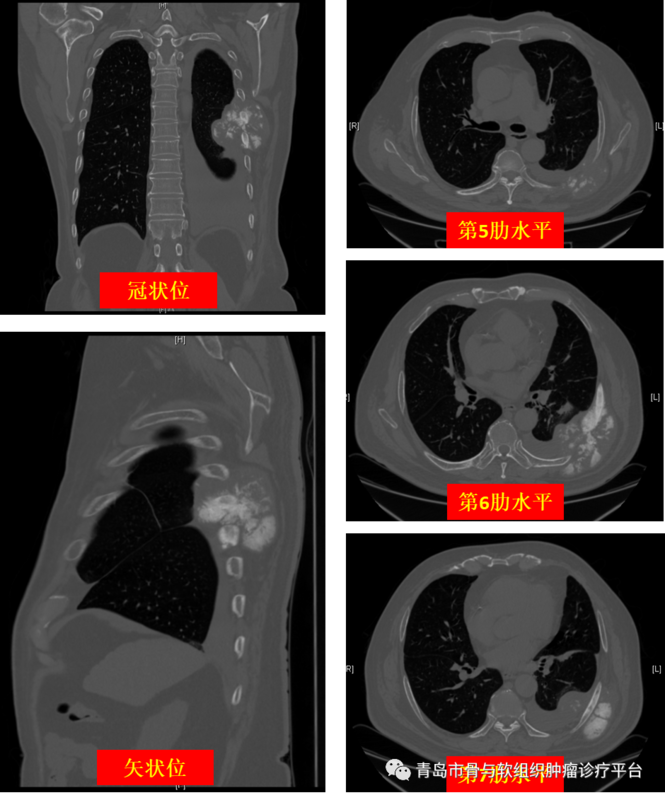
【患者情况】患者张某某,男,62岁。主诉:发现左胸壁肿物10余天。现病史:患者10余天前无明显诱因发现左侧胸后壁肿物,肿物呈进行性增大,质地较硬,轻度疼痛。就诊于外院,外院行胸部CT示左侧6、7肋并周围软组织明显占位。为求进一步治疗,就诊于我院平度院区,行穿刺活检,考虑为软骨肉瘤不能排除。为求进一步治疗,就诊于我科。患者自发病来,饮食睡眠可,大小便正常,体重无明显变化。目前诊断:左侧胸壁巨大软骨肉瘤。手术方案:左侧胸壁肿瘤切除+肋骨肿瘤切除+人工韧带胸壁重建术【术前检查】胸部(肋骨)CT三维成像提示左侧第6肋骨占位性病变,肿瘤侵犯胸膜。胸部增强CT提示肿瘤未侵及重要血管神经。【穿刺病理】患者(左胸壁、左胸膜)送检穿刺组织两处,均为软骨组织伴钙化,部分区域软骨细胞增生,部分区域可见卵圆形细胞及梭形细胞,细胞密度增加,结合影像学,考虑软骨肉瘤。【手术过程】为避免肺损伤,对该患者采取术中单肺通气。术野可见肿瘤组织,肿瘤组织质地较硬,色发白,大小约10cm8cm8cm,累及第5-7肋,肿瘤上缘位于肩胛骨下方。离断第5-7肋,完整切除肿瘤组织。肿瘤组织侵犯胸膜,一并切除。使用Lars韧带重建胸壁。将Lars韧带固定至第8肋、肩胛骨关节囊,将背阔肌等胸壁肌肉固定于Lars韧带。【病例总结】胸壁肿瘤可为良性或恶性,可原发于胸壁,也可源于原发性肺肿瘤或转移病灶的直接扩张,原发性胸膜恶性肿瘤也可侵犯胸壁。胸壁肿瘤切除术是对外科医生最具挑战的手术,可能导致严重的术后肺功能不全。约55%的胸壁肿瘤为恶性,其中软骨肉瘤是最常见的胸壁恶性肿瘤之一,约占原发性胸壁恶性肿瘤的30%。本例患者中,根据患者的临床表现及影像学资料,考虑为诊断为胸壁软骨肉瘤。软骨肉瘤的特征是疼痛、质地较硬及肿块固定,约10%的患者会出现同时性肺转移。软骨肉瘤通常位于胸前壁(肋骨与肋软骨交界处或胸骨),可能来源于骨软骨瘤恶变。本例患者中肿瘤位于胸后壁,肿瘤体积较大,侵犯三根肋骨。对于胸壁软骨肉瘤,手术切除是主要治疗方法,切缘无肿瘤是局部复发的最佳预测指标。切缘阴性的患者复发率为10%,而切缘阳性患者的局部复发率为75%。放疗和化疗通常对软骨肉瘤无效。胸壁肿瘤通常需行局部扩大切除术,这可提高患者无进展生存率和总生存率。在大多数病例中,包括≥3根肋骨的胸壁切除术需要使用假体材料进行重建,以保持胸壁结构,避免肺疝、胸壁矛盾运动,保护前胸壁切除下方的纵膈器官,同时提供美观的胸部轮廓。本例患者中,我们选择使用Lars人工韧带重建胸壁。LARS(LigamentAdvancedReinforcementSystem)是一种人工合成的韧带增强及重建材料,其设计依据“仿生学原理”,内部结构与人体正常的韧带纤维结构相似,关节内的纵形纤维有弹性但不会被拉长,有强大的抗疲劳能力并允许人体细胞长入,从而达到修复重建的目的。本例手术中,我们将Lars韧带分别坚固固定到第8肋、第5-7肋残端、肩胛骨关节囊,同时将胸壁肌肉缝合固定到Lars韧带,实现了良好的软组织覆盖,重建患者胸壁,以期尽量减少肺暴露和感染的风险。胸壁/腹壁肿瘤毗邻胸腔/腹腔,需要完善的术前检查评估肿瘤与胸腹腔脏器的解剖关系,同时需要术后需要进行胸壁/腹壁组织重建。近年来,青大附院骨肿瘤科团队已成功开展各类复杂巨大的胸壁/腹壁肿瘤切除重建术,越来越多的患者从中获益。参考文献1.KucharczukJC,KaiserLR.Chestwallresections.In:MasteryofCardiothoracicSurgery,2nded,KaiserLR,KronIL,SprayTL(Eds),LippincottWilliams&Wil,Philadelphia2007.p.222.2.SomersJ,FaberLP.Chondromaandchondrosarcoma.SeminThoracCardiovascSurg1999;11:270.3.TateishiU,GladishGW,KusumotoM,etal.Chestwalltumors:radiologicfindingsandpathologiccorrelation:part2.Malignanttumors.Radiographics2003;23:1491.4.FongYC,PairoleroPC,SimFH,etal.Chondrosarcomaofthechestwall:aretrospectiveclinicalanalysis.ClinOrthopRelatRes2004;:184.5.KawaguchiS,WeissI,LinPP,etal.Radiationtherapyisassociatedwithfewerrecurrencesinmesenchymalchondrosarcoma.ClinOrthopRelatRes2014;472:856.
 郑炳鑫 主治医师 青岛大学附属医院 骨肿瘤科445人已读
郑炳鑫 主治医师 青岛大学附属医院 骨肿瘤科445人已读
问诊记录 查看全部
- 左肩胛骨骨软骨瘤 10年前检查左肩胛骨那里长了软骨瘤,最近半年感觉左左肩胛骨不... 是否是病变,是否需要用药总交流次数13已给处置建议
- 患者:男 60岁 右胸肋部疼痛1月余 最后交流时间 01.16右胸肋部疼痛1月余 患者近1月前无明显原因出现右胸肋部疼痛,当地医院完善相关检查... 该肿瘤是骨肿瘤吗还是骨肉瘤? 另外是否需要等手术后取出肋骨化验才能知道是否为原发癌?取肋骨手术后能恢...总交流次数19已给处置建议
- 2年前左乳乳腺癌保乳手术,近期怀疑骨转移 2021年11月左乳乳腺癌,保乳治疗,之后进行了放疗,近期复... 请诊断一下是否确认骨转移,接下来怎么治疗总交流次数20已给处置建议
- 脊柱肿瘤 下肢无力,走路缓慢,近期摔跤后发现脊柱肿瘤 可否去您哪里门诊并手术?总交流次数21已给处置建议
- 骨转移癌 左肾肾细胞癌摘除,右肾肾盂尿路上皮癌经过两次激光消融术后,最... 医生建议pd1+靶向药治疗,老人目前胸椎骨折,很疼,是否有缓解办法,骨折恢复后是否能正常行走总交流次数17已给处置建议







