科室医生 查看全部
科普·直播义诊专区 查看全部
- 软组织肉瘤诊治中国专家共识(2015年版)
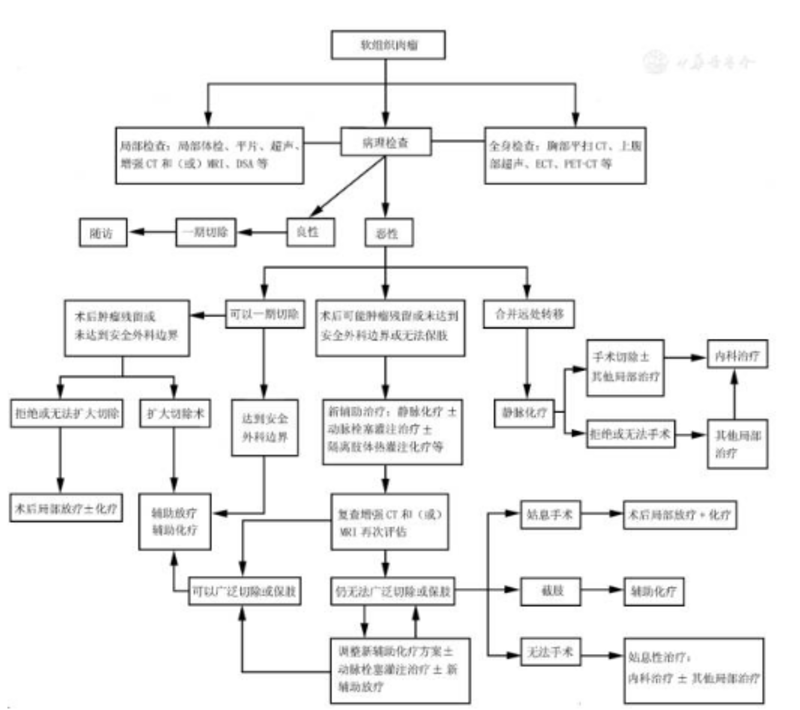
2016-05-05 中华医学网 软组织肉瘤是一组源于黏液、纤维、脂肪、平滑肌、滑膜、横纹肌、间皮、血管和淋巴管等结缔组织的恶性肿瘤,包括起源于神经外胚层的神经组织肿瘤,不包括骨、软骨和淋巴造血组织。软组织肉瘤起源于中胚层的间充质组织中的多能干细胞,各种病理类型在发生部位、转化细胞类型和组织病理学特征等方面具有鲜明异质性。 软组织肉瘤有19个组织类型和50个以上的不同亚型。各国不同类型软组织肉瘤发病率的数据不同,综合各大诊治中心的数据,其中未分化多形性肉瘤最多见(25%~35%),其次是脂肪肉瘤(25%~30%)、平滑肌肉瘤(12%)、滑膜肉瘤(10%)和恶性周围神经鞘膜瘤(6%)。 多学科综合诊治原则及流程 目前软组织肉瘤的诊治仍强调遵循多学科综合诊治原则,需要多学科综合诊治的主要是诊断疑难复杂或在治疗上各学科存在争议的软组织肉瘤患者,组织骨与软组织肉瘤外科、肿瘤内科、放疗科、影像科、病理科和介入治疗科等相关科室的专家进行讨论。根据患者的年龄、身体基本状况、病理类型和肿瘤侵犯范围等,认真阅片分析病情,依据最有利于患者疾病治疗和改善预后的原则,制订出有计划、按步骤地逐步实施的整体治疗方案,尽量让患者在治疗计划中获得最大的收益。但是对于已经获得R0切除、病理级别较低的Ⅰ级或部分Ⅱ级软组织肉瘤,术后予以定期随访或局部辅助放射治疗即可,无需所有病例均一成不变、刻板地进行多学科讨论。软组织肉瘤的多学科综合诊治流程见图1。 图1 软组织肉瘤的多学科综合诊治流程图 外科治疗 正确的外科手术是治疗软组织肉瘤最有效的方法,也是绝大多数软组织肉瘤唯一的治愈措施。手术的目标不仅是完整切除肿瘤,而且要求获取安全的外科边缘。术后功能恢复与安全边界发生矛盾时,通常以牺牲部分功能为代价。 通常,安全外科边界是指MRI显示软组织肉瘤边缘或反应区外1 cm处,手术是在保证安全外科边界基础上追求完整切除肿瘤。对于体积较大、较深或侵犯邻近大血管、神经、关节和骨骼等重要组织的肿瘤,预计一期手术难以达到根治切除,而对化放疗相对敏感的肿瘤,需要术前放化疗和介入治疗等手段使肿瘤体积缩小、坏死和形成明显的假包膜,从而为手术获得安全外科边界创造条件。 不规范的手术操作往往会导致:(1)非计划再次手术,即软组织肉瘤患者在第1次手术时,因各种原因导致肿瘤残留(R1~R2切除)或切缘未达到安全外科边界,需接受计划外再次手术;(2)人为破坏肿瘤包膜不能完整切除肿瘤;(3)活检穿刺道不包括在手术切除的范围内;(4)手术中反复挤压肿瘤组织等影响外科手术治疗的成功率。 规范的手术操作建议:(1)术前基于病理和MRI等资料制订手术方案,设计最佳瘤体取出路径和重建所需的技术准备;(2)将活检道与肿瘤作为一个整体同时切除;(3)直视下必须努力获得安全边界,必要时可以同期进行2个方向的显露,如躯干和骨盆的软组织肉瘤;(4)误入肿瘤时无论是否达到肿瘤实质,均应立即严密缝合并扩大切除;(5)贴肿瘤面切除时需要特别标记,并在术后获取切缘信息;(6)切除的标本必须标记极相,并要求病理医师出具边缘是否残留的评价报告;(7)肢体位置较深的高级别软组织肉瘤,尽量实施间室切除或间隙切除。软组织肉瘤手术不推荐常规清扫区域淋巴结,对于容易发生淋巴结转移的透明细胞肉瘤、上皮样肉瘤、血管肉瘤、胚胎型横纹肌肉瘤和未分化肉瘤等,应常规检查淋巴结。如影像学检查怀疑有淋巴结转移,应在切除原发肿瘤的同时行淋巴结清扫术,术后病理若证实区域淋巴结转移且侵及包膜外者,需要术后放疗。软组织肉瘤的综合治疗流程见图2。 图2 软组织肉瘤的综合治疗流程图 放射治疗 局部广泛切除+辅助放疗目前是可手术切除、病理高级别软组织肉瘤的标准治疗模式,放疗的疗效取决于软组织肉瘤的病理类型和肿瘤负荷量。通常,病理高级别软组织肉瘤,如尤文肉瘤和横纹肌肉瘤等对放疗的敏感性较高,肿瘤负荷量愈小放疗效果愈好。不同病理类型软组织肉瘤的放疗时机、放射野设计和射线种类与能量、照射剂量和分割方式等的选择仍有待进一步达成统一意见。 主要类型 1术后辅助放疗(1类推荐) 可以杀灭手术后残存的肿瘤细胞,减少局部复发甚至远处转移的机会。主要适应证:(1)病理高级别肿瘤;(2)肿瘤最大径>5 cm;(3)手术切缘阳性或未达到安全外科边界,肿瘤侵犯周围血管、神经;(4)肿瘤位置表浅、体积小、病理低级别、手术已达到安全外科边界者,术后辅助放疗不作推荐。 2术前放疗(2A类推荐) 对于肿瘤较大、较深,与血管神经关系密切,局部切除困难或预期无法达到安全外科边界者,术前放疗联合或序贯化疗、介入治疗等可能缩小肿瘤体积,提高R0切除或保肢治疗的概率。 3姑息性放疗 主要适应证:(1)对于经术前抗肿瘤治疗仍无法手术切除或手术可能严重影响肢体功能、无法保肢或拒绝截肢的局部晚期软组织肉瘤患者;(2)针对局部晚期无法手术切除肿瘤导致的各种并发症,如疼痛、急性脊髓压迫症和肢体功能障碍等。主要目的:(1)较长时间控制局部肿瘤生长;(2)尽量延缓或减轻局部严重症状,提高生活质量;(3)联合或序贯化疗、介入等其他治疗方法,达到延长患者总生存时间的目的。 内科治疗 化学治疗 化疗仍是当今软组织肉瘤最重要的内科治疗手段,分为新辅助化疗、辅助化疗和姑息性化疗等。 1新辅助化疗 对一期切除困难或不能获得R0切除,且对化疗敏感的成人高级别软组织肉瘤,可以使用新辅助化疗。具体适应证:①化疗相对敏感的高级别软组织肉瘤;②肿瘤体积较大,与周围重要血管神经关系密切,预计无法一期R0切除或保肢治疗;③局部复发需要二次切除或远处转移行姑息手术前。术前化疗推荐方案:阿霉素(ADM)±异环磷酰胺(IFO)方案或MAID方案(美司钠+阿霉素+异环磷酰胺+达卡巴嗪)。 隔离肢体热灌注化疗不仅能使肿瘤局部获得更高的药物浓度,还可以利用局部热效应(38℃~39℃)进一步杀灭肿瘤细胞,提高肿瘤广泛切除率、增加保肢治疗的机会,能否带来生存获益目前尚无法最终定论。隔离肢体热灌注化疗可与术前静脉化疗、放疗等治疗手段同步或序贯进行,因联合治疗不良反应较重,推荐功能状态(PS)评分0~1分、病理分级为2~3级且肿瘤体积巨大、肿瘤与重要血管神经关系密切预期常规新辅助化疗后仍难以获得R0切除或需要保肢的患者采用。 2辅助化疗 对于Ⅰ期有安全外科边界的软组织肉瘤患者,不推荐辅助化疗;对于Ⅱ~Ⅲ期患者,建议术后放疗±辅助化疗,对有以下情况的Ⅱ~Ⅲ期患者强烈推荐术后辅助化疗 (2A类推荐):(1)化疗相对敏感;(2)高级别、深部、直径>5 cm;(3)手术未达到安全外科边界或局部复发二次切除后的患者。横纹肌肉瘤建议术后辅助化疗12个周期,骨外骨肉瘤12~15个周期,骨外尤文肉瘤16~18个周期。除此以外的其他软组织肉瘤的辅助化疗一致推荐ADM±IFO方案,建议化疗6个周期。 3姑息性化疗 对于不可切除的局部晚期或转移性软组织肉瘤,积极有效的化学治疗有利于减轻症状、延长生存期和提高生活质量。对于多次多线化疗失败,已经证明很难从化疗中获益,且美国东部肿瘤协作组体能状态(ECOG-PS )评分>1分的患者,不推荐再次化疗。 化疗药物及方案 1一线化疗药物及方案 ADM和IFO是软组织肉瘤化疗的两大基石,一线化疗方案推荐ADM单药75 mg/m2,每3周为1个周期,不推荐增加ADM的剂量密度或序贯除IFO以外的其他药物。 表阿霉素(EPI)和聚乙二醇脂质体阿霉素(PLD)的不良反应,尤其是心脏毒性和血液学毒性均小于ADM,但治疗软组织肉瘤的疗效并不优于ADM。因此,对于患心脏基础疾病不适合使用ADM以及ADM已接近最大累积剂量的晚期软组织肉瘤患者,一线使用EPI和PLD的依据不足,有ADM化疗失败者使用PLD获益的报告。 与ADM相比,IFO无疗效和不良反应优势。对于无法耐受或拒绝蒽环类药物的患者,一线化疗可推荐IFO单药8~10 mg/m2,每3周为1个周期,不推荐大剂量IFO(12~14 g/m2)或持续静脉滴注作为辅助治疗。 与ADM单药化疗相比,ADM+IFO方案以及其他含ADM的联合化疗方案尽管可以提高有效率和无进展生存时间,但也增加了不良反应,并未显示出总生存优势。因此,不常规推荐作为一线辅助化疗。对于希望通过化疗尽快缩小肿瘤、缓解症状或因此而获取手术切除机会的
 1410人已读
1410人已读 - 射波刀联合贝伐单抗治疗复发高级别脑胶质瘤的 疗效与安全性
放射治疗已被证明是恶性胶质瘤最有效的辅助治疗之一,但内在放射敏感性和周围正常脑组织耐受剂量的限制,在这些肿瘤中可以从中受益是有限 的[1 ̄2]。通过提高局部脑肿瘤照射剂量以及使用放射增敏剂治疗,并没有
康静波 主任医师 中国人民解放军总医院第六医学中心 肿瘤诊疗中心3096人已读 - 图像引导多源γ射束立体定向放射治疗临床测试
[摘要]目的介绍图像引导的体部多源γ射束立体定向放射治疗系统性能测量。方法应用深圳市奥沃医学新技术发展有限公司生产的体部多源γ射束立体定向放射治疗系统及江苏瑞尔医疗科技有限公司的图像引导放射治疗定位系统,采用PTW ̄UNIDOS剂量仪、PTW0.6cc电离室、PTW0.125cc电离室、PTW0.015cc电离室、PTW ̄TW60008半导体探测器、EPSON10000XL背透光扫描仪、EBT2免冲洗放疗胶片,测量γ射束立体定向放射治疗定位参考点偏差、焦点剂量率、治疗计划软件三维图像重建位置误差以及系统综合定位精度。结果定位参考点偏差Δ=0.433mm,焦点吸收剂量率285.5Gy/min,三维图像重建位置误差0.8mm,综合定位精度最大值Δ=1.729mm。结论该图像引导的体部多源γ射束立体定向放射治疗系统符合国家标准要求。20世纪50年代初,瑞典Karolinska大学的Lek ̄sell教授首先研发使用γ射束立体定向放射治疗系统[1 ̄2]。2000年后,我国也研发出自主知识产权的γ射束立体定向放射治疗系统,该系统为多源立体定向放射治疗设备,同时用多个密封放射源对一个等中心进行辐照。放射治疗在肿瘤治疗中占有越来越重要的地位60%~70%的肿瘤患者需接受放射治疗。图像引导放射治疗(imageguidedradiotherapy,IGRT)是近十几年逐步发展起来的肿瘤精确放射治疗的最新理论和技术,通过先进的医学影像设备及图像处理方法对患者的病灶在治疗前和治疗中进行定位跟踪,实现对肿瘤的精确放射治疗,降低对肿瘤周边正常组织及关键器官的损伤,改善患者的治疗效果。图像引导是现代新兴放射治疗技术的基础,如立体定向神经放射外科手术、体部立体定向放射治疗(stereo ̄tacticbodyradiationtherapy,SBRT)、图像引导调强放射治疗。体部γ刀放疗系统采用γ射线多元几何聚焦方式,通过精确的立体定向,将经过治疗计划系统计算规划的一定剂量的γ射线从不同方向集中射于体内的预选靶区,聚焦效应使该点产生一个γ射线高剂量区,一次性或分几次摧毁靶区内的病变组织,以达到外科手术切除或损毁的效果,而靶区周边的正常组织和关键器官仅受到很小剂量的瞬时照射,基本不受损伤。体部γ刀自诞生以来,一直沿用机械框架和体表画线相结合的传统定位技术,然而体部γ刀系统需要精确图像引导定位,以满足SBRT对精度的要求。由江苏瑞尔医疗科技有限公司研发生产的IGPS-V型图像引导放疗定位系统,采用kV级X射线投影交角成像技术,用于体部γ刀以及其他放疗设备的精确图像引导定位。IGPS-V型系统采用的kV级X射线交角透视成像技术已成功应用于放疗中的图像引导定位多年,与电子直线加速器等多种放射治疗系统结合使用,技术成熟,临床应用广泛大量的临床数据已证实了其有效性和安全性。美国Accuray公司的CyberKnife目标定位系统和德国Brainlab公司的ExacTrac患者定位系统均采用类似的kV级X射线交角透视成像技术。CyberKnife和ExacTrac从2003年开始在全球得到广泛应用,到目前为止,在全球范围内已安装了近300台CyberKnife、600余台ExacTrac,已有数十万患者得到了安全、有效的治疗,并发表了几千篇技术和临床应用的学术论文。美国放射肿瘤学会和美国医学物理学家协会根据大量文献资料得到的临床应用历史数据,对SBRT的图像引导定位精度作了分析和总结,推荐符合SBRT要求的定位精度应≤1mm。IGPS-V型图像引导放疗定位系统在线校正、验证患者摆位实现图像引导体部肿瘤立体定向放射治疗。1材料与方法1.1材料采用深圳市奥沃医学新技术发展有限公司生产的体部多源γ射束立体定向放射治疗系统、江苏瑞尔医疗科技有限公司的图像引导放疗定位系统,以及PTW-UNIDOS剂量仪、PTW0.6cc电离室、PTW0.125cc电离室、PTW0.015cc电离室、PTW-TW60008半导体探测器、EPSON10000XL背透光扫描仪和EBT2(美国InternationalSpecialtyPro-ducts公司)免冲洗放疗胶片分别对焦点剂量率和绝对剂量精度进行测量。1.2方法根据临床质量保证和质量控制要求[3],测量定位参考点偏差、焦点剂量率、治疗计划软件三维图像重建位置误差、综合定位精度。1.2.1定位参考点偏差定位参考点偏差≤0.5mm测量方法:①把裁剪好的胶片装入焦点测量棒的暗盒腔内,用白色透明胶带固定,在胶片上标志方向并写上编号。②将胶片平面处在X ̄0 ̄Y平面,把焦点测量棒固定安装在测量支架上,预选足够辐照时间开启直径10mm准直器进床辐照。③辐照结束用焦点测量棒的专用扎针在胶片上扎出标志点胶片上的小孔作为定位参考点的机械中心位置重复以上3步,把胶片摆在X-0-Z方向进床辐照。1.2.2焦点剂量率水中的吸收剂量率不应小于2.0Gy/min用于测量的电离室和剂量仪应满足测量条件的要求[4 ̄12]将直径160mm的专用球形模体安装在定位支架上,模体中心位于定位参考点,插入电离室,使其有效测量点与模体中心重合将专用模体随治疗床送入预定辐射位置,使用最大聚焦野,开启辐照系统进行辐照辐照时间为t分钟,读取剂量计读数,计算焦点处相应于水中的吸收剂量Dwater。焦点处在水中的吸收剂量率DRate按式(1)计算[13]:DRate=Dwatert(1)其中,DRate为测量时刻最大聚焦野水中焦点吸收剂量率,单位为Gy/minDwater为最大聚焦野时模体内焦点处水中的吸收剂量,单位Gy利用式(2)将测量时刻水中的剂量率转换到初装源时刻的剂量率[14]:D0Rate=DRate.e0.693(T0-T1)/T1/2(2)其中,D0Rate为初装源时的焦点剂量率,T0为初装源的日期,T1为测量日期,T1/2为放射源衰变的半衰期对于钴 ̄60,T1/2=5.27年=1926d。1.2.3治疗计划软件三维图像重建位置误差治疗计划软件三维图像重建位置偏差≤1.5mm采用2个直径160mm有机玻璃球模、测量支架分别将2个直径160mm有机玻璃球模放置在测量支架上和负压袋(负压袋上的球模放上N型尺)上进行CT扫描,将扫描后的图片进行治疗计划设计计算出测量支架上球模中心的坐标与实际坐标的误差,分别计算出X、Y、Z3个方向上3个靶区的位置坐标,按式(3)计算治疗计划软件三维图像重建位置偏差:Δ=(3)式中:Δ为实际靶区中心与治疗计划软件重建靶区中心之间的距离,单位为mmΔX为X轴方向实际靶区中心与治疗计划软件重建靶区中心之间的距离,单位为mmΔY为Y轴方向实际靶区中心与治疗计划软件重建靶区中心之间的距离,单位为mm;ΔZ为Z轴方向实际靶区中心与治疗计划软件重建靶区中心之间的距离,单位为mm。1.3综合定位精度综合定位精度≤2.5mm采用一个直径160mm有机玻璃球模、负压袋/负压床、仿真体模(海军总医院射波刀仿真体模)、N型尺用胶片法测试,测试结果应符合企业标准中5.6.2的要求,胶片应采用低灵敏度的自显影胶片。测试步骤:(1)把球模/仿真体模连同测量专用的空暗盒装于负压定位床的A位置,送入CT机扫描(分别用N型尺定位和激光定位)。(2)把球模连同测量专用的空暗盒装于负压定位床的B位置,送入CT机扫描(分别用N型尺定位和激光定位)。(3)把球模连同测量专用的空暗盒装于负压定位床的C位置,送入CT机扫描(分别用N型尺定位和激光定位)。(4)根据CT片治疗计划系统分别采用4种方式(做4种计划)用1号准直器在靶点中心布靶:①扫描使用N型尺定位,治疗使用IGRT辅助定位;②扫描使用N型尺定位,治疗不用IGRT辅助定位;③扫描使用激光定位,治疗使用IGRT辅助定位;④扫描使用激光定位,治疗不用IGRT辅助定位计算出该中心在患者坐标系的坐标X0、Y0、Z0。(5)将X0、Y0、Z0经坐标转换后输出到服务器由控制机/IGRT计划软件读取。(6)把胶片放入暗盒中,将胶片粘牢于暗盒上,并用专用扎针在胶片上扎出标志点,作为靶点在胶片上的位置,将暗盒装进球模/仿真体模中。(7)分别把胶片、球模/仿真体模、负压袋装于治疗床上,并分别:①扫描使用N型尺定位,治疗使用IGRT辅助定位②扫描使用N型尺定位,治疗不用IGRT辅助定位③扫描使用激光定位,治疗使用IGRT辅助定位④扫描使用激光定位,治疗不用IGRT辅助定位用1号准直器进行辐照。(8)取出胶片,测量靶点中心对辐射野中心的偏离,即为在该方向的定位偏离把3个方向的偏离合成即得空间偏离。取4个靶点中心与辐射野中心的距离偏离值ΔX中的最大值、ΔY中的最大值、ΔZ中的最大值按式(4)计算靶点位置总误差:Δ=(4)式中:Δ为实际靶区中心与治疗计划软件重建靶区中心之间的距离,单位为mm;ΔX为X轴方向实际靶区中心与治疗计划软件重建靶区中心之间的偏离最大值,单位为mm;ΔY为Y轴方向实际靶区中心与治疗计划软件重建靶区中心之间的偏离最大值,单位为mm;ΔZ为Z轴方向实际靶区中心与治疗计划软件重建靶区中心之间的偏离最大值,单位为mm2,结果定位参考点偏差,△=0.433mm,小于0.5mm,合格(表1)焦点吸收剂量率平均值285.5Gy/min治疗计划软件三维图像重建位置误差;综合定位精度最大值Δ为1.729mm,小于2.5mm,合格。3结论辐射剂量学指标测量结果满足体部多源γ射束立体定向放射治疗系统要求。4讨论用0.6cc电离室可准确刻度直径30mm以上的聚焦野,能够得到准确的刻度参数[15]湿度修正(20%~70%):Kh=0.997;电离室照射量修正因子:Nx=1.003;离子收集非饱和修正因子:Ks=1;Katt为光子在电离室材料(包括平衡帽)中的吸收与散射的修正因子;Km为电离室材料非空气等效的修正因子:Katt×Km=0.975;有机玻璃与空气的组织本领比:So,air=1.120;扰动修正因子:Pu=1.02;电离室中心电极的非空气等效的修正因子:Pcel=1;水对有机玻璃的质能吸收系数:u/p=1.03;R-cGy转换因子=2.58×10-4×33.97=0.876由于0.6cc电离室体积过大,对于直径30mm以下的聚焦野测量不准用0.125cc电离室和0.015cc电离室,能准确测量直径30mm以上尺寸聚焦野胶片测量有待更深入研究对于直径30mm以上尺寸聚焦野,胶片测量也能测量准确;而对于直径30mm以下尺寸聚焦野,胶片测量效果则不理想采用半导体和电离室结合的测量方法,能较好地完成γ射束立体定向放射治疗质量控制中焦点剂量率和绝对剂量精度的测量,先用电离室测量准直径30mm以上尺寸聚焦野的焦点剂量率和绝对剂量精度,再由高灵敏度半导体测量出各个尺寸聚焦野的输出因子,推出各个尺寸聚焦野的焦点剂量率和绝对剂量,能较好地完成γ射束立体定向放射治疗质量控制工作。
康静波 主任医师 中国人民解放军总医院第六医学中心 肿瘤诊疗中心1455人已读
问诊记录 查看全部
- 肺癌 教授好!我爸这次的检查结果想麻烦您看看? 教授好!麻烦您看看我爸这次检查结果?总交流次数13已给处置建议
- 右肺下叶有1.0*1.5的结节 肺结节术后刚出病理 请大夫帮忙看看病理结果 请大夫帮忙看看病理 不知道后续怎么治疗总交流次数5已给处置建议
- 乳腺癌骨转移 发现左乳片状肿物2年一直没在意以为是腺体,2024.3.8体... 是否可以手术,怎么控制病情,最佳治疗方案,不能手术粒子治疗可不可以总交流次数3已给处置建议
- 肾癌根治术后 2021年8月份做右肾根治性切除后,术后病理显示透明细胞癌,... 属于哪个阶段?复发率和转移率是多少?寿命会受到影响吗?总交流次数13已给处置建议
- 三阴性乳腺癌术后一年结疗九个月复发出 三阴性乳腺癌术后一年半。结了九个月。出现胸壁转移灶,你做手术... 希望得到专家的化疗方案。总交流次数18已给处置建议
总访问量 8,019,486次
在线服务患者 851位
科普文章 1,257篇








