科室介绍 查看全部
科室医生 查看全部
-
神经内科

苏立凯
主任医师 教授
神经内科主任
神经内科
李会敏
主任医师 教授
内科主任
神经内科
张平
主任医师 教授
3.5
神经内科
代瑞廷
主任医师 教授
3.4
神经内科
王德超
主任医师 教授
3.4
神经内科
田文艳
主任医师 教授
3.4
神经内科
史福平
主任医师 教授
3.4
神经内科
邸卫英
副主任医师 副教授
3.4
神经内科
凌丽
主任医师 副教授
3.4
神经内科
张杏红
主任医师 教授
3.4
-
神经内科

高娟
主任医师
3.3
神经内科
李晓芳
副主任医师 副教授
3.3
神经内科
康增军
副主任医师
3.3
神经内科
王秀娟
主任医师
3.3
神经内科
李同凯
副主任医师
3.2
神经内科
姜晔
副主任医师
3.2
神经内科
王惠凌
副主任医师
3.2
神经内科
陈立英
主治医师
3.2
神经内科
宋月平
主治医师
3.2
神经内科
赵慧新
主治医师
3.2
-
神经内科

金鑫
主治医师
3.2
神经内科
曹巍
主治医师 讲师
3.2
神经内科
崔蕾
主治医师
3.2
神经内科
王铎
主治医师
3.2
神经内科
李宁
医师 助教
3.2
神经内科
陈雅静
医师
3.2
神经内科
任思敏
医师
3.2
科普·直播义诊专区 查看全部
- 精选 写给帕金森病人家属:如何照料帕金森病人
帕金森病,是一种渐进性神经退变疾病,病程逐渐进展,后期症状多,用药效果欠佳,如何照料帕金森病人往往家属带来很多烦恼和压力。 首先,作为帕金森病人的家属,要对疾病有基本的认知,帕金森病前期,运动障碍不显著,病人往往仅有轻微手颤,动作缓慢不明显,不会摔倒,生活可以自理,不需要家人陪伴。但有些病人会有嗅觉障碍,睡眠障碍,往往会有梦魇现象,这些都是帕金森病不典型症状。作为家属,需要细心观察患者,如果出现向后跌倒、男性性功能障碍、低血压等症状,则需要提防帕金森综合征可能,需要尽快再次就诊,以便尽早确诊。 其次,随着病情进展,帕金森病人出现逐渐加重的运动障碍,动作缓慢,转身障碍,易向前跌倒等,日常生活不能自理,需要家人陪伴。此外,在此阶段,病人逐渐调整用药种类和药量,往往会增加心理负担,认为“药吃多了减不下来”,而自行停药和减量,造成治疗障碍。家属在这阶段帮助病人要配合医生治疗,督促其按时服药。 在帕金森病后期,病人“开”期逐渐减少,且病程5年以上病人可能出现认知障碍,家属要及时观察,必要时需服用相关药物改善认知障碍。这个阶段服药种类多,家属要帮助病人正确服药。有些需要服用一半,或者四分之一的药物,可以把片剂研磨成粉末状以利分开服用。这阶段的病人往往神志清醒,精神压力大,更需要家属的安慰和支持。 本文系陈雅静医生授权好大夫在线(www.haodf.com)发布,未经授权请勿转载。
陈雅静 医师 河北大学附属医院 神经内科8959人已读 - 轻中度认知功能下降吃什么好?日常通过哪些途径改善?
很多人反映自己家老人近期出现记忆力减退的情况,说了没多久的话很快就忘了,有时还会重复提问。这种情况马虎大意不得,因为这些症状很有可能是轻中度认知功能下降的表现,即阿尔茨海默病(AD)的表现,需要及早到医院检查,确诊后及早治疗。可是,轻中度认知功能下降吃什么好? 轻中度认知功能下降吃什么好? 老年认知功能下降对患者、家庭及其照料者的生活都会产生重大影响。痴呆不是正常老化的一部分,其明显影响老年人的健康生活。目前尚无特效治疗方法逆转认知功能下降甚至痴呆的发生。随着微生态学的发展,大量科学证据表明肠道菌群可通过神经、内分泌、代谢及免疫等多种途径影响认知功能。 当出现轻中度认知功能障碍的相关表现时,比如:老人近期记忆减退、语言能力下降、判断能力受损、情绪不稳定、对周围环境兴趣减少、对人缺乏热情等等,需特别注意,早发现、早诊断、早治疗,此阶段被称为“黄金治疗窗口”,家属不容易发现,但此时治疗能够有效缓解病情,是黄金时期。 如果身边老人出现相关表现,应及时前往医院就诊。通过药物和非药物干预方式去减缓甚至逆转病情的进展。去年,我国新上市的药物甘露特钠胶囊(九期一),可用于“轻度至中度阿尔茨海默病,改善患者认知功能”。该药物通过重塑肠道菌群失衡,降低外周免疫细胞浸润,降低脑内神经炎症,减少脑内毒性蛋白沉积,进而改善认知障碍,使病情减速进展。 另外,日常通过哪些途径改善轻中度认知功能下降? 途径一:运动 运动干预对AD患者认知改善具有良好而稳定的效果。运动作为一种公认的改善认知的策略,不仅可以影响大脑相关的结构和功能,还能促进心血管系统的功能,增强身体健康,改善情绪;中等强度的有氧运动具有良好的耐受性和安全性。 途径二:多用脑 老年人要培养自己的兴趣爱好,例如画画、下象棋、写毛笔字等,多多学习、用脑,多与朋友交流,做益智类游戏。有医学类的研究表明,人在变老的同时,大脑也会随之萎缩,严重的时候就是出现记忆力不足、健忘等症状, 因此要多用脑,预防和改善大脑的功能退化。 途径三:饮食 在食物的营养成分中,水果、蔬菜和鱼类的消耗量与认知障碍的风险降低密切相关,较高的消耗量,特别是多酚和鱼类中的脂肪酸,可降低记忆功能衰退。 均衡和多样化的饮食是多酚和蛋白质的天然来源,无需额外补充。 途径四:情绪 保持心情愉悦,避免情绪的波动,家里人要经常跟老人沟通,否则老人没有倾诉对象很有可能造成抑郁、烦躁等负面情绪,不良的情绪将是阿尔茨海默病的导火索。 以上就是关于轻中度认知功能下降吃什么好的相关介绍,相信大家对此都有了一定的认识。轻中度认知功能下降,通过合理有效的药物治疗,再加上平时的调理,是能够控制病情进一步发展的。
王秀娟 主任医师 河北大学附属医院 神经内科2156人已读 - 为什么会得阿尔茨海默病?其发病机制是什么?
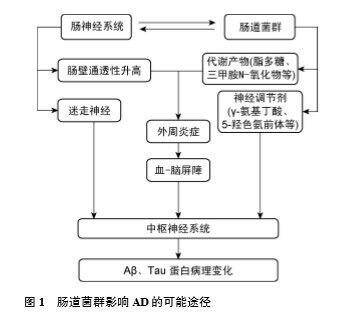
阿尔茨海默病(AD)在临床上又被称为老年痴呆症,是在1906年由一位德国医生首次发现并且报道的。该病的病理主要以神经炎性斑、神经元死亡以及神经原纤维缠结为主要的特征,属于一种慢性进行性的中枢神经系统退行性的病变。 病患在患病的初期会出现记忆方面的障碍,主要特征为对近期发生过的事情容易忘记以及记忆力受到损害。随着病患病情的不断加重,病患会出现失语、行为障碍、认知障碍以及失忆等现象,甚至逐渐丧失机体功能,最终导致死亡。 阿尔茨海默病的发病机制目前在临床上对于阿尔茨海默病的相关发病机制研究主要有以下几种说法,分别为胆碱能学说、tau蛋白假说、神经血管学说、氧化应激学说以及β-淀粉样蛋白瀑布学说、脑肠轴理论等,是否存在脑细胞外淀粉样肽β(amyloidβ,Aβ)沉积和细胞内Tau蛋白(tauprotein,Tau)过度磷酸化而神经原纤维缠结(neurofibrillarytangle,NFT)是该疾病的病理诊断标准,但AD的确切病因尚未明了,至今缺乏有效治愈AD的方法。 近年来报道AD的发生与肠道菌群改变有关,微生物和中枢神经系统相互作用的假说也成为AD发生的可能机制之一。 肠道菌群与中枢神经系统相互作用的基础———肠脑轴大脑和肠道微生物群之间通过脑‐内脏‐交感神经轴(脑肠轴)进行交流。脑肠轴由中枢神经系统、神经内分泌系统、免疫系统、自主神经系统的交感神经、副交感神经分支、肠神经系统和肠道微生物群构成。 肠道与大脑之间的沟通主要有3种方式: 1、传入神经纤维,通过神经免疫调控和利用神经内分泌途径。 2、肠道微生物群参与调控大脑的许多功能,例如:细菌通过迷走神经和肾 上腺素能神经等多种通讯方式,调控外周神经系统和中枢神经系统的活动。 3、调节下丘脑‐垂体‐肾上腺(hypothalamic pituitary adrenal,HPA) 轴的激活状态,HPA轴受刺激而释放皮质醇,进而控制脑小胶质细胞的活化状态;影响细胞因子的释放及单核细胞从外周向大脑的迁移;产生神经递质、神经肽和激素等多种物质,影响宿主的精神健康。 另外,脑损伤及不同的心理状态均可影响肠道微生物群的组成,并可能诱发疾病。如卒中引起的脑损伤被证明会改变小鼠盲肠菌群的组成,表现为普雷沃菌科显著降低,肠球菌科比例升高,并与脑损伤的严重程度呈正相关。 肠道菌群影响AD的可能机制肠道菌群可通过包括代谢产物、神经递质及慢性神经炎症等多途径,影响AD的发生。 1. 肠道菌群影响AD的可能机制 肠黏膜屏障在保持吸收营养能力的同时,还能阻隔有害物质进入体内环境, 在衰老过程中,肠黏膜屏障和血‐脑屏障的通透性也会增高。Leblhuber等通过高效液相色谱分析发现AD患者血液中的钙网蛋白浓度显著升高,表明钙网蛋白可穿过紊乱的肠道屏障功能,从肠道进入循环系统导致神经炎症。提示肠道菌群产生的有害代谢产物,可穿过血‐脑屏障损害神经元的功能。 2.肠道菌群通过神经递质影响AD 压力和情绪会导致大脑通过释放激素或神经递质影响肠道微生物组成,肠道菌群也可通过产生神经递质前体或调节神经递质,影响大脑功能,比如,5-羟色胺(5‐HT)是一种单胺类神经递质,在调节认知、学习、记忆和许多生理过程中起重要的作用,超过95%的5‐HT在肠道中合成。 3. 肠道菌群与慢性神经炎症 炎症反应对大脑既有利又有害。一方面,慢性、轻度TLR4刺激可通过激活 神经元自噬来减少Tau蛋白的过磷酸化;另一方面,炎症在AD的发展过程中起促进作用。 肠道微生物群可通过激活宿主的先天免疫系统 ,从而增强对脑内Aβ的炎症反应,导致神经炎症。 阿尔茨海默病的风险因素衰老、遗传、家族史、性别均是影响AD不可干预的危险因素,心脑血管疾病、血压、血脂、2型糖尿病、体质量、体力活动与脑力、脑外伤、吸烟、饮酒、饮食、情绪、受教育水平等都是影响AD可干预的危险因素。 其中,环境因素如饮食失衡,抗生素的滥用和生活方式的改变,都可能通过肠道微生物群的改变,而引起外周和中枢神经系统炎症,导致认知功能下降或障碍。(或者其他一些疾病、长久服药也可能直接或间接导致肠道微生物群发生改变,而且老年人肠道微生物的多样性本身是降低的。) 综上,认为肠道菌群紊乱所诱发的神经炎症是阿尔茨海默症的重要发病机制,治疗用药甘露特钠胶囊(九期一)的作用机制是通过重塑肠道菌群失衡,降低脑内神经炎症,从而改善认知功能。这为抗AD药物研发策略提供了新的思路,填补了该领域17年无新药上市的空白。
 王秀娟 主任医师 河北大学附属医院 神经内科7567人已读
王秀娟 主任医师 河北大学附属医院 神经内科7567人已读
问诊记录 查看全部
- 胸闷,心跳快,突然的背部燥热,手心出汗 多年前就身体燥热,出汗,有甲亢,目前甲亢指标正常,但是燥热出... 请主任帮我看看我这个是不是交感神经的毛病,需要怎么治疗,认为阴虚中药也吃了好多,不知道怎么查这个病了总交流次数19已给处置建议
- 帕金森 81岁,女性,认知和智力正常,且比2年前好。
2年前202... 今天服用金刚烷胺,下午上厕所又坐不下1次,走路定住半小时总交流次数5已给处置建议
- 头疼头晕,左下肢无力半年 2022年9月5日临汾中心医院住院治疗14天,10月24日复... 评估一下脑梗的具体原因情况及治疗用药总交流次数15已给处置建议
- 体检生化14项,血脂高,冠状动脉颈动脉粥 体检发现血脂高,动脉粥样硬化,请问需要什么药物降血脂? 用什么药物控制?总交流次数7已给处置建议
- 头晕,昏昏沉沉,头顶发紧,有压榨感。 头晕,难受严重的时候感觉从腋窝开始到头顶都发紧,有压榨感,感... 想知道患者的病情和CTA检测所述是否有关,都需要什么治疗能缓解症状?总交流次数6已给处置建议
总访问量 1,430,399次
在线服务患者 1,806位
科普文章 3篇



